veröffentlichende Fachgesellschaft: Japanese Society of Anesthesiologists (JSA)
Klassifikation gemäß AWMF:
Datum der Veröffentlichung: 08.01.2026
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.1007/s00540-025-03647-y
Grundsätzliches
- maligne Hyperthermie (MH) ist eine erbliche Muskelerkrankung
- Inzidenz der MH liegt bei 0,18 – 3,9 Fällen pro 100.000 Allgemeinanästhesien
- mehr als die Hälfte der über gemeldenten 600 MH-Fällen in Japan betraf Personen < 18 Jahren, wobei das Verhältnis von Männern zu Frauen etwa 3:1 beträgt
- Häufigkeit von Personen mit latenter Prädisposition (Träger einer ursächlichen Genvariante) ist deutlich höher als die Inzidenz klinischer Episoden und liegt zwischen etwa 1:856 und 1:1075
- Mortalitätsrate bei MH sank deutlich von 70 – 80 % in den 1960er Jahren auf 0 – 18,2 % im Jahr 2010 (Mortalitätsrate bei Patient*innen mit Dantrolen-Theapie bei ≤ 10 %)
Pathophysiologie
- Mechanismus der Calciumionen (Ca2+)-induzierten Ca2+-Freisetzung (CICR) aus dem sarkoplasmatischen Retikulum (SR), dem Ca2+-Reservoir in den Skelettmuskelzellen, in das Zytoplasma ist bei Betroffenen abnormal beschleunigt
- ersten MH-Symptome sind unerklärlicher Anstieg des endtidalen Kohlendioxids (etCO2
> 55 mmHg), unerklärliche Tachykardie und Muskelrigidität, v.a. des Musculus masseter (Schwierigkeiten beim Öffnen des Mundes) - zusätzlich rascher Temperaturanstieg (> 0,5 °C/15 min) mgl., wobei die KKT potenziell bei > 40 °C liegt
- schwere respiratorische und metabolische Azidose (BE ≤ – 8,0 mmol/L), Herzrhythmusstörungen und cola-farbener Urin (Myoglobinurie aufgrund von Muskelabbau) ebenfalls mgl.
- Serumkaliumspiegel ggf. erhöht –> ggf. spitze T-Wellen im EKG sichtbar (CAVE: Gefahr von Herzstillstand)
- Komplikationen wie disseminierte intravaskuläre Koagulopathie und Nierenversagen mgl.
- alle volatilen Inhalationsanästhetika, inkl. Sevofluran und Desfluran, sowie depolarisierende Muskelrelaxanzien wie Suxamethonium sind dafür bekannt, ein MH-Auslöser zu sein
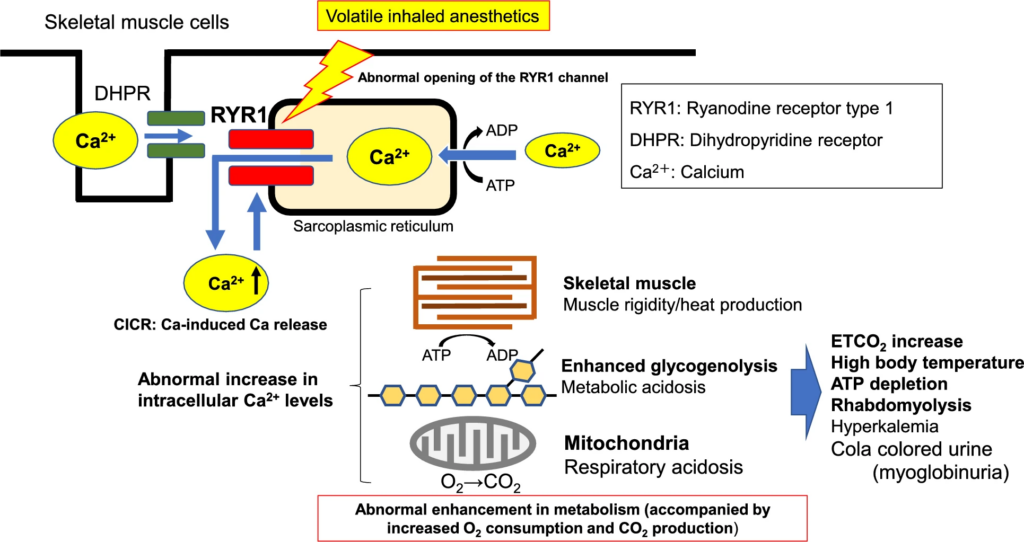
- Dantrolen wirkt als Antidot auf die Ca²⁺-Freisetzungskanäle (RYR1) im sarkoplasmatischen Retikulum (SR) von Skelettmuskelzellen und hemmt so die Ca²⁺-Freisetzung –> Dantrolen blockiert nicht die postsynaptischen Acetylcholinrezeptoren, sondern entfaltet seine Wirkung direkt in den Skelettmuskelzellen
Management intra- und postoperativer MH
- Gabe von Dantrolen ist v.a. bei Vorliegen von Frühsymptomen (erhöhtes etCO₂ trotz erhöhter Atemminutenventilation, unerklärliche Tachykardie, Hyperthermie oder Muskelrigidität) indiziert
- Managementalgorithmus für maligne Hyperthermie (MH)
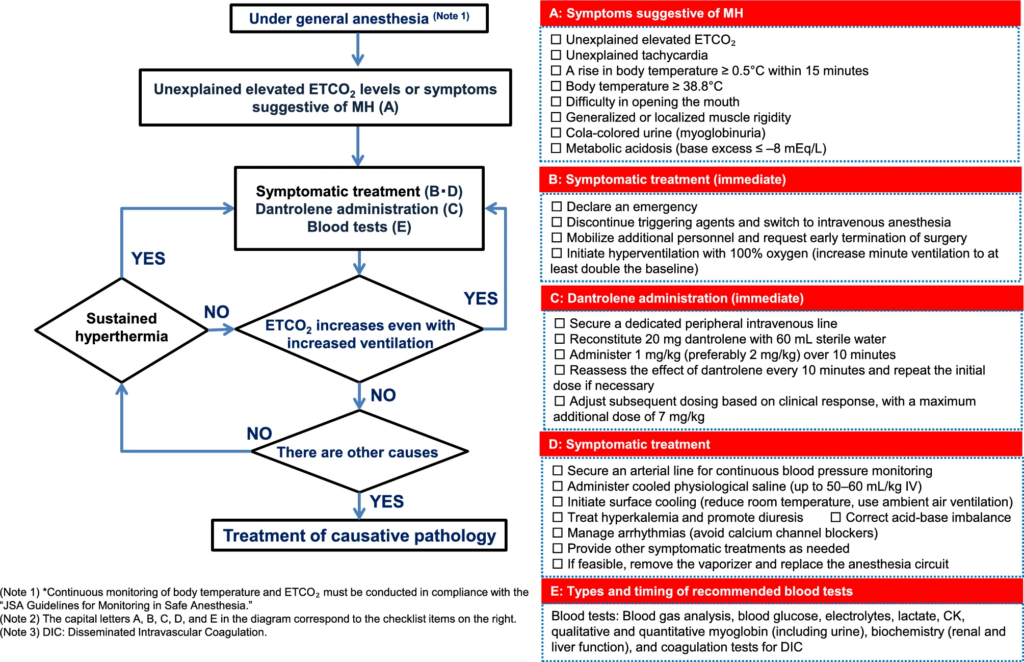
Vorgehen bei MH-Krise
- Verabreichung von auslösenden Substanzen wie volatilen Inhalationsanästhetika oder Suxamethonium sofort einstellen und auf i.v.Anästhesie und nicht-depolarisierende Muskelrelaxanzien umzustellen
- MH-Notfall kommunizieren, zusätzliche Hilfe anfordern und Chirurg*n bitten, die Operation umgehend abzuschließen
- hochdosierte Gabe von reinen Sauerstoff (≥ 10 L/min), um Hyperventilation durchzuführen (AMV mind. doppelt so hoch wie der Normalwert), um Anästhetikakonzentration im Beatmungssystem zu reduzieren
- Dantrolen vorbereiten (sichergestellte Bevorratung einer Gesamtdosis von bis zu 7,0 mg/kg)
- Inhalt der 20-mg-Dantrolen-Ampulle in 60 mL destilliertem Wasser für Injektionszwecke auflösen und Lösung schütteln, bis sie klar ist
- Dantrolen über separaten großlumigen peripheren Venenkatheter verabreichen (Gabe von mind. 1,0 mg/kg, bezogen auf das tatsächliche Körpergewicht, über ca. 10 min; vorzugsweise 2,0 mg/kg über ca. 10 min)
- Gabe nach Bedarf wiederholen bis eine Senkung des etCO₂-Wertes und KKT sowie eine Besserung der Muskelrigidität eintreten
- Beurteilung alle 10 min, bis die MH-Symptome abklingen (max. Dosis von 7,0 bis > 10 mg/kg, je nach Literatur)
- arteriellen Zugang für BGA etablieren, um Grad der metabolischen Azidose zu bestimmen
- Gabe gekühlter physiologischer Kochsalzlösung i.v. zur Senkung der Körpertemperatur (max. Volumen: 50 – 60 mL/kg)
- Raumtemperatur senken und Körperoberfläche aktiv mit Raumluft kühlen (stemische Kühlung beenden, sobald die KKT < 38 °C)
- Hyperkaliämie nach Bedarf behandeln (Glukose-Insulin-Therapie sowie Gabe von Calciumgluconat und Natriumbicarbonat erwägen
- forcierte Diurese mit Furosemid anstreben (Ziel-Urinmenge: 1,0 mL/kg/h)
- metabolische Azidose sachgemäß behandeln und Gabe von Natriumbicarbonat erwägen (Natriumbicarbonat zur Förderung der Harnalkalisierung bei erhöhten CK-Werten oder cola-farbenem Urin (Myoglobinurie))
- Arrhythmien klinisch indiziert behandeln (CAVE: keine Kalziumkanalblocker; Amiodaron oder Betablocker in Betracht ziehen)
- unterstützende oder symptomatische Behandlungen, sofern klinisch indiziert
- zur Beurteilung des Patient*innenzustandes folgende Blutuntersuchungen durchführen:
- arterielle BGA: BZ, Elektrolyte, Laktat, CK
- qualitative und quantitative Myoglobinbestimmung (inkl. Urin)
- biochemische Tests (Nieren- und Leberfunktion)
- Gerinnungstests zur Diagnose einer DIC)
- CAVE: Auftreten eines Rezidiv einer malignen Hyperthermie ist möglich
- klinische Verbesserung bei MH anhand von Trends beurteilen, wie z.B. sinkende oder normalisierte etCO2-Werte, Stabilisierung der Herzfrequenz oder weniger Arrhythmien, Rückkehr zur Normothermie ohne die Notwendigkeit einer aktiven Kühlung und Auflösung der Muskelrigidität


kurze Anmerkung zum Dantrolen:
das erwähnte Dantrolen 20mg ist in Deutschland nicht mehr bestellbar. Der Nachfolger AGILUS® enthält 120mg pro Ampulle ist besser löslich und es müssen entsprechend der höheren Wirkstoffkonzentration nicht mehr 7 oder mehr Flaschen aufgelöst werden sondern nur noch 1-2 Flaschen!