veröffentlichende Fachgesellschaft: American Heart Association (AHA)
Klassifikation gemäß AWMF:
Datum der Veröffentlichung: 26.01.2026
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.1161/STR.0000000000000513
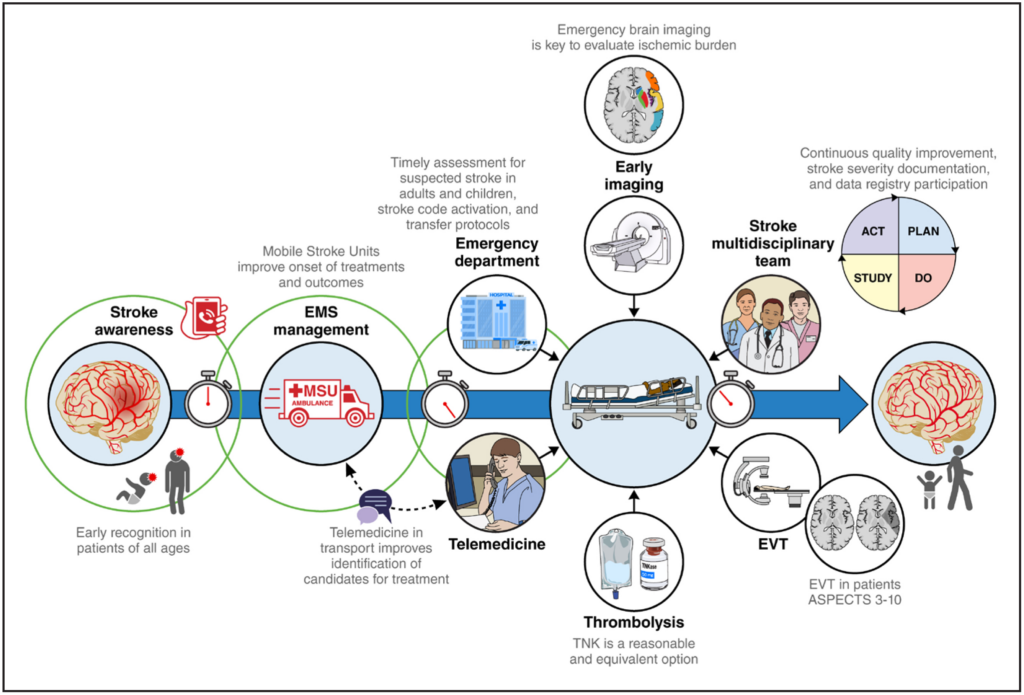
Stroke-Versorgungssysteme & präklinische Versorgung
Stroke Awareness
- Durchführung von Aufklärungskampagnen zur Erkennung von Schlaganfällen für alle Altergruppen in der breiten Öffentlichkeit (Gestaltung, die auch verschiedene soziale Gruppen und Bevölkerungsgruppen erreicht)
- Aufklärungskampagnen auch so gestalten, dass sie langfristig das Wissen über die Warnzeichen eines Schlaganfalls verbessern
- gezielte Aufklärungskampagnen für med. Personal, um Verzögerungen vor KH-Einlieferung zu reduzieren und die Eignung für eine akute Behandlung des ischämischen Schlaganfalls (z. B. Thrombolyse) zu maximieren
Rettungsdienst-System
- Einrichtung regionaler Systeme für die Schlaganfallversorgung, um den Zugang zur raschen Therapieeinleitung zu verbessern mit Klassifizierung in
- Kliniken mit Notfallversorgung, inkl. i.v.-Lyse-Therapie
- Kliniken mit Notfallversorgung, inkl. i.v.-Lyse-Therapie und Thrombektomie
- Entwicklung von Protokolle für die Triage vor KH-Einlieferung, um sicherzustellen, dass Patient*innen mit V.a. Schlaganfall schnell identifiziert, mit einem validierten Screening-Instrument untersucht und vorrangig in die bestgeeignete Klinik transportiert werden
- Überwachung und Rückmeldung von Qualitätskennzahlen im Zusammenhang mit der präklinischen Versorgung, um Verzögerungen zu reduzieren und das Outcome zu verbessern
präklinische Beurteilung und Behandlung
Leitstelle
- Einsatz telefonischer Schlaganfall-Bewertungstools durch die Rettungsleitstelle ist sinnvoll und kann zur frühzeitigen Schlaganfall-Erkennung mit Verkürzung der präkl. Zeiten beitragen
rettungsdienstliche Versorgung und Transport
- Einsatz schneller Schlaganfall-Screeningtools zur Schlaganfall-Erkennung (inkl. LVO-Stroke)
- telefonische KH-Voranmeldung zur Verkürzung der Behandlungszeiten
- keine Verbesserung des funktionellen Outcomes durch und daher keine Empfehlung für Remote Ischemic Conditioning in der Präklinik (nicht-invasive Therapiemethode, bei der mithilfe automatisierter Blutdruckmanschetten an den Extremitäten kurze, abwechselnde Zyklen von Ischämie und Reperfusion erzeugt werden)
- keine Verbesserung des funktionellen Outcomes durch transdermale Glyceryltrinitrat-Applikation in der Präklinik (CAVE: potenziell schädlich)
- präklinische Blutdruckkontrolle mit Zielwerten von RRsys 130 – 140 mmHg verbessert das funktionelle Outcome nicht
- Nutzen von Schlaganfall-Screeningtools für Erwachsene bei pädiatrischen Patient*innen ist ungewiss –> gute Interrater-Reliabilität für neuere Screening-Instrumente für Kindern, jedoch noch keine Validierung in der Präklinik
Zielklinik-Auswahl
Grundsätzliches
- Transport in nächstgelegene geeignete Klinik mit Stroke Unit bei V.a. akuten Schlaganfall priorisieren
Gebiete mit lokalem Zugang zu Thrombektomie-fähigen Schlaganfallzentren
- bei V.a. LVO-Schlaganfall kann der direkte Transport in Thrombektomie-fähiges Schlaganfallzentrum vorteilhaft, um Thrombektomie-Rate zu erhöhen und Zeit bis zur Therapie zu verkürzen
Gebiete ohne lokalem Zugang zu Thrombektomie-fähigen Schlaganfallzentren
- in Gebieten ohne gut koordinierte Schlaganfallversorgungssysteme und lokale Thrombolyse- & Thrombektomie-fähige Schlaganfallzentren kann es sinnvoll bei LVO-Schlaganfall sein den direkte Transport in das nächstgelegene geeignete Thrombektomie-fähige Schlaganfallzentrum zu erwägen (CAVE: sofern der Transport die Patient*innen nicht von einer i.v.-Lyse-Therapie ausschließt)
- in Gebieten mit gut koordinierten Schlaganfallversorgungssystemen und lokalen KH mit Erfahrung in Thrombolyse und der Möglichkeit einer sekundären Verlegung, verbessert der direkte Transport bei V.a. LVO-Schlaganfall in ein entfernteres (z. B. 45 – 60 Minuten) Thrombektomie-fähiges Schlaganfallzentrum im Vergleich zum Transport in lokale Schlaganfallzentrum die klinischen Ergebnisse nach 3 Monaten nicht
Krankenhausverlegung
- Treffen von Vereinbarungen und Festlegung von Protokollen durch KH’s und RD’s, um die Verlegung von Patient*innen mit akutem Schlaganfall zu priorisieren und so die Door-in-Door-out-Zeiten zu verkürzen
Rolle mobiler Stroke Units
- Einsatz mobiler Schlaganfall-Einheiten (MSU) bei V.a. akuten ischämischen Schlaganfall anstatt herkömmlicher RTWs empfohlen, sofern diese verfügbar sind, um Transport und Behandlung von Patient*innen, die für eine Thrombolyse in Frage kommen, zu gewährleisten
- MSU müssen mit intravenöser Thrombolyse ausgerüstet sein
- MSU-Versorgung für die Notfalldiagnostik & -therapie der Symptome ohne Sicherheitsbedenken von Vorteil
- bei Patient*innen, die für eine Thrombektomie in Frage kommen, kann der MSU-Einsatz von Vorteil sein, um diese Patient*innen zu identifizieren und direkt in geeignete Klinik mit Thrombektomie-Möglichkeit zu transportieren
Kompetenzen von Krankenhäusern im Bereich Schlaganfall
- für KHs, die akute ischämische Schlaganfälle (AIS) versorgen, wird eine Zertifizierung als Spezialklinik (Stroke Unit o.Ä.) empfohlen
Notfalluntersuchung bei V.a. Schlaganfall (inkl. Notaufnahme und Schlaganfallteams)
- Patient*innen aller Altersgruppen mit akuten neurologischen Ausfällen sollten von standardisierten, notfalldiagnostischen Protokollen im Hinblick auf frühzeitige Erkennung und Behandlung profitieren
- bei pädiatrischen Patienten mit plötzlich auftretenden und anhaltenden fokalen neurologischen Ausfällen (inkl. erstmaligen Krampfanfällen), akuten Schlaganfall vermuten, um rechtzeitige Diagnose zu ermöglichen
- Einrichtung von Akut-Schlaganfallteams, bestehend aus Ärzt*innen, Pflege und Labor-/Radiologiepersonal, um sorgfältige klinische Beurteilung (inkl. neurologische Untersuchung) sicherzustellen
- Entwicklung und Ausbildung multidisziplinärer Schlaganfallteams mit Schlaganfall-Fachwissen, um die Rate der iv.-Lyse-Therapie sicher zu erhöhen
- Thrombolyse- & Thrombektomie-geeignete Patient*innen sollten von Schlaganfallteams profitieren, um die schnellstmögliche Zeit vom Auftreten bis zur Therapie zu gewährleisten und das bestmögliche klinische Outcome zu erreichen
Telemedizin
präklinische Telemedizin
- bei V.a. Schlaganfall vor KH-Einlieferung, sofern möglich, Telemedizin im RTW erwägen, um die präklinische Beurteilung zu ergänzen und Kandidat*innen für Reperfusionsmaßnahmen zu identifizieren
Teleradiologie
- tele-radiologische Systeme für Notaufnahmen ohne interne Bildauswertungsexpertise empfohlen, um zeitnahe Auswertung der Hirnbildgebung zu ermöglichen
Telemedizin für Entscheidungsfindung über Thrombolyse und deren Durchführung
- Telestroke-Systeme sind ggü. der üblichen Versorgung durch Notaufnahmeteam bei Entscheidung über i.v.-Thrombolyse und optimale Thrombolyse-Durchführung wirksamer bei AIS-Patient*innen in Notaufnahmen ohne neurologische Fachabteilung
- Telestroke-Systeme sind in Notaufnahmen ohne neurologische Fachabteilung sinnvoll, um die kurzfristige Mortalität zu senken
- Entscheidungsunterstützung durch telefonische Beratung mit Schlaganfallspezialist*innen kann bei AIS-Patient*innen in Notaufnahmen ohne neurologische Fachabteilung und Telestroke-Systeme von Vorteil sein
Telemedizin in Versorgungssystemen für Schlaganfälle
- Unterstützung für Einsatz von Telemedizin-/Telestroke-Ressourcen und -Systemen durch Gesundheitseinrichtungen, staatliche Kostenträger und Anbieter, um angemessene Abdeckung rund um die Uhr an sieben Tagen in der Woche sicherzustellen
- Einsatz von Telestroke-Systemen kann bei AIS-Patient*innen in Notaufnahmen ohne neurologische Fachabteilung sinnvoll sein, die für eine Verlegung zwecks Notfall-Thrombektomie anstelle einer lokalen Versorgung in Frage kommen
Organisation und Integration von Komponenten
- Beteiligung von Krankenhäusern als regionalen Schlaganfallversorgung-Systemen, bestehend aus zertifizierten KHs und RDs, um gute & zeitnahe Versorgung bei der akuten Schlaganfallversorgung zu ermöglichen bzw. zu optimieren
- Entwicklung von Protokollen für Verlegungen in KH mit 24/7-Thrombektomie-Möglichkeit, um schnelle, sichere und effiziente Verlegung von Thrombektomie-Kandidat*innen zu gewährleisten
- primäre Stroke Units ohne 24/7-Thrombektomie-Möglichkeit sollten in der Lage sein, schnell eine intrakranielle Gefäßbildgebung (Angio-CT oder Angio-MRT) durchzuführen und auszuwerten, um Patient*innen mit LVO zu identifizieren, die für EVT in Frage kommen
- Entwicklung und Einführung von Behandlungsprotokollen in KHs, die Patient*innen mit akutem Schlaganfall versorgen, welche den aktuellen klinischen Leitlinien entsprechen
- Entwicklung von Protokollen für die umfassende Erfassung wichtiger Zeitparameter und anderer für die Thrombektomie relevanter Behandlungsprozesse sowie die langfristigen Patientenergebnisse in Stroke Units mit Thrombektomie-Möglichkeit
- Stroke Units mit Thrombektomie-Möglichkeit sollten Neurointerventionist*innen anhand festgelegter & klar vereinbarter Ausbildungs- & Zertifizierungsstandards zertifizieren
- je nach den Merkmalen der lokalen und regionalen Versorgungssysteme kann auch die Einrichtung mobiler Interventionsteams in Betracht gezogen werden für eine zeitnahe Thrombektomie
Schlaganfallregister, Qualitätsverbesserung und Risikoanpassung
- KHs mit Stroke Unit sollten multidimensionale Qualitätsverbesserungs-Prozesse durchführen, die die kontinuierliche Überwachung, Überprüfung und Rückmeldung von Qualitätsindikatoren, Benchmarks und evidenzbasierten Praktiken für Schlaganfälle umfassen, um die Versorgungqualität zu erhöhen
- Beteiligung aller KHs mit Stroke Unit an Schlaganfall-Datenregistern, um die Einhaltung von Qualitätsindikatoren und Leitlinienempfehlungen zu verbessern und Behandlungsergebnisse zu optimieren
- KHs mit Stroke Unit sollten den Schlaganfallschweregrad bei allen Patient*innen messen und dokumentieren (z. B. NIHSS-Score), damit die zur Vergleichung der Krankenhausleistung verwendeten Risikoanpassungsmodelle ausreichend genau und zuverlässig sind
Notfall-Diagnostik & -Therapie
Schlaganfall-Skalen
- Verwendung von Skalen zur Bewertung des Schlaganfallschweregrads (vorzugsweise NIHSS), um klinische Defizite zu Beginn und nach Reperfusionstherapien zu messen
initiale vaskuläre & multimodale Bildgebungsverfahren
Evaluation für i.v.-Thrombolyse
- Notfall-Hirnbildgebung mittels CT ohne Kontrastmittel oder MRT als Erstdiagnostik bei V.a. AIS, um ischämische Belastung (z.B. ASPECTS) zu beurteilen und ICB vor Reperfusion auszuschließen
- Stroke Units sollten Protokolle auf Grundlage von Prozessverbesserungsinitiativen festlegen, damit eine Notfall-Hirnbildgebung so schnell wie möglich (z.B. innerhalb von 25 min) für rechtzeitige Reperfusion durchgeführt werden kann
- Notfall-Hirnbildgebung mit CT-Angio und/oder Perfusions-CT bei V.a. AIS und LVO nicht verzögern, wegen der Serumkreatininkonzentration-Bestimmung
- Notfall-Hirnbildgebung mit MRT/Angio-MRT der zervikalen und intrakraniellen Gefäße bei pädiatrischen Patient*innen mit V.a. AIS sinnvoll, um große Gefäßokklusion zu identifizieren und arteriellen ischämischen Schlaganfall von hämorrhagischem Schlaganfall oder Schlaganfall-Mimics zu unterscheiden
- Notfall-Hirnbildgebung mit CT/Angio-CT der zervikalen und intrakraniellen Gefäße bei pädiatrischen Patient*innen mit Verdacht auf AIS, wenn MRT/Angio-MRT nicht sofort verfügbar ist (innerhalb von 25 min), um große Gefäßokklusionen zu identifizieren
- bei V.a. AIS als Wake-up-Stroke oder mit Symptombeginn vor > 4,5 h, bei dem Thrombolyse in Frage kommt, kann die Auswahl anhand eines Mismatch zw. MRT-DWI und FLAIR hilfreich sein, um die Eignung für eine i.v.-Thrombolyse mit verlängertem Zeitfenster zu bestimmen
- bei V.a. AIS als Wake-up-Stroke oder mit Symptombeginn vor 4,5 – 24 h kann die Auswahl von Perfusions-CT oder MR DWI-PWI (perfusionsgewichtete Bildgebung) mit automatisierter Nachbearbeitungssoftwareanalyse hilfreich sein, um die Eignung für i.v.-Thrombolyse mit verlängertem Zeitfenster zu bestimmen
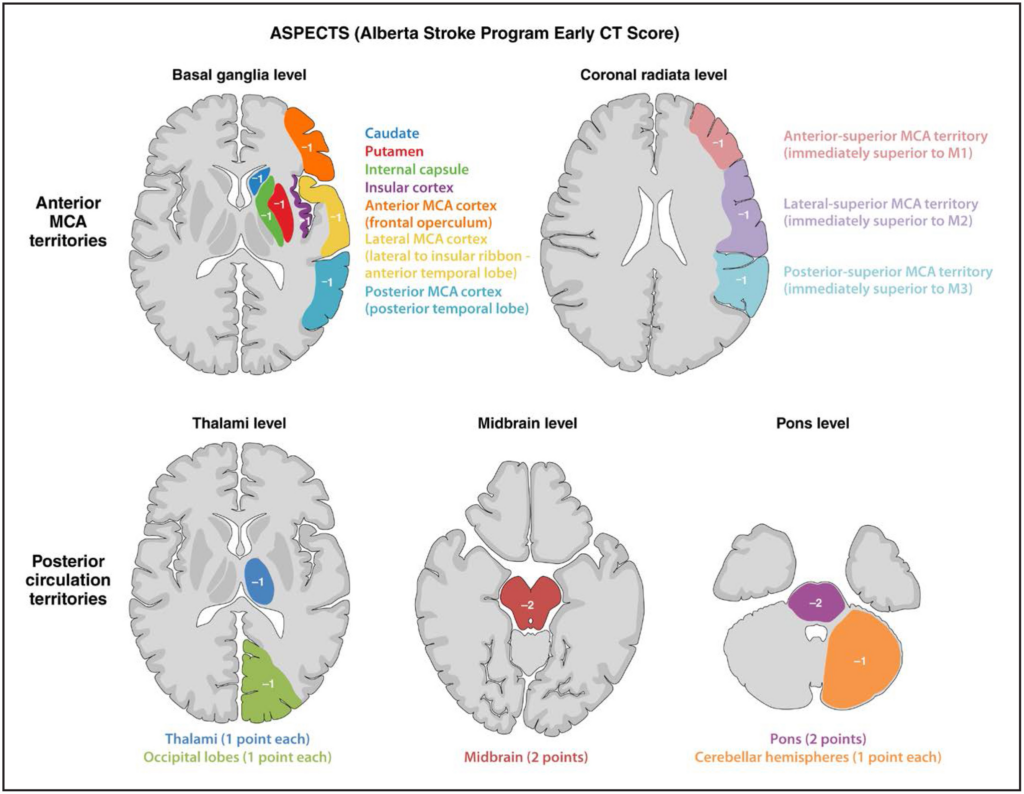
Evaluation für endovaskuläre Thrombektomie (EVT)
- bei V.a. AIS und LVO, die sich innerhalb von 24 h nach dem letzten bekannten gesunden Zustand vorstellen, so schnell wie möglich Notfall-Hirnbildgebung der zervikalen und intrakraniellen Gefäße (CT/CT-Angio oder MRT/Angio-MRT), um die EVT auszuwählen und die Behandlung zu planen
- bei V.a. AIS und LVO, die sich innerhalb von 6 – 24 h nach dem letzten bekannten gesunden Zustand vorstellen, kann ein zusätzliches Perfusions-CT, MRT (DWI-FLAIR-Mismatch) oder MR DWI-PWI mit automatisierter Nachbearbeitungssoftwareanalyse bei der Beurteilung bzgl. EVT-Eignung hilfreich sein, sofern diese sofort verfügbar ist
- bei V.a. AIS und LVO aufgrund präklinischer Beurteilung mit validierter Schlaganfall-Schweregradskala (z.B. RACE > 4) und EVT-Eignung kann der direkte Transport in den Angiographie-Raum für Flachbild-Kopf-CT anstelle des herkömmlichen Bildgebungs-Workflows mit anschließender kathetergestützter Angiographie in Betracht gezogen werden, um Zeit bis zur Intervention zu verkürzen und das funktionelle Outcome zu verbessern
- bei V.a. AIS aufgrund von LVO (basierend auf Bildgebung oder klinischer Beurteilung) und Eignung für EVT kann der direkte Transport in den Angiographie-Raum ohne wiederholte Hirn-Bildgebung bei Ankunft im Thrombektomiezentrum in Betracht gezogen werden (sofern keine klinischen Veränderungen oder Verzögerungen beim Transport vorliegen)
andere diagnostische Tests
- Basis-EKG bei V.a. akuten Schlaganfall empfohlen, sollte aber Beginn der i.v.-Thrombolyse oder EVT nicht verzögern
- Troponin-Testung bei V.a. akuten Schlaganfall empfohlen, sollte aber Beginn der i.v.-Thrombolyse oder EVT nicht verzögern
allgemeine unterstützende Frühbehandlung
Atemwegssicherung, Atmung & Oxygenierung
- je nach Bedarf Atemwegssicherung und Beatmungshilfe bei Patient*innen mit akutem Schlaganfall und Bewusstseinsstörungen oder bulbären Funktionsstörungen
- bei AIS und Hypoxie zusätzlich O2-Gabe, um SpO2 > 94 % aufrechtzuerhalten
- bei AIS mit Beginn < 6 h, NIHSS-Score von 10 – 20, CT-ASPECTS-Score ≥ 6 und LVO des vorderen Kreislauf (M1 oder Karotis-Terminus) mit geplanter EVT (mit/ohne IVT) kann normobare Hyperoxie vor EVT sinnvoll sein
- bei AIS aufgrund LAE kann hyperbare O2-Therapie sinnvoll sein
- bei AIS ohne Hypoxie, der nicht für EVT in Frage kommt, keine zusätzliche O2-Gabe zur Verbesserung des funktionellen Outcome empfohlen
- bei AIS, der nicht mit Luftembolie assoziiert ist, keine hyperbare O2-Therapie zur Verbesserung des funktionellen Outcome empfohlen
Kopfpositionierung
- kein Vorteil einer routinemäßigen 0°-Kopfpositionierung im Vergleich zu einer 30°-Positionierung über 24 h in Bezug auf die Verbesserung des funktionellen Outcomes
- bei AIS, deren Ursache wahrscheinlich eine Arteriosklerose der großen Arterien ist und für die keine Reperfusionsintervention verfügbar ist, gibt es keinen Vorteil einer routinemäßigen Trendelenburg-Positionierung (−20°) im Vergleich zu einer 0°- bis 30°-Kopfpositionierung hinsichtlich der Verbesserung des funktionellen Outcomes
Blutdruckmanagement
allgemeine Empfehlungen (auch ohne Reperfusionstherapie)
- Hypotonie und Hypovolämie korrigieren, um ausreichende Perfusion für Organfunktion zu gewährleisten
- frühzeitige Hypertonie-Therapie, wenn dies aufgrund von Begleiterkrankungen (z. B. begleitendes akutes koronares Ereignis, akute Herzinsuffizienz, Aortendissektion, postthrombolytische sICH oder Präeklampsie/Eklampsie) zur Komplikationsverringerung erforderlich ist
- bei Patient*innen mit RR ≥ 220/120 mmHg, ohne i.v.-Lyse oder EVT und ohne Begleiterkrankungen, die eine dringende Blutdrucksenkung brauchen, ist der Nutzen einer Einleitung oder Wiederaufnahme der Hypertoniebehandlung innerhalb der ersten 48 – 72 h ungewiss
- bei Patient*innen mit RR < 220/120 mmHg, ohne i.v.-Lyse oder EVT und ohne Begleiterkrankungen, der eine dringende Blutdrucksenkung erfordert, ist die Einleitung oder Wiederaufnahme der Hypertoniebehandlung innerhalb der ersten 48 – 72 h nach AIS nicht wirksam, um Mortalität oder Morbidität zu verhindern
vor Reperfusionstherapie
- RR-Senkung auf RRsys < 185 mmHg und RRdia < 110 mmHg vor i.v.-Lyse bei AIS mit erhöhtem Blutdruck, der ansonsten für eine i.v.-Lyse in Frage kommt
- RR unter 185/110 mmHg halten bei Patient*innen mit geplanter EVT, die keine i.v.-Lyse erhalten haben
nach i.v.-Lyse
- RR mindestens 24 h nach i.v.-Lyse auf <180/105 mmHg halten
- bei leichtem bis mittelschwerem AIS mit i.v.-Lyse-Therapie starke RR-Senkung (Ziel-RRsys <140 mmHg im Vergleich zu <180 mmHg) nicht empfohlen
Temperaturmanagement
- bei AIS und Hyperthermie Normothermie anstreben (inkl. der Anwendung zur Protokollen zur Fieberbehandlung)
- bei AIS und Hyperthermie Ursachen der Hyperthermie, wie z. B. Infektionen, identifizieren und behandeln
- keine Empfehlung für induzierte Hypothermie oder prophylaktische Fieberprävention bei AIS und Normothermie
BZ-Management
- Hypoglykämie (BZ < 60 mg/dL) bei AIS behandeln
- anhaltende Hyperglykämie behandeln, um BZ im Bereich von 140 – 180 mg/dL zu halten (engmaschige Überwachung erforderlich)
- bei hospitalisierten AIS-Patient*innen mit Hyperglykämie wird Therapie mit Insulin i.v. zum Erreichen eines BZ im Bereich von 80 – 130 mg/dL nicht empfohlen
i.v.-Thrombolytika
Entscheidungsfindung bei Thrombolyse
- allgemeine Grundsätze
- schnelle i.v.-Thrombolyse bei Erwachsenen mit AIS und behindernden Defiziten (unabhängig vom NIHSS-Score), die für i.v.-Lyse in Frage kommen, verbessert das funktionelle Outcome
- bei Erwachsenen mit AIS, die innerhalb von 4,5 h nach Symptombeginn für i.v.-Lyse in Frage kommen, Lyse-Therapie so schnell wie möglich beginnen (sichere Gabe sicherstellen; Verzögerungen durch zusätzliche multimodale Neurobildgebung wie CT-Angio/Angio-MRT und Perfusions-CT/MRT vermeiden
- bei AIS mit i.v.-Lyse darauf vorbereitet sein, mögliche auftretende Nebenwirkungen zu behandeln (z.B. Blutungskomplikationen und Angioödem)
- bei AIS, die für i.v.-Lyse in Frage kommen die potenziellen Risiken und Vorteile mit Patient*innen und/oder Patient*innenvertreter*innen besprechen, sofern möglich, um gemeinsame Entscheidungsfindung sicherzustellen
- vor i.v.-Lyse-Therapie BZ-Spiegel bestimmen, um schwere Hypo- und Hyperglykämie als Stroke-Mimics auszuschließen oder rasch zu behandeln
- bei V.a. ischämischen Schlaganfall mit schwerer Hypo-/Hyperglykämie ist die i.v.-Lyse-Therapie empfohlen, wenn die Schlaganfallsymptome trotz BZ-Korrektur bestehen bleiben
- i.v.-Lyse bei AIS empfohlen, wenn bei der ersten Hirn-Bildgebung leichte bis mittelschwere ischämische Veränderungen (mit Ausnahme einer eindeutigen Hypodensität) festgestellt werden
- keine i.v.-Lyse empfohlen bei Erwachsenen mit AIS, die innerhalb von 4,5 h nach Symptombeginn oder dem letzten bekannten Normalzustand leichte, nicht behindernde Ausfallerscheinung aufweisen (keine Überlegenheit im Vergleich zur dualen Thrombozytenaggregationshemmung)
- Blutungsrisiko
- Empfehlung für i.v.-Lyse bei Patient*innen mit V.a. AIS, die Mono- oder Duale Thrombozytenaggregationshemmer einnehmen und für i.v.-Lyse in Frage kommen, trotz eines erhöhten ICB-Risikos im Vergleich zu keiner Thrombozytenaggregationshemmung
- bei Patient*innen mit V.a. AIS mit Symptombeginn < 4,5 h, die für i.v.-Lyse in Frage kommen, diese nicht verzögern, während auf hämatologische oder Gerinnungstests gewartet wird, wenn kein Grund zur Annahme eines abnormalen Laborergebnis besteht
- bei Patient*innen mit V.a. AIS mit Symptombeginn < 4,5 h, die für i.v.-Lyse in Frage kommen und bei denen das Ausmaß zerebraler Mikroblutungen unbekannt ist, wird die i.v.-Lyse ohne vorheriges MRT zum Ausschluss empfohlen
- bei Patient*innen mit V.a. AIS mit Symptombeginn < 4,5 h, die für i.v.-Lyse in Frage kommen, ist die i.v.-Lyse sinnvoll, wenn im MRT geringe zerebrale Mikroblutungen nachgewiesen wurden
- bei Patient*innen mit V.a. AIS mit Symptombeginn < 4,5 h, die für i.v.-Lyse in Frage kommen, ist der Nutzen einer i.v.-Lyse bei hoher Belastung durch zerebrale Mikroblutungen ungewiss
- pädiatrische Patient*innen
- bei pädiatrischen Patient*innen im Alter von 28 Tagen bis 18 Jahren mit bestätigter akuter ischämischer, zerebrovaskulärer Erkrankung, die innerhalb von 4,5 h nach Symptombeginn und mit neurologischen Defiziten vorstellig werden, i.v.-Thrombolyse mit Alteplase in Betracht ziehen (Applikation sicher; Wirksamkeit jedoch ungewiss)
Behandlung symptomatischer ICB, die innerhalb von 24 h nach Alteplase oder Tenecteplase i.v. zur Behandlung von AIS bei Erwachsenen auftreten
- Alteplase- oder Tenecteplase-Gabe abbrechen (falls noch laufend)
- Notfall-Blutbild, PT (INR), aPTT, Fibrinogenspiegel sowie Typisierung & Kreuzprobe
- notfallmäßiges Kopf-CT ohne Kontrastverstärkung, wenn klinische Bedenken bestehen
- Kryopräzipitat (inkl. Faktor VIII): 10 U über 10 – 30 min, um Fibrinogenspiegel von ≥ 150 mg/dL aufrechtzuerhalten; (Faustregel: 10 U Kryopräzipitat erhöhen den Fibrinogenspiegel um fast 50 mg/dL)
- 1000 mg Tranexamsäure i.v. über 10 min ODER 4 – 5 g E-Aminocapronsäure über 1 h, gefolgt von 1 g i.v., bis die Blutung unter Kontrolle ist (Spitzenwirkung nach 3 h)
- bei Bedarf Hämatologie- und Neurochirurgie-Konzil
- unterstützende Therapie ergreifen, inkl. RR-Management, ICP, CPP, MAP, Temperatur- & BZ-Kontrolle
Behandlung von orolingualem Angioödem im Zusammenhang mit Thrombolytika-Gabe i.v. bei akutem ischämischem Schlaganfall bei Erwachsenen
- ETI ggf. nicht erforderlich, wenn das Ödem auf die vordere Zunge und Lippen beschränkt ist
- ETI, wenn Ödem den Kehlkopf, Gaumen, Mundboden oder Oropharynx betrifft und schnell fortschreitet (innerhalb von 30 min)
- Intubation bei Vigilanz mittels Fiberoptik ist optimal (ggf. nasotracheale Intubation erforderlich, aber Epistaxis-Risiko nach Thrombolyse i.v.; Krikothyreotomie selten erforderlich und nach Thrombolyse i.v. ebenfalls problematisch)
- i.v.-Thrombolytika-Gabe abbrechen (bei Alteplase) und ACE-Hemmer aussetzen
- Gabe von 125 mg Methylprednisolon i.v.
- Gabe von 50 mg Diphenhydramin i.v.
- Gabe von 50 mg Ranitidin oder 20 mg Famotidin i.v.
- 0,3 mL 0,1 % Adrenalin (1 mg/mL) s.c. oder 0,5 mg/dL 0,1 % Adrenalin (1 mg/mL) vernebelt bei weiterem Fortschreiten des Angioödems
- Gabe von 3 mL Icatibant s.c. im Bauchbereich (30 mg) –> ggf. zusätzliche Injektion von 30 mg in Abständen von 6 h (max. 3 Injektionen in 24 h)
- Plasma-abgeleiteter C1-Esterase-Inhibitor (20 IE/kg) erfolgreich bei hereditärem Angioödem und ACE-Hemmer-bedingtem Angioödem eingesetzt
- unterstützende Therapie ergreifen
Auswahl des Thrombolytikums
- 0,25 mg/kgKG Tenecteplase (max. 25 mg) oder 0,9 mg/kgKG Alteplase bei Erwachsenen mit V.a. AIS, mit Symptombeginn oder letztem gesunden Zustand < 4,5 h, die für i.v.-Lyse in Frage kommen
- keine Empfehlung für Tenecteplase in Dosierung von 0,4 mg/kgKG bei Erwachsenen mit V.a. AIS, mit Symptombeginn oder letztem gesunden Zustand < 4,5 h, die für i.v.-Lyse in Frage kommen
Behandlung von AIS bei Erwachsenen – i.v.-Lyse
- Alteplase: 0,9 mg/kg (max. 90 mg) über 60 min, wobei 10 % der Dosis als Bolus über 1 min verabreicht werden
- Tenecteplase: 0,25 mg/kgKG (max. 25 mg)
| Gewicht (kg) | TNK (mg) | Zu verabreichendes Volumen (mL) |
|---|---|---|
| <60 kg | 15 | 3 |
| 60 – < 70 kg | 17,5 | 3,5 |
| 70 – < 80 kg | 20 | 4 |
| 80 – < 90 kg | 22,5 | 4,5 |
| ≥ 90 kg | 25 | 5 |
- nach i.v.-Lyse Überwachung auf ITS oder Stroke Unit
- Alteplase-Infusion abbrechen bei starke Kopfschmerzen, akuter Hypertonie, Übelkeit oder Erbrechen und Notfall-Kopf-CT durchführen
- RR-Messung und neurologische Untersuchungen alle 15 min während und nach der i.v.-Lyse für 2 h, dann alle 30 min für 6 h und anschließend stündlich bis 24 h nach Lyse-Gabe
- RR-Mess-Intervall erhöhen, wenn RRsys > 180 mmHg oder RRdia > 105 mmHg, um den Blutdruck auf oder unter diesen Werten zu halten
- Platzierung von Magensonden, Blasenkathetern oder intraarteriellen Druckkathetern verzögern, wenn Patient*innen ohne sicher behandelt werden können
- Folge-CT oder -MRT 24 h nach Lyse-Gabe vor dem Beginn der Antikoagulanzien- oder Thrombozytenaggregationshemmern-Gabe
verlängertes Zeitfenster für die i.v.-Thrombolyse
- bei Patient*innen mit AIS mit unklarem Zeitpunkt des Beginns und sich im Zeitfenster < 4,5 h nach Erkennung befinden UND eine MRI-DWI-Läsion aufweisen, die kleiner als 1/3 des MCA-Gebiets ist, und keine deutliche Signaländerung auf FLAIR, kann die i.v.-Lyse innerhalb von 4,5 Stunden nach Erkennung der Schlaganfallsymptome verabreicht werden
- bei Patient*innen mit AIS, bei denen in der automatisierten Perfusionsbildgebung eine rettbare ischämische Penumbra festgestellt wurde und die einen Wake-Up-Stroke haben (Erwachen mit Symptomen innerhalb von 9 h nach dem mittleren Zeitpunktes des Schlafes) ODER sich im Zeitfenster zw. 4,5 – 9 h nach dem letzten beobachteten gesunden Zustand befinden, kann die i.v.-Lyse sinnvoll sein
- bei AIS aufgrund LVO mit rettbarer ischämischer Penumbra im Zeitfenster zw. 4,5 – 24 h nach Symptombeginn oder nach dem letzten beobachteten gesunden Zustand UND die keine EVT erhalten, kann die i.v.-Lyse unter Anleitung von Fachpersonen in der thrombolytischen Schlaganfallversorgung von Vorteil sein
andere i.v.-Fibrinolytika und Sonothrombolyse
- andere i.v.-Fibrinolytika
- bei AIS im Zeitfenster von 4,5 h nach dem letzten beobachteten gesunden Zustand, die keine EVT erhalten, kann anstelle der Alteplase-Gabe die Reteplase-Gabe erwogen werden (erhöhte Wahrscheinlichkeit eines besseren funktionellen Outcomes nach 90 Tagen)
- bei geeigneten Patient*innen mit AIS im Zeitfenster von 4,5 h nach dem letzten beobachteten gesunden Zustand, die keine EVT erhalten, kann die Gabe von mutiertem Prourokinase i.v. anstelle von Alteplase in Betracht gezogen werden
- bei geeigneten Patient*innen mit AIS im Zeitfenster von 3 – 9 h nach dem letzten beobachteten gesunden Zustand, keine Gabe von Desmoteplase i.v.
- bei geeigneten Patient*innen mit AIS im Zeitfenster von 4,5 h nach dem letzten beobachteten gesunden Zustand, keine Gabe von mutiertem Prourokinase in Verbindung mit niedrig dosiertem Alteplase i.v.
- bei geeigneten Patient*innen mit AIS im Zeitfenster von 6 h nach dem letzten beobachteten gesunden Zustand, keine Gabe von Urokinase i.v.
- bei geeigneten Patient*innen mit AIS im Zeitfenster von 6 h nach dem letzten beobachteten gesunden Zustand, keine Gabe von Streptokinase i.v. (keine Verbesseurng des funktionellen Outcomes nach 90 d, aber erhöhte Frühmortalität)
- Sonothrombolyse
- keine Empfehlung für Sonothrombolyse als Zusatztherapie zur i.v.-Lyse im Vergleich zur Mono-i.v.-Lyse
sonstige besondere Umstände
- bei geeigneten Erwachsenenn mit AIS und bekannter Sichelzellenkrankheit kann die i.v.-Lyse von Vorteil sein (verbessertes funktionelles Outcome, ohne Zunahme von ICB, lebensbedrohlichen systemischen Blutungen oder anderen thrombolytischen Komplikationen
- bei Erwachsenen mit akuter nicht-arterieller Zentralarterienverschlusserkrankung, die zu Sehbeeinträchtigung führt, aber ansonsten für die i.v.-Lyse in Frage kommt, ist die i.v.-Lyse innerhalb von 4,5 h nach dem letzten beobachteten gesunden Zustand ungewiss
endovaskuläre Thrombektomie (EVT)
EVT begleitend zur i.v.-Lyse
- bei AIS, der sowohl für i.v.-Lyse und EVT in Frage kommt, ist die i.v.-Lys sicher und wird um die allgemeine Reperfusionswirksamkeit und das klinische Outcome zu verbessern empfohlen
- bei AIS, der sowohl für i.v.-Lyse und EVT in Frage kommt, sollte die i.v.-Lyse so schnell wie möglich und ohne Beobachtung zur Beurteilung des klinischen Ansprechens oder zur Verzögerung des Beginns der EVT verabreicht werden
EVT bei Erwachsenen
- Thrombektomie innerhalb von 0 – 6 h nach Symptombeginn (ASPECTS 3 – 10)
- EVT bei AIS aufgrund proximaler LVO der ICA oder M1 im vorderen Kreislauf empfohlen bei Vorstellung innerhalb von 6 h nach Symptombeginn, NIHSS-Score ≥ 6, mRS-Score vor Schlaganfall von 0 – 1 und ASPECTS-Score von 3 – 10
- Thrombektomie innerhalb von 6 – 24 h nach Symptombeginn (ASPECTS 6 – 10)
- EVT bei AIS aufgrund proximaler LVO der ICA oder M1 im vorderen Kreislauf empfohlen bei Vorstellung innerhalb von 6 – 24 h nach Symptombeginn, NIHSS-Score ≥ 6, mRS-Score vor Schlaganfall von 0 – 1 und ASPECTS-Score ≥ 6
- Thrombektomie innerhalb von 6 – 24 h nach Symptombeginn (ASPECTS 3 – 5)
- EVT bei AIS aufgrund proximaler LVO der ICA oder M1 im vorderen Kreislauf empfohlen bei Vorstellung innerhalb von 6 – 24 h nach Symptombeginn, Alter < 80 Jahre, NIHSS-Score ≥ 6, mRS-Score vor Schlaganfall von 0 – 1, ASPECTS-Score 3 – 5 ohne signifikante Massenwirkung in der Bildgebung
- Thrombektomie innerhalb von 0 – 6 h nach Symptombeginn (ASPECTS 0 – 2)
- EVT bei AIS aufgrund proximaler LVO der ICA oder M1 im vorderen Kreislauf sinnvoll bei Vorstellung innerhalb von 6 h nach Symptombeginn, Alter < 80 Jahre, NIHSS-Score ≥ 6, mRS-Score vor Schlaganfall von 0 – 1, ASPECTS-Score 0 – 2 ohne signifikante Massenwirkung in der Bildgebung
- Thrombektomie innerhalb von 0 – 6 h nach Symptombeginn bei leichter vorbestehender Behinderung
- EVT bei AIS aufgrund proximaler LVO der ICA oder M1 im vorderen Kreislauf sinnvoll bei Vorstellung innerhalb von 6 h nach Symptombeginn, NIHSS-Score ≥ 6, mRS-Score vor Schlaganfall von 2 und ASPECTS-Score 0 – 2 (auch zur Verringerung akkumulierter Behinderungen)
- Thrombektomie innerhalb von 0 – 6 h nach Symptombeginn bei mäßiger vorbestehender Behinderung
- EVT bei AIS aufgrund proximaler LVO der ICA oder M1 im vorderen Kreislauf sinnvoll bei Vorstellung innerhalb von 6 h nach Symptombeginn, NIHSS-Score ≥ 6, mRS-Score vor Schlaganfall von 3 – 4 und ASPECTS-Score ≥ 6
- Thrombektomie innerhalb von 0 – 6 h bei Verschlüssen des dominanten proximalen M2-Astes der Arteria cerebri media (MCA)
- EVT bei AIS aufgrund eines Verschlusses des dominanten proximalen M2-Astes der MCA sinnvoll bei Vorstellung innerhalb von 6 h nach Symptombeginn, NIHSS-Score ≥ 6, mRS-Score vor Schlaganfall von 0 – 1 und ASPECTS-Score ≥ 6 (Nutzen jedoch ungewiss)
- Thrombektomie innerhalb von 0 – 6 h bei Verschlüssen des nicht-dominanten proximalen M2-Astes der MCA, der distalen MCA, der Arteria cerebri anterior (ACA) und der Arteria cerebri posterior (PCA)
- keine Empfehlung für EVT bei AIS aufgrund eines Verschlusses des proximalen nicht-dominanten oder kodominanten proximalen M2-Segments der MCA oder der distalen MCA, der ACA oder der PCA wird eine EVT
Schlaganfall im Bereich der hinteren Zirkulation
- EVT innerhalb von 24 h nach Symptombeginn bei AIS und Basilarisarterienverschluss mit mRS-Score vor Schlaganfall von 0 – 1 , NIHSS-Wert ≥ 10 bei Aufnahme und PC-ASPECTS-Wert ≥ 6 (leichte ischämische Schädigung) empfohlen
- EVT-Wirksamkeit innerhalb von 24 h zur Verbesserung des funktionellen Outcomes und zur Senkung der Mortalität bei AIS und Basilarisarterienverschluss, mRS-Score vor Schlaganfall von 0 – 1, NIHSS-Wert von 6 – 9 bei Aufnahme und PC-ASPECTS-Wert ≥ 6 (leichte ischämische Schädigung) nicht ausreichend belegt
EVT bei pädiatrischen Patient*innen
- bei Kindern> 6 Jahre mit akuten neurologischen Symptomen und ischämischem Schlaganfall aufgrund LVO kann die EVT innerhalb von 6 h nach Symptombeginn durch erfahrene Neurointerventionist*innen das funktionelle Outcome verbessern
- bei Kindern> 6 Jahre mit akuten neurologischen Symptomen und ischämischem Schlaganfall aufgrund LVO kann die EVT innerhalb von 6 -24 h nach Symptombeginn mit potenziell rettbarem Hirngewebe das funktionelle Outcome verbessern
- bei Kindern zw. 28 Tagen und 6 Jahren mit akuten neurologischen Symptomen (inkl. erstmaliger Krampfanfall) und ischämischem Schlaganfall aufgrund LVO kann die EVT durch erfahrene Neurointerventionist*innen innerhalb von 24 h nach Symptombeginn mit potenziell rettbarem Hirngewebe das funktionelle Outcome verbessern
Thrombozytenaggregationshemmung
allgemeine Grundsätze für frühzeitige Thrombozytenaggregationshemmung
- Empfehlung für Aspirin-Gabe innerhalb von 48 Stunden nach Schlaganfallbeginn bei AIS
- Risiko einer Thrombozytenaggregationshemmung in den ersten 24 h nach i.v.-Lyse (mit oder ohne EVT) ungewiss –> Gabe erwägen, wenn Begleiterkrankungen vorliegen, bei denen eine solche Behandlung ohne i.v.-Lyse bekanntermaßen einen erheblichen Nutzen hat, oder wenn bekannt ist, dass das Unterlassen einer solchen Behandlung ein erhebliches Risiko mit sich bringt
- Wirksamkeit von Tirofiban i.v. zur Verbesserung der klinischen Outcoms nicht eindeutig nachgewiesen
- keine Gabe von Abciximab i.v. (CAVE: erhöhte Blutungskomplikationen)
frühzeitige Sekundärprävention
- Thrombozytenaggregationshemmung der oralen Antikoagulation bei nicht-kardioembolischem AIS oder TIA vorziehen
- bei nicht-kardioembolischem AIS oder TIA Auswahl eines Thrombozytenaggregationshemmers individuell auf Grundlage des Risikoprofils der Patient*innen, der Kosten, der Verträglichkeit, der relativen bekannten Wirksamkeit der Wirkstoffe und anderer klinischer Merkmale
- mind. 3-monatige Behandlung mit Thrombozytenaggregationshemmern oder Antikoagulanzien bei AIS und extrakranieller Karotis- oder vertebraler Arteriendissektion
- bei Patient*innen, die zum Zeitpunkt eines nicht-kardioembolischen ischämischen Schlaganfalls oder einer TIA bereits Aspirin einnehmen, ist die Wirksamkeit einer Dosiserhöhung oder ein Wechsels zu einem anderen Thrombozytenaggregationshemmer nicht eindeutig belegt
- keine Empfehlung für Ticagrelor ggü. Aspirin bei leichtem nicht kardioembolischem AIS (NIHSS-Score ≤ 3) oder hochriskantem TIA (ABCD2-Score ≥ 4) zur Verringerung des kombinierten Endpunkts aus Schlaganfall, Myokardinfarkt oder Tod
- keine dreifache Thrombozytenaggregationshemmung (Aspirin, Clopidogrel und Dipyridamol) bei Patienten mit nicht-kardioembolischem ischämischem Schlaganfall (CAVE: erhöhtes Blutungsrisiko)
- keine routinemäßige Zusatzgabe einer Thrombozytenaggregationshemmung zur oralen Antikoagulation bei Patient*innen mit ischämischem Schlaganfall und VHF ohne aktive KHK oder kürzlich implantiertem intravaskulären Stent (CAVE: potenziell schädlich aufgrund erhöhten Blutungsrisikos)
duale Thrombozytenaggregationshemmung bei leichter ischämischer Hirninfarkt und TIA mit hohem Risiko
- frühzeitige (innerhalb von 24 h nach Symptombeginn) DAPT, bestehend aus Aspirin & Clopidogrel mit Initialdosis Clopidogrel, über 21 Tage bei Patient*innen mit leichtem nicht-kardioembolischem ischämischem Hirninfarkt (NIHSS-Score ≤ 3) oder TIA mit hohem Risiko (ABCD2-Score ≥ 4), die keine i.v.-Thrombolyse erhalten haben –> gefolgt von Einzeltherapie mit Thrombozytenaggregationshemmern
- DAPT mit Ticagrelor (inkl. Initialdosis) plus Aspirin über 30 Tage erwägen bei Patient*innen mit kürzlich (< 24 h) aufgetretenem leichtem nicht-kardioembolischem AIS (NIHSS-Score ≤ 5) oder hochriskanter TIA (ABCD2-Score ≥ 6 oder symptomatischer intrakranieller oder extrakranieller ≥ 50 %-iger Stenose einer Arterie, die für die TIA verantwortlich sein könnte), die keine i.v.-Lyse erhalten haben
- DAPT (Clopidogrel & Aspirin) über 21 Tage sinnvoll bei Patient*innen mit vermuteter atherosklerotischer Ursache (≥ 50 % Stenose der intrakraniellen oder extrakraniellen Stenose, die wahrscheinlich für das klinische Erscheinungsbild verantwortlich war, oder akute neue Infarkte im Bildgebungsverfahren bei vermuteter atherosklerotischer Ursache in großen Arterien) mit leichtem nicht-kardioembolischem AIS (NIHSS-Score ≤ 5) oder hochriskanter TIA (ABCD2-Score ≥ 4) innerhalb von 24 – 72 h nach Schlaganfallbeginn oder NIHSS-Score von 4 – 5 innerhalb von 24 Stunden nach Schlaganfallbeginn, die keine IVT erhielten
- 21-tägige DAPT mit Ticagrelor und Aspirin (gefolgt von Monotherapie mit Ticagrelor) sinnvoll ggü. DAPT mit Clopidogrel und Aspirin bei Patient*innen mit leichtem nicht-kardioembolischem AIS (NIHSS-Score ≤ 3) oder hochriskanter TIA (ABCD2-Score ≥ 4) innerhalb von 24 h nach Symptombeginn, die keine i.v.-Lyse erhalten haben und das CYP2C19-Funktionsverlust-Allel tragen
Thrombozytenaggregationshemmung im Rahmen einer i.v.-Lyse
- Aspirin nicht als Ersatz für akute Schlaganfall-Therapie empfohlen bei Patient*innen mit AIS, die ansonsten für i.v.-Lyse oder EVT in Frage kommen
- Aspirin nicht gleichzeitig oder innerhalb von 90 min nach Beginn der i.v.-Lyse verabreichen (CAVE: Blutungsrisiko)
- Zusatzbehandlung mit Eptifibatid i.v. bei Patient*innen mit AIS, die innerhalb von 3 h nach Symptombeginn eine i.v.-Lyse erhalten, nicht empfohlen
Antikoagulanzien
- bei sorgfältig ausgewählten (z.B. leichteren) Patient*innen mit AIS und VHF ist eine Strategie der frühzeitigen oralen Antikoagulation nach Schlaganfall mit geringem Risiko verbunden und im Vergleich zu einer Strategie der verzögerten Antikoagulation sinnvoll
- Nutzen einer raschen Antikoagulation bei Patient*innen mit AIS und ipsilateraler, hochgradiger ICA-Stenose nicht eindeutig nachgewiesen
- Sicherheit und Wirksamkeit einer kurzfristigen Antikoagulation bei Patient*innen mit AIS und ipsilateralem, nicht-okklusivem, extrakraniellen intraluminalen Thrombus nicht eindeutig belegt
- je nach spezifischem klinischem Szenario und zugrunde liegender Indikation die Einleitung oder Fortsetzung einer Antikoagulation bei Patienten mit AIS, die an hämorrhagischer Transformation/Konversion leiden, in Betracht ziehen
- Argatroban als Zusatztherapie zur i.v.-Lyse bei Patient*innen mit AIS nicht wirksam
- frühzeitige Antikoagulation (innerhalb von 48 h nach Schlaganfallbeginn) verringert nicht die Wahrscheinlichkeit einer frühzeitigen neurologischen Verschlechterung oder erhöht die Wahrscheinlichkeit eines günstigen funktionellen Outcomes, daher keine Empfehlung
Volumenexpansion/Hämodilution, Vasodilatatoren und hämodynamische Therapie
- hämodynamische Augmentation mittels Hämodilution, hochdosiertem Albumin oder chemischen Vasodilatatoren wie Pentoxifyllin zur Verbesserung der funktionellen klinischen Outcomes nicht empfohlen
- mechanische hämodynamische Augmentation mit Gegenpulsationsgeräten oder Stimulation des Ganglion sphenopalatinum zur Verbesserung der funktionellen klinischen Outcomes nicht empfohlen
neuroprotektive Substanzen
- derzeit keine Empfehlung für die Anwendung pharmakologischer oder nicht-pharmakologischer neuroprotektiver Therapien
notfallmäßige Karotisendarteriektomie, Karotisangioplastie und Stentimplantation ohne intrakranielles Thrombus
- bei Patienten mit AIS oder instabilem neurologischem Status (z. B. Schlaganfall in Entwicklung), verursacht durch hochgradige Karotisstenose oder -okklusion ohne intrakranielle Okklusion, ist eine Notfall-Karotisendarteriektomie (innerhalb von 48 h) nicht von Vorteil
innerklinisches AIS-Management – allgemeine supportive Therapie
Stroke Units
- Behandlung auf Strok Unit für AIS-Patient*innen aller Altersgruppen
Dysphagie
- vor Aufnahme von Flüssigkeiten oder Nahrung Schluck-Screening am Krankenbett
- Durchführung des Dysphagie-Screening durch Logopäd*innen oder andere geschulte medizinische Fachkräfte
- endoskopische Untersuchung der Schluckfunktion sinnvoll bei Patient*innen mit AIS, die aufgrund neurologischer Beeinträchtigungen nicht an Schlucktests am Krankenbett teilnehmen können
- Mundhygieneprotokoll sinnvoll, um das Pneumonie-Risiko zu verringern
- pharyngeale Elektrostimulation (PES) kann bei Patient*innen mit Schlaganfall und Dysphagie vorteilhaft sein, um Dysphagie-Schweregrad zu verringern und das Aspirationsrisiko zu senken
- Behandlung mit PES nach Beatmungs-Weaning bei Patient*innen mit schwerem Schlaganfall und Dysphagie vorteilhaft, die eine Tracheotomie und mechanische Beatmung erforderte
Nutrition
- Beginn der enteralen Ernährung innerhalb von 7 d nach Aufnahme
- Ernährungsscreening empfohlen, um Ernährungsbehandlung frühzeitig nach Aufnahme, vorzugsweise innerhalb von 48 h nach Aufnahme, zu beginnen
- Anlage einer perkutanen Gastrostomie-Sonde bei Patient*innen, bei denen in den ersten 7 Tagen zunächst eine nasogastrale Sonde zur Ernährung verwendet wurde und bei denen eine länger anhaltende Unfähigkeit zum sicheren Schlucken zu erwarten ist (> 2 – 3 Wochen)
Prophylaxe tiefer Venenthrombosen
- intermittierende pneumatische Kompression (IPC) zusätzlich zur Routineprophylaxe bei mobilitätseingeschränkten Patient*innen empfohlen
- prophylaktisches Heparin s.c. (UFH oder LMWH) bei mobilitätseingeschränkten Patient*innen sinnvoll
- Nutzen einer prophylaktischen Heparin-Gabe s.c. (UFH oder LMWH) ggü. keiner prophylaktischen Heparin-Gabe hinsichtlich einer Erhöhung der Gesamtüberlebensrate nicht eindeutig belegt
- Nutzen einer prophylaktischen LMWH-Gabe ggü. UFH-Gabe ungewiss
- elastische Kompressionsstrümpfe verursachen im Vergleich zur üblichen Therapie Schäden wie Hautschäden, Ulzerationen und Gewebenekrosen
Depression
- strukturiertes, routinemäßiges Depression-Screening empfohlen, um Post-Schlaganfall-Depression zu detektieren (optimaler Zeitpunkt für Screening ungewiss)
- Behandlung mit Antidepressiva und/oder nicht-pharmakologischen Interventionen (d. h. Psychotherapie, nicht-invasive Hirnstimulation, Akupunktur) bei Patienten, bei denen eine PSD diagnostiziert wurde, empfohlen
weitere Überlegungen zum KH-Management
- Überweisung an palliativmedizinische Einrichtungen für ausgewählte AIS-Patient*innen und ihre Familien sinnvol
- routinemäßige, prophylaktische Antibiotika-Gabe nicht vorteilhaft für die Verbesserung der funktionellen Outcomes
- keine routinemäßige Anlage eines Blasenkatheters aufgrund des damit verbundenen Risikos von Katheter-assoziierten Harnwegsinfektionen
Rehabilitation
- formelle, interdisziplinäre Beurteilung und eine auf die einzelnen Patient*innen abgestimmte Rehabilitation empfohlen
- SSRI zur Verbesserung der motorischen Erholung oder des Funktionsstatus nicht wirksam
- hochfrequente, sehr frühzeitige Mobilisierung innerhalb von 24 h nach Schlaganfallbeginn nicht empfohlen (CAVE: kann sogar schädlich sein)
innerklinisches AIS-Management – Therapie von Komplikationen
Hirnschwellung/-ödem
allgemeine Empfehlungen
- frühzeitig Besprechung der Behandlungsoptionen und möglichen Ergebnisse mit den Patient*innen (sofern möglich) und den Angehörigen bei Patient*innen mit großen Hirn- oder Kleinhirninfarkten, bei denen ein hohes Risiko für Hirnschwellungen und Hernien besteht
- engmaschiges Monitoring Anzeichen einer neurologischen Verschlechterung in den ersten Tagen nach Schlaganfall bei Patient*innen mit großen Hirn- oder Kleinhirninfarkten, um die Notwendigkeit potenzieller Interventionen schnell beurteilen zu können
- frühzeitige Verlegung in Klinik mit entsprechender neurochirurgischer und intensivmedizinischer Expertise bei Patient*innen mit großen Hirn- oder Kleinhirninfarkten
medizinische Therapie
- Einsatz einer osmotischen Therapie als Überbrückung bis zu einem chirurgischen Eingriff bei Patient*innen mit großen Hirn- oder Kleinhirninfarkten und neurologischem Rückgang sinnvoll
- Glibenclamid i.v. bei Patient*innen mit großflächigen Hemisphäreninfarkten im Alter von 18 – 70 Jahren nicht empfohlen
- kein Einsatz von Hypothermie, Barbituraten oder Kortikosteroiden zur Therapie einer Hirnschwellung bei Patient*innen mit großflächigen Hirn- oder Kleinhirninfarkten und Hirnschwellungen
supratentorieller Infarkt (chirurgische Behandlung)
- Bewusstseinsminderung aufgrund Hirnschwellung ist ein vernünftiger Grund für die Entscheidung für eine dekompressive Hemikraniektomie bei Patient*innen mit großflächigen Hirninfarkten, bei denen ein hohes Risiko für Hirnschwellungen und Hernien besteht
- dekompressive Kraniektomie mit Duralerweiterung vorteilhaft bei Patient*innen ≤ 60 Jahren mit einseitigen MCA-Infarkten, deren neurologischer Zustand sich trotz medikamentöser Therapie innerhalb von 48 h aufgrund Hirnschwellung verschlechtert
- dekompressive Kraniektomie mit Duralerweiterung in Betracht ziehen bei Patient*innen > 60 Jahren mit einseitigen MCA-Infarkten, deren neurologischer Zustand sich trotz medikamentöser Therapie innerhalb von 48 h aufgrund Hirnschwellung verschlechtert
- frühzeitige dekompressive Kraniektomie innerhalb von 48 Stunden ohne zusätzliche Sicherheitsbedenken in Betracht ziehen bei AIS-Patient*innen, die eine i.v.-tPA-Thrombolyse erhalten haben und trotz medikamentöser Therapie ein malignes Hirnödem entwickeln
Kleinhirninfarkt (chirurgische Behandlung)
- Ventrikulostomie bei Kleinhirninfarkt und obstruktivem Hydrozephalus empfohlen –> begleitende/anschließende dekompressive Kraniektomie ggf. je nach Faktoren wie Größe des Infarkts, neurologischem Zustand, Grad der Hirnstammkompression und Wirksamkeit der medizinischen Behandlung erforderlich
- dekompressive subokzipitale Kraniektomie mit Duralerweiterung bei Kleinhirninfarkt, der zu einer neurologischen Verschlechterung aufgrund einer Kompression des Hirnstamms führt oder ein Volumen ≥ 35 mL hat
Krampfanfälle
- Antiepileptika-Gabe bei Erwachsenen mit unprovozierten Anfällen nach AIS auf Grundlage spezifischer Patient*innenmerkmale empfohlen, um Rezidivrisiko zu verringern
- prophylaktische Antiepileptika-Gabe bei Erwachsenen nicht empfohlen


Sei der Erste der einen Kommentar abgibt