veröffentlichende Fachgesellschaft: American Heart Association (AHA), American College of Cardiology (ACC), American College of Clinical Pharmacy (ACCP), American College of Emergency Physicians (ACEP), American College of Chest Physicians (CHEST), Society for Cardiovascular Angiography & Interventions (SCAI), Society of Hospital Medicine (SHM), Society of Interventional Radiology (SIR), Society for Vascular Medicine (SVM) & Society of Vascular Nursing (SVN)
Klassifikation gemäß AWMF:
Datum der Veröffentlichung: 19.02.2026
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.1161/CIR.0000000000001415
Ersteinschätzung und Diagnose
klinische Beurteilung
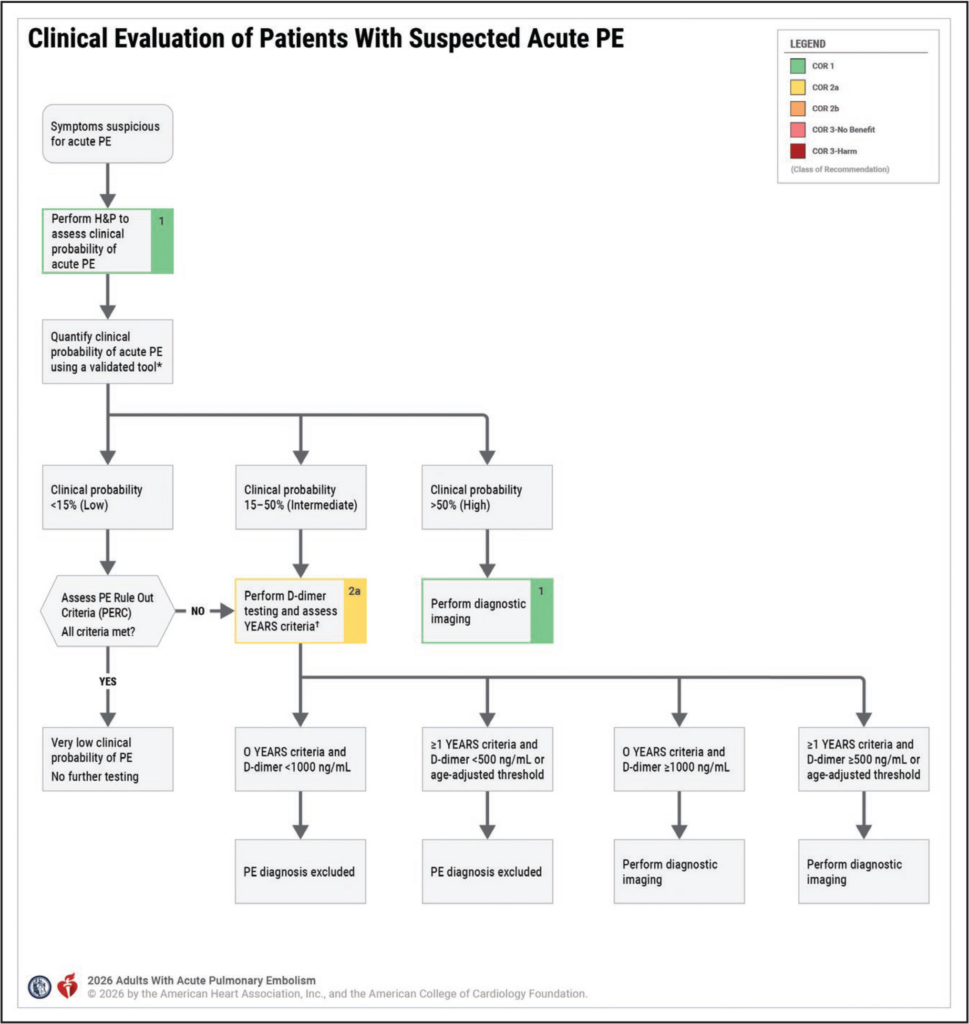
- gezielte Anamnese und umfassende körperliche Untersuchung bei V.a. akute Lungenarterienembolie (LAE), um die klinische Vortestwahrscheinlichkeit einer akuten Lungenembolie zu bestimmen
- altersbereinigter D-Dimer-Wert unterhalb des Schwellenwerts (Alter × 10 μg/L für FEU-Assays) schließt Lungenembolie und Notwendigkeit einer Bildgebung bei Erwachsenen mit V.a. LAE und klinisch geringer oder mittlerer LAE-Wahrscheinlichkeit (< 50 %) nach Risikobewertung wirksam aus
- YEARS-Algorithmus bei Erwachsenen mit V.a. LAE hilfreich, um die Indikation für eine Bildgebung zu stellen
- D-Dimer-Schwellenwert von 1000 μg/L bei Patient*innen, die keine YEARS-Kriterien erfüllen
YEARS-Algorithmus
D-Dimer > 500 μg/L bei Patient*innen, die ≥ 1 der folgenden Symptome aufweisen:
1) klinische TVT-Zeichen und/oder
2) Hämoptyse und/oder
3) Lungenembolie als wahrscheinlichste Diagnose
- bei Schwangeren kann es sinnvoll sein schwangerschaftsangepasste YEARS-Kriterien für die Indikationsstellung einer Bildgebung zu nutzen
- Clinical Decision Rules
Wells-Score
– klinische Zeichen für eine TVT (3 Punkte)
– andere Diagnosen sind unwahrscheinlich (3 Punkte)
– HF > 100/min (1,5 Punkte)
– Immobilisation > 3 d oder OP vor < 4 Wochen (1,5 Punkte)
– frühere LAE oder TVT (1,5 Punkte)
– Hämoptyse (1 Punkt)
– Krebs/Neoplasie (1 Punkt)
Auswertung
< 2 Punkte: geringe Wahrscheinlichkeit
2 – 6 Punkte: mittlere Wahrscheinlichkeit
≥ 7 Punkte: hohe Wahrscheinlichkeit
PERC-Regel
– Alter ≥ 50 Jahre
– HF ≥ 100/min
– SpO2 < 95 %
– keine Hämoptyse
– keine Hormonsubstitution (z.B. Östrogen)
– keine frühere LAE oder TVT
– keine einseitige Beinschwellung
– kein Trauma oder OP vor < 4 Wochen
Auswertung
alle Kriterien erfüllt = geringe LAE-Wahrscheinlichkeit –> keine weiteren Untersuchungen erforderlich
Simplified Revised Geneva Score
– Alter ≥ 65 Jahre (1 Punkt)
– keine frühere LAE oder TVT (1 Punkt)
– OP unter Vollnarkose oder Fraktur der unteren Extremitäten < 1 Monat (1 Punkt)
– aktive Krebserkrankung/Neoplasie (1 Punkt)
– keine einseitige Beinschwellung (1 Punkt)
– keine Hämoptyse (1 Punkt)
– HF 75 – 94/min (1 Punkt)
– HF > 95/min (1 Punkt)
– schmerzhafte Palpation der tiefen Beinvenen und einseitiges Beinödem (1 Punkt)
Auswertung
0 – 1 Punkt: geringe Wahrscheinlichkeit
2 – 5 Punkte: mittlere Wahrscheinlichkeit
5 – 7 Punkte: hohe Wahrscheinlichkeit
0 – 2 Punkte: LAE unwahrscheinlich
3 – 7 Punkte: LAE wahrscheinlich
Revised Geneva Score
– Alter ≥ 65 Jahre (1 Punkt)
– keine frühere LAE oder TVT (3 Punkte)
– OP unter Vollnarkose oder Fraktur der unteren Extremitäten < 1 Monat (2 Punkte)
– aktive Krebserkrankung/Neoplasie (2 Punkte)
– keine einseitige Beinschwellung (3 Punkte)
– keine Hämoptyse (2 Punkte)
– HF 75 – 94/min (3 Punkte)
– HF > 95/min (5 Punkte)
– schmerzhafte Palpation der tiefen Beinvenen und einseitiges Beinödem (4 Punkte)
Auswertung
0 – 3 Punkte: geringe Wahrscheinlichkeit
4 – 10 Punkte: mittlere Wahrscheinlichkeit
≥ 11 Punkte: hohe Wahrscheinlichkeit
diagnostische Tests
- Bildgebung zur Bestätigung/zum Ausschluss empfohlen bei Patient*innen mit V.a. LAE, die anhand eines validierten klinischen Risikoprädiktionsscores oder eines erhöhten D-Dimer-Spiegels als hochwahrscheinlich klassifiziert werden (> 50 % LAE-Wahrscheinlichkeit)
- CT-Pulmonalisangiographie (CTPA) oder Ventilations-/Perfusions-Scan (V/Q-Scan) ausreichend, um LAE zu diagnostizieren
- CTPA ggü. V/Q-Scan bevorzugen
- bei Schwangeren mit positiven YEARS-Kriterien und normalem Thorax-Röntgen CTPA mit niedriger Strahlendosis ggü. Perfusionsszintigraphie mit niedriger Dosis sinnvoller
- V/Q-Einzelphotonen-Emissionscomputertomographie (SPECT) als diagnostische Untersuchung einem planaren V/Q-Scan vorziehen
- bei Patient*innen mit V.a. auf akute LAE, die sich keiner CTPA unterziehen können, V/Q-Scan ggü. einer kontrastverstärkten Magnetresonanzangiographie (MRA) vorziehen
- bei bestätigter akuter LAE kann Duplex-Sonographie der unteren Extremitäten sinnvoll sein, wenn klinische Befunde auf TVT hindeuten oder wenn das Vorliegen einer TVT die Behandlung verändert oder die Prognose beeinflusst
- venöse Duplexsonographie für weitere diagnostische Abklärung bei V.a. LAE sowie negativem CTPA-Befund oder normalem V/Q-SPECT-Befund nicht sinnvoll
- EKG zur Bestätigung oder Widerlegung der Diagnose einer LAE nicht empfohlen
- bei V.a. akute LAE CT-Venographie der unteren Hohlvene und der Venen der unteren Extremitäten nicht als routinemäßige Ergänzung zur CTPA zur Diagnose einer Venenthrombose empfohlen
Berichterstattung über Befunde der diagnostischen Bildgebung
- bei akuter LAE wird für die Risikostratifizierung die Angabe des numerischen Verhältnisses zw. rechter (RV) und linker Herzkammer (LV) ggü. einer subjektiven Quantifizierung empfohlen
- bei akuter LAE und TTE RV-Dysfunktion anhand der folgenden Parameter beurteilen: RV/LV-Enddiastolisches Verhältnis; RV-Enddiastolischer Durchmesser; Trikuspidalklappen-Anulus-Ekskursion (TAPSE); geschätzter systolischer RV-Druck; RV-Freuwandhypokinesie mit Schonung der Spitze (McConnell-Zeichen); Trikuspidalklappen-Systolengeschwindigkeit; paradoxe Septumbewegung; und IVC-Respirophasenkollaps zur Unterstützung der Risikostratifizierung
- Meldung chronischer Merkmale (z.B. intravaskuläre Verwachsungen, RV-Hypertrophie, Bronchialarteriendilatation, Pulmonalarterienretraktion oder -dilatation und intraventrikuläre Septumabflachung) im CTPA ggf. hilfreich für die Identifizierung von Patient*innen, bei denen das Risiko für chronische klinische Folgeerscheinungen einer Lungenembolie besteht
Risikobewertung anhand klinischer Risikoscores
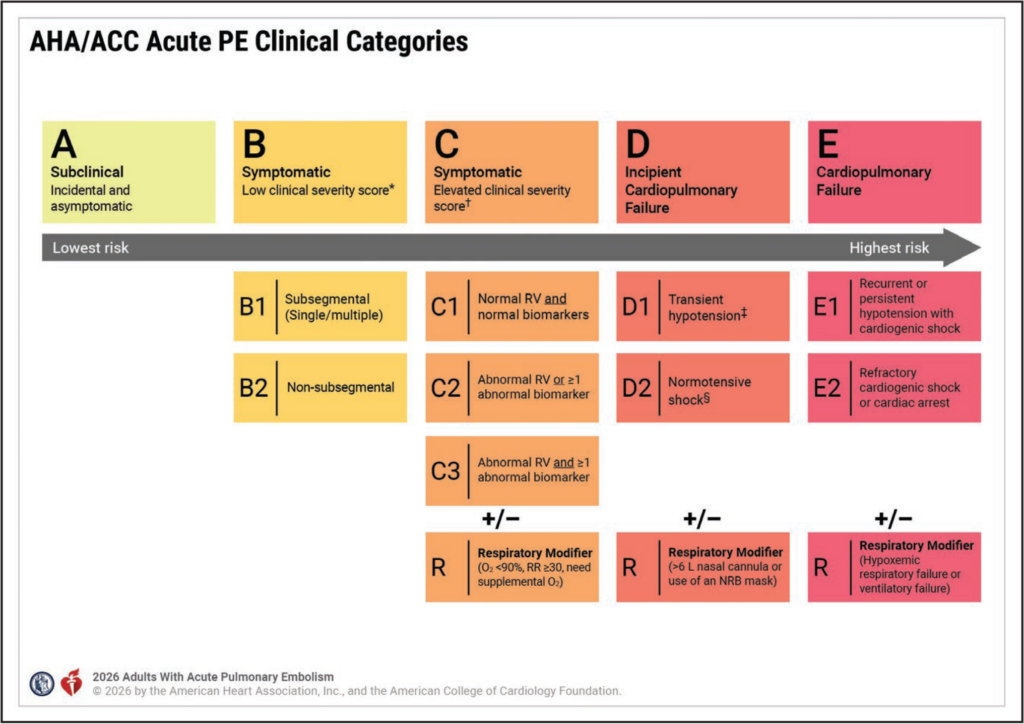
- Empfehlung für die Verwendung von Hestia-Kriterien, PESI und/oder sPESI bei Patient*innen mit akuter LAE der Kategorie A & B, um Patient*innen mit geringem Risiko für kurzfristige unerwünschte Ereignisse zu identifizieren
- Verwendung eines validierten LAE-spezifischen Risikoscores bei hämodynamisch stabilen Patient*innen mit akuter LAE der Kategorie C & D sinnvoll, um Patient*innen mit höherem Risiko für kurzfristige unerwünschte Ereignisse zu identifizieren
- bei hämodynamisch stabilen Patient*innen mit akuter LAE der Kategorie C & D können NEWS und NEWS2 sinnvolle Alternativen zu LAE-spezifischen Risikoscores sein, um Patient*innen mit höherem Risiko für kurzfristige unerwünschte Ereignisse zu identifizieren
klinische Risikobewertungsscores für akute LAE
Pulmonary Embolism Severity Index (PESI)
– Alter (Alter in Jahren = Punkte)
– männliches Geschlecht (10 Punkte)
– Krebsvorerkrankung (30 Punkte)
– Herzinsuffizienz in der Anamnese (10 Punkte)
– chronische Lungenerkrankung (10 Punkte)
– HF ≥ 110/min (20 Punkte)
– RRsys < 100 mmHg (30 Punkte)
– AF ≥ 30/min (20 Punkte)
– Körpertemperatur < 36 °C (20 Punkte)
– Bewusstseinsstörung (60 Punkte)
– SpO2 < 90 % (20 Punkte)
Auswertung
Klasse I (geringstes Risiko): ≤ 65 Punkte
Klasse II: 66 – 85 Punkte
Klasse III: 86 – 105 Punkte
Klasse IV: 106 – 125 Punkte
Klasse V (höchstes Risiko): ≥ 126 Punkte
simplified Pulmonary Embolism Severity Index (sPESI)
– Alter > 80 Jahre (1 Punkt)
– Krebserkrankung in der Vergangenheit (1 Punkt)
– chronische kardiopulmonale Erkrankung (1 Punkt)
– HF ≥ 110/min (1 Punkt)
– RRsys < 100 mmHg (1 Punkt)
– SpO2 < 90 % (1 Punkt)
Auswertung
0 Punkte: geringes Risiko der 30-Tage-Mortalität
≥1 Punkt: hohes Risiko der 30-Tage-Mortalität
Bova-Score
– RRsys 90 – 100 mmHg (2 Punkte)
– erhöhte kardiale Troponinwerte (2 Punkte)
– rechtsventrikuläre Dysfunktion (2 Punkte)
– HF ≥ 110/min (1 Punkt)
Auswertung
Stadium I (geringstes Risiko): 0 – 2 Punkte
Stadium II: 3 – 4 Punkte
Stadium III (höchstes Risiko): > 4 Punkte
Hestia-Kriterien
– Patient*in hämodynamisch instabil?
– Thrombolyse oder Embolektomie erforderlich?
– aktive Blutung oder hohes Blutungsrisiko vorliegend?
– O2 länger als 24 h nötig, um SpO2 > 90 % aufrechtzuerhalten?
– LAE während Antikoagulationstherapie diagnostiziert?
– Schmerzen so stark, sodass diese eine i.v.-Analgesie über > 24 h erfordern?
– medizinische oder soziale Gründe für KH-Aufenthalt von > 24 h vorliegend? (z.B. Infektion, Krebs, fehlende Unterstützung durch ein soziales Netzwerk)
– Kreatinin-Clearance < 30 mL/min?
– schwere Leberfunktionsstörung vorliegend?
– Patientin schwanger?
– dokumentierte Heparin-induzierte Thrombozytopenie in der Anamnese vorliegend?
Auswertung
alle Antworten „Nein“ = Hestia-Rule negativ –> ambulante Therapie erwägen
mind. eine Antwort „Ja“ = Hestia-Rule positiv –> stationäre Aufnahme erwägen
Composite Pulmonary Embolism Shock (CPES) Score
– erhöhtes kardiales Troponin (1 Punkt)
– erhöhtes B-Typ-natriuretisches Peptid (1 Punkt)
– mäßig bis schwer eingeschränkte rechtsventrikuläre Funktion (1 Punkt)
– zentrale Thrombuslast (Sattel-Lungenembolie; 1 Punkt)
– begleitende tiefe Venenthrombose (1 Punkt)
– HF ≥ 100/min (1 Punkt)
Auswertung
0 – 5 Punkte: geringeres Risiko für normotensiven Schock (Herzindex ≤ 2,2 L/min/m²)
6 Punkte: höheres Risiko für normotensiven Schock
hämodynamische Beurteilung
- Untersuchung bzgl. des Vorliegens eines normotensiven Schocks bei Patient*innen mit akuter LAE der Kategorie D2, um Patient*innen mit erhöhtem Risiko für klinische Verschlechterung und KH-Aufenthalt zu identifizieren (normotensiver Schock = isolierte Hypoperfusion ohne Hypotonie, die anhand eines der folgenden Marker festgestellt wird: Serumlaktat > 2 mmol/L, Urinausscheidung < 720 mL in 24 h, Kreatininanstieg ≥ 0,3 mg/mL in 24 h, Herzindex ≤ 2,2 L/min/m2 aus peripheren arteriellen und gemischten venösen SpO2-Werten)
- MAP <80 mmHg bei Patient*innen mit akuter LAE der Kategorie C3 hilfreich, um Patient*innen zu identifizieren, die ggf. eine Intensivierung der Therapie benötigen
Biomarker für Risikostratifizierung
- Messung mindestens eines kardialen Biomarkers (d.h. Troponin, BNP) bei Patient*innen mit akuter LAE und erhöhtem klinischem Schweregrad ohne Anzeichen von Hypotonie oder Schock (d.h. AHA/ACC-Lungenembolie-Kategorie C) empfohlen, um die Risikostratifizierung für kurzfristige Komplikationen und/oder Mortalität zu unterstützen
- Messung von Laktat (entweder venös oder arteriell) bei Patienten mit akuter LAE (d.h. Kategorien C bis E), die in Notfallaufnahme untersucht werden, empfohlen, um die Risikostratifizierung für kurzfristige Komplikationen und/oder Mortalität zu unterstützen
Bildgebung der rechten Herzkammer zur Risikostratifizierung
- RV-Bildgebung zur kurzfristigen Risikostratifizierung bei akuter LAE mit erhöhtem klinischem Schweregrad, aber ohne Schockzeichen empfohlen (d.h. Kategorien C bis D)
- Echokardiographie ggü. CT bevorzugen
Quantifizierung der Thrombuslast für kurzfristige Risikostratifizierung
- keine Empfehlung für Quantifizierung der angiographischen Thrombuslast zur kurzfristigen Risikostratifizierung bei Patient*innen mit akuter LAE der Kategorien A bis C
Akutmanagement
Überlegungen zur Entscheidung über die Einweisung ins Krankenhaus
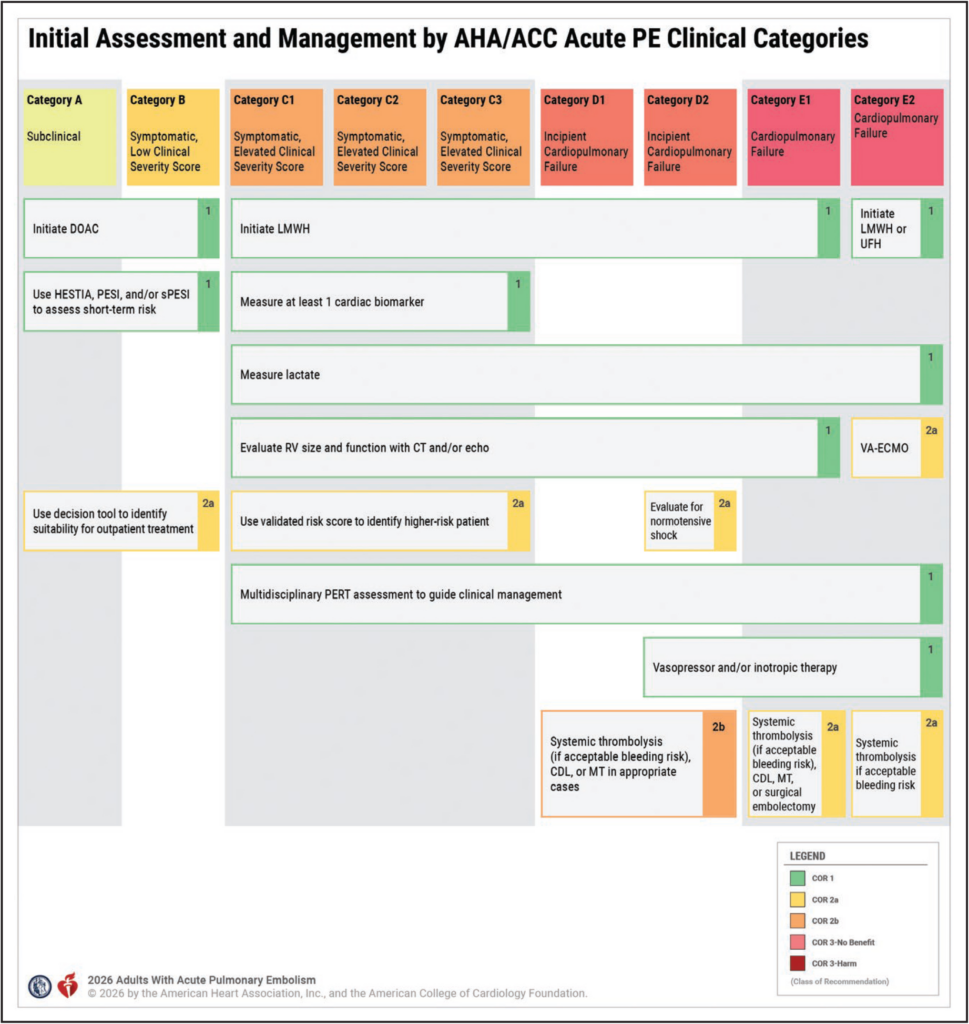
ambulante Versorgung
- Entscheidungsinstrumente wie z.B. Hestia-Rule, PESI und sPESI nutzen, um die Eignung für eine ambulante Behandlung zu prüfen
- bei ausgewählten Patient*innen, bei denen eine akute LAE der Kategorien A und B diagnostiziert wurde, ist eine ambulante Behandlung eine sinnvolle Option im Vergleich zum KH-Aufenthalt, wenn die Rate der unerwünschten Ereignisse innerhalb von 90 Tagen gering ist und dies den Zielen des Patienten entspricht (sofortiger Zugang zu Antikoagulanzien und schnelle, zuverlässige und fachkundige Nachsorge notwendig)
Einweisung ins Krankenhaus bzw. stationäre Behandlung
- bei akuter LAE mit Thrombolysetherapie (systemisch oder katheter-gestützt) Versorgung auf ITS oder IMC mit engmaschiger Überwachung
- bei akuter, hämodynamisch stabiler LAE mit mechanischer Thrombektomie ist die Aufnahme auf Station sinnvoll, die eine kontinuierliche Telemetrie und Pflege ermöglicht
Interhospitaltransfer
- bei akuter, hämodynamisch stabiler LAE der Kategorie C3 bis D mit Hochrisikomerkmalen (z.B. Rechtsherzinsuffizienz und erhöhte kardiale Biomarker) Verlegung in ein Zentrum mit erweiterten Möglichkeiten anbieten (z.B. chirurgische Embolektomie, kathetergesteuerte Thrombolyse, mechanische Thrombektomie, ECMO und IVC-Filter)
- instabile Patient*innen mit akuter Lungenembolie (Kategorie E) nicht in ein anderes Zentrum verlegen, bevor sich ihr Zustand stabilisiert hat
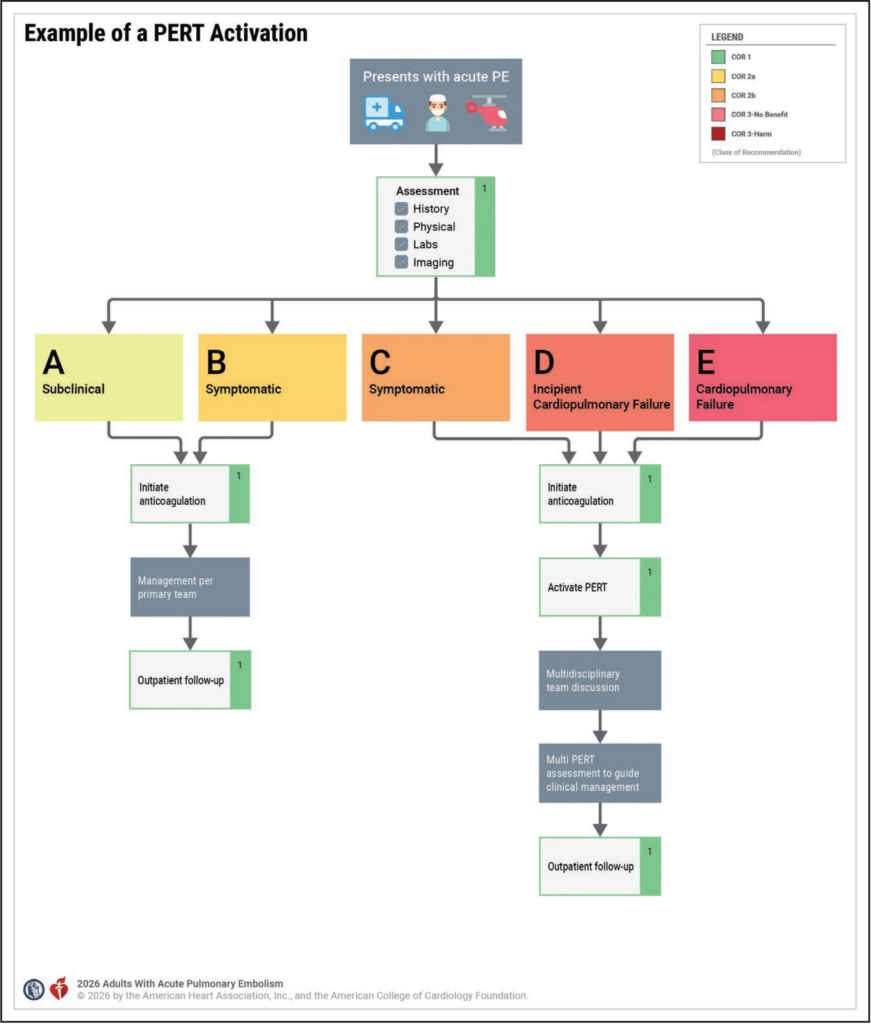
Pulmonary Embolism Response Team (PERT)
- multidisziplinäre Beurteilung durch PERT bei akuter LAE der Kategorie C bis E empfohlen (Kategorien A oder B mit mehreren Begleiterkrankungen können ebenfalls von PERT profitieren)
Vorteile des PERT-Programm
– verbesserte Risikostratifizierung
– vielfältige Erkenntnisse verschiedener Spezialist*innen
– Auswahl und sachgerechter Einsatz fortschrittlicher Therapien
– Implementierung evidenzbasierter Protokolle und Behandlungspfade
– Weiterbildung von Kollegen und Auszubildenden
– Förderung von Wegen für eine angemessene Nachsorge
– Schließung von Evidenzlücken
mögliche PERT-Mitglieder
– Gefäßmedizin
– Pneumologie/Intensivmedizin
– Herzchirurgie
– nicht-interventionelle Kardiologie
– interventionelle Radiologie
– Radiologie
– Gefäßchirurgie
– interventionelle Kardiologie
– Hämatologie/Onkologie
– Notfallmedizin
– Pflege
– Pharamakologie/Apotheke
– Patient*innen und Angehörige
medizinische Behandlung
Antikoagulation
- allgemeine Empfehlungen
- Antikoagulationstherapie bei Patient*innen mit akuter LAE, die keine absoluten Kontraindikationen haben
- niedermolekulares Heparin (LMHW) ggü. unfraktioniertem Heparin (UFH) vorziehen bei akuter LAE der Kategorien C1 bis E1
- wenn orale Antikoagulation bei akuter LAE in Frage kommt, DOAK ggü. Vitamin-K-Antagonisten (VKA) vorziehen, sofern keine Kontraindikationen vorliegen
- therapeutische Antikoagulation bei V.a. akuter LAE der Kategorie C2 oder höher mit geringem Blutungsrisiko ggf. vorteilhaft, wenn die Bildgebung verzögert oder nicht sofort verfügbar ist
- besondere Überlegungen bei Adipositas
- bei Adipositas (BMI > 30 kg/m²) und akuter LAE, die orale Antikoagulanzien erhalten, DOAK ggü. Vitamin-K-Antagonisten vorziehen
- bei Adipositas Klasse III (BMI > 40 kg/m²) und akuter LAE, die LMWH erhalten, kann eine Dosis-Reduzierung sinnvoll sein, um das Blutungsrisiko zu senken
- besondere Überlegungen bei Antiphospholipid-Syndrom
- bei akuter LAE und nachgewiesenem Antiphospholipid-Syndrom zur Prävention venöser und arterieller Thrombosen VKA ggü. DOAK bevorzugen
- bei akuter LAE mit nur einem einzigen nachgewiesenem Anticardiolipin- oder β2-Glykoprotein-Antikörper kann ein DOAK eine sinnvolle Alternative
- besondere Überlegungen bei primärem oder metastasierendem Hirntumor
- bei akuter LAE und primären/metastasierten Hirntumoren, die ansonsten für eine orale Antikoagulation in Frage kommen, kann ein DOAK ggü. LMWH erwogen werden
- besondere Überlegungen bei chronischer Nierenerkrankung
- bei akuter LAE und leichter bis mittelschwerer chronischer Nierenerkrankung (Stadium 2 – 3), die eine orale Antikoagulanzientherapie benötigen, DOAK ggü. VKA bevorzugen
- bei schwerer Nierenerkrankung (Stadium 4 – 5) oder Nierenerkrankung im Endstadium unter Hämodialyse und bestätigter LAE, die orale Antikoagulanzientherapie benötigt, ist unklar, ob Apixaban zur Verringerung schwerer Blutungen besser geeignet ist als VKA
- besondere Überlegungen bei Schwangerschaft
- bei akuter LAE während der Schwangerschaft, die eine Antikoagulation benötigt, LMWH oder UFH verwenden
- CAVE: DOAK und Warfarin potenziell schädlich –> Gefahr von Fehlgeburten oder fetalen Anomalien
- besondere Überlegungen während des Stillens
- bei akuter LAE während der Stillzeit werden LMWH, UFH oder Warfarin ggü. DOAK empfohlen
- besondere Überlegungen bei chronischer Lebererkrankung
- Therapie mit DOAK anstelle von VKA bei akuter LAE und chronischer Lebererkrankung der Child-Pugh-Klasse A & B sinnvoll
- keine Empfehlung für Therapie mit DOAK anstelle von VKA bei akuter LAE und chronischer Lebererkrankung der Child-Pugh-Klasse C (CAVE: erhöhte Gefahr von Blutungen)
- besondere Überlegungen bei endovaskulären Eingriffen
- gleichzeitige therapeutische Antikoagulation (LMWH oder UFH) oder subtherapeutische Antikoagulation (UFH) ggü. keiner Antikoagulation empfohlen bei akuter LAE, die sich einer kathetergesteuerten Thrombolyse
- initiale parenterale Antikoagulation mit LMWH ggü. UFH bei Patient*innen mit akuter LAE vorziehen, die sich einem endovaskulären Eingriff unterzogen haben oder eine thrombolytische Therapie erhalten haben
- LMWH ggü. UFH sinnvoll bei Patient*innen mit akuter LAE, bei denen wahrscheinlich endovaskuläre Eingriffe zur Behandlung der Lungenembolie durchgeführt werden
- Antikoagulationsüberwachung und besondere Überlegungen
- bei akuter LAE, bei der LMWH überwacht wird, 3 – 5 h nach LMWH-Dosis, sobald Steady State erreicht ist (≥ 3 Dosen), den max. Anti-Xa-Spiegel messen anstatt Überprüfung des Talspiegel oder zufälliger Spiegel, um möglichst genau festzustellen, ob sich die Patient*innen innerhalb des erwarteten therapeutischen Bereichs befinden
- bei akuter LAE mit schwerer chronischer Nierenerkrankung (CrCl < 30 mL/min), die mit LMWH behandelt wurde, ost die Überwachung des Anti-Xa-Spiegel sinnvoll, um die Dosis anzupassen und so das Blutungsrisiko zu verringern
- bei Schwangeren, die wegen einer akuten LAE mit LMWH behandelt werden, ist die Nützlichkeit einer mind. einmal pro Trimester durchgeführten Überwachung des max. Anti-Xa-Spiegels zur Dosiseinstellung und zur Verringerung des Blutungs- und/oder Thromboembolierisikos nicht eindeutig erwiesen
- bei Körpergewicht > 150 kg oder BMI > 40 kg/m2 und akuter LAE unter LMWH-Therapie ist der Nutzen einer Überwachung der Anti-Xa-Spiegel zur Vermeidung supratherapeutischer LMWH-Spiegel nach der Initialtherapie nicht erwiesen
- bei LAE, die auf ITS mit LMWH behandelt wird, ist der Nutzen einer Überwachung der Anti-Xa-Spiegel zur Vermeidung supratherapeutischer und/oder subtherapeutischer Spiegel nicht erwiesen
- Antikoagulationsüberwachung und besondere Überlegungen ist der Nutzen einer Überwachung der Anti-Xa-Spiegel und eine Dosisanpassung zur Verringerung wiederkehrender VTE oder Blutungen nicht erwiesen
hämodynamische Pharmakotherapie
- Verwendung von Vasopressoren und/oder Inotropika empfohlen bei akuter LAE (Kategorie D2 – E2) mit kardiogenem Schock
- bei akuter LAE der Kategorien D1 bis D2, bei denen aufgrund der klinischen Beurteilung eine verminderte Vorlast zu befürchten ist, kann die Verwendung normaler Kochsalzlösung oder anderer Infusionslösungen erwogen werden, um das HZV und den RR zu verbessern
- Verwendung inhalativer pulmonaler Vasodilatatoren in Betracht ziehen bei akuter LAE der Kategorien C2 bis E, um die RV-Nachlast zu reduzieren
Sedierung und Beatmungsstrategien
- hämodynamische unterstützende Therapien (Vasopressoren, Inotropika und/oder venoarterielle [VA]-ECMO) sollten bei akuter LAE der Kategorie C bis E, die zur Intubation sediert werden müssen, zur Verfügung stehen
- bei akuter LAE mit mittelschwerer bis schwerer Hypoxie kann die HFNC-Beatmung anstelle einer normalen O2-Gabe mittels Nasenbrille von Vorteil sein
- tiefe Sedierung und mechanische Beatmung nur bei klinischer Indikation bei akuter LAE der Kategorien C bis E durchführen, um einen hämodynamischen Kollaps zu vermeiden
mechanische Kreislaufunterstützung
- Fortsetzung der parenteralen systemischen Antikoagulation bei bekannter oder vermuteter akuter LAE unter VA-ECMO empfohlen, sofern keine Blutungen vorliegen
- Einsatz von VA-ECMO bei akutem, refraktärem kardiogenem Schock infolge einer bekannten oder vermuteten akuten Lungenembolie (Kategorie E2), sofern geeignete Ressourcen verfügbar sind, um die Hämodynamik zu stabilisieren und die Sauerstoffversorgung zu verbessern
- bei akuter LAE der Kategorie E2 mit VA-ECMO-Therapie ist der Nutzen zusätzlicher erweiterter Therapien nicht eindeutig belegt
Rolle von Vena-Cava-Filtern
- wieder entfernbare ggü. permanenten Filtern bei Patient*innen mit akuter LAE, die keine Antikoagulation vertragen, bei denen jedoch ein IVC-Filter als notwendig erachtet wird, bevorzugen
- sobald das Risiko einer Lungenembolie ausreichend gesunken ist und Antikoagulation ohne Probleme möglich ist, Versuch der Entfernung von wieder entfernbaren Filtern, um das Risiko langfristiger filterbedingter Komplikationen zu minimieren
- bei Patient*innen mit akuter LAE, die keine Antikoagulation vertragen, können Filter in der Vena Cava inferior helfen die kurzfristige Inzidenz wiederkehrender Lungenembolien zu reduzieren
- strukturierte Nachsorgeprogramme bei permanenten Vena-Cava-Filtern sinnvoll
- bei akuter LAE der Kategorie D bis E, die erweiterte Maßnahmen unterziehen (z.B. systemische Thrombolyse, kathetergestützte Lyse, mechanische Thrombektomie oder chirurgischer Embolektomie) ist der Nutzen einer Filter-Platzierung zur Verringerung der kurzfristigen Inzidenz wiederkehrender Lungenembolien und der Mortalität ungewiss
- bei rezidivierender Lungenembolie der Kategorien B bis E trotz optimaler therapeutischer Antikoagulation kann die Filter-Platzierung erwogen werden, um die kurzfristige Inzidenz einer weiteren rezidivierenden Lungenembolie zu senken
- keine routinemäßige Filter-Platzierung bei akuter LAE mit therapeutischer Antikoagulation
erweitertes Management
- Einsatz erweiterter Therapieansätze bei akuter LAE der Kategorien C3 bis E2 mit Anzeichen für frei schwebende Gerinnsel im rechten Vorhof und/oder im rechten Ventrikel ggü. der alleinigen Antikoagulation
- bei akuter LAE der Kategorien C2 bis D2 ohne Thrombolyse-Kontraindikationen, bei der erweiterte Therapien in Betracht gezogen werden ist die Überlegenheit einer kathetergestützten Lyse oder einer mechanischen Thrombektomie hinsichtlich der Verringerung der Mortalität oder schwerer Blutungen ungewiss
systemische Thrombolyse
- systemische Thrombolyse und Antikoagulation ggü. alleiniger Antikoagulation bei akuter LAE der Kategorien E1 – E2 und akzeptablem Blutungsrisiko sinnvoll, bei Patient*innen, bei denen erweiterte Therapien in Betracht gezogen werden
- systemische Thrombolyse und Antikoagulation ggü. alleiniger Antikoagulation in Betracht ziehen bei akuter LAE der Kategorien D1 – D2 und akzeptablem Blutungsrisiko, wenn bei dieser erweiterte Therapien in Betracht gezogen werden
- bei akuter LAE mit systemischer Thrombolyse kann eine niedrigere Dosis systemischer Thrombolytika in Betracht gezogen werden, um das Blutungsrisiko zu verringern
- bei akuter LAE der Kategorien A1 bis C2 systemische Thrombolyse aufgrund des erhöhten Risikos für schwere Blutungen und intrazerebrale Blutungen nicht ggü. alleiniger Antikoagulation bevorzugen
kathetergestützte Thrombolyse
- kathetergestützte Thrombolyse in Kombination mit Antikoagulation sinnvoll bei akuter LAE der Kategorie E1
- bei akuter LAE der Kategorien D1 – D2, bei der erweiterte Therapien erwogen werden, kathetergestützte Thrombolyse in Kombination mit Antikoagulation in Betracht ziehen, um weitere klinische Verschlechterung zu verhindern
- Nutzen der kathetergestützten Thrombolyse in Kombination mit Antikoagulation ggü. alleiniger Antikoagulation zur Prävention von Komplikationen und zur Verbesserung der langfristigen Mortalität, der Funktionsfähigkeit und der Lebensqualität unklar bei akuter LAE der Kategorien C2 – C3
- bei akuter LAE der Kategorien D1 bis E1, bei der eine Thrombolyse in Betracht gezogen wird, ist der Nutzen der kathetergestützter Thrombolyse ggü. einer systemischen Thrombolyse zur Prävention von Komplikationen und zur Verbesserung der langfristigen Mortalität, der Funktionsfähigkeit und der Lebensqualität unklar, aber kathetergestützter Thrombolyse kann ggü. systemischer Thrombolyse erwogen werden, um das Risiko schwerer Blutungen zu verringern
- bei akuter LAE, welche mit kathetergestützter Thrombolyse therapiert wird, wird eine reduzierte Thrombolysedosis von < 5 mg Alteplase pro Lungenarterie ggü. Standarddosis von 5 – 10 mg Alteplase pro Lungenarterie nicht empfohlen
- keine Empfehlung für kathetergestützte Thrombolyse ggü. alleiniger Antikoagulation bei akuter LAE der Kategorien A bis C1
mechanische Thrombektomie
- mechanische Thrombektomie plus Antikoagulation ggü. alleiniger Antikoagulation bei akuter LAE der Kategorie E1 bevorzugen
- bei akuter LAE der Kategorien D1 – D2, bei der erweiterte Therapien in Betracht gezogen werden, mechanische Thrombektomie plus Antikoagulation ggü. alleiniger Antikoagulation bevorzugen
- bei akuter LAE der Kategorien C2 – C3 ist der Nutzen der mechanischen Thrombektomie plus Antikoagulation ggü. alleiniger Antikoagulation bzgl. der Prävention von Komplikationen und zur Verbesserung der langfristigen Mortalität, der Funktionsfähigkeit und der Lebensqualität unklar
- bei akuter LAE der Kategorien D1 bis E1, bei der erweiterte Therapien in Betracht gezogen werden, ist der Nutzen einer mechanischen Thrombektomie ggü. einer systemischen Thrombolyse unklar, aber die mechanische Thrombektomie kann ggü. einer systemischen Thrombolyse in Betracht gezogen werden, um das Risiko schwerer Blutungen zu verringern
- keine Empfehlung für die mechanische Thrombektomie ggü. einer alleinigen Antikoagulation zur Verbesserung des klinischen Outcomes oder Symptome bei akuter LAE der Kategorien A bis C1
chirurgische Embolektomie
- bei akuter LAE der Kategorie E1 ist eine chirurgische Embolektomie ggü. einer alleinigen Antikoagulation sinnvoll
- bei akuter LAE der Kategorien D1 – D2, bei der erweiterte Therapien in Betracht gezogen werden, kann eine chirurgische Embolektomie in Kombination mit Antikoagulation ggü. einer alleinigen Antikoagulation in Betracht gezogen werden
- bei akuter LAE der Kategorien D1 bis E1, die für OP in Frage kommt und bei der erweiterte Therapien in Betracht gezogen werden, ist der Nutzen einer chirurgischen Embolektomie ggü. einer systemischen Thrombolyse unklar, aber eine chirurgische Embolektomie kann ggü. einer systemischen Thrombolyse in Betracht gezogen werden, um das Risiko einer ICH zu verringern
- keine Empfehlung für chirurgische Embolektomie ggü. alleiniger Antikoagulation bei akuter LAE der Kategorien A bis C3
- keine Empfehlung für chirurgische Embolektomie ggü. anderer erweiterter Therapien bei LAE der Kategorie E2, die keine mechanische Kreislaufunterstützung erhält
Monitoring & Follow-up
Nachsorge bei akuter Lungenembolie
- bei akuter LAE ist eine klinische Nachuntersuchung innerhalb der ersten Woche nach der Entlassung sinnvoll (Aufklärung der Patient*innen, Probleme bei Antikoagulationstherapie beseitigen, Sicherstellen der Medikamentencompliance und Erkennung von Blutungskomplikationen)
- Arzttermin spätestens 3 Monate nach Diagnose, um Dauer der Antikoagulation zu besprechen, Bedarf an weiteren Untersuchungen zu überprüfen und persistierende Lungenembolie-bedingte Symptome abzuklären
- mind. 1 Jahr lang bei jedem Besuch Abklärung von Lungenembolie-bedingten Symptomen und funktionellen Einschränkungen, chronisch-thromboembolische Lungenerkrankung (CTEPD) oder andere Ursachen für Atemnot und funktionelle Einschränkungen auszuschließen
- regelmäßige Neubewertung des Nutzen-Risiko-Verhältnisses der fortgesetzten Antikoagulation bei Patient*innen, die auch in der verlängerten Phase (> 3 bis 6 Monate nach Diagnose) eine Antikoagulation erhalten
- Einsatz allgemeiner oder krankheitsspezifischer Fragebögen zur Erfassung von Angstzuständen und Depressionen im Rahmen der Nachuntersuchungen sinnvoll
- Nachsorge in einer spezialisierten Lungenembolie-Ambulanz (sofern verfügbar) zur Optimierung der Behandlung bei ausgewählten komplexen Patient*innen sinnvoll
- bei Patient*innen, die nach 3 – 6 Monate weiterhin Symptome aufweisen, kann ein Leistungstest (z. B. 6-Minuten-Gehtest, „Incremental shuttle walk“-Test, Ausdauer-Shuttle-Gehtest) sinnvoll sein, um körperliche Einschränkungen zu quantifizieren und diejenigen Patient*innen zu identifizieren, die einer weiterführenden Diagnostik bedürfen
Krebsvorsorge und Thrombophilie-Testung bei fehlenden Risikofaktoren für eine Lungenembolie
- gründliche Anamnese, körperliche Untersuchung und altersentsprechende Krebsvorsorge bei akuter LAE ohne identifizierbare Risikofaktoren, um bisher unentdeckte Krebserkrankung zu diagnostizieren
- Testung auf genetische und erworbene Thrombophilie bei Patient*innen ohne wesentliche reversible Risikofaktoren für akute LAE, die eine familiäre Thromboseanamnese aufweisen oder < 55 Jahre sind, ggf. sinnvoll, wenn die Testergebnisse voraussichtlich die Therapie beeinflussen oder die Risikothematisierung in der Familie verbessern
- keine Empfehlung für routinemäßige Bildgebung mittels CT oder PET-CT zur Diagnose einer bisher unentdeckten Krebserkrankung
Verhütung, Schwangerschaft und Hormontherapie
- Aufklärung über Verhütungs- und Antikoagulationsmöglichkeiten für den Fall einer Schwangerschaft bei Patientinnen im gebärfähigen Alter mit akuter LAE
- Betreuung durch ein auf thrombotische Komplikationen spezialisiertes Team bei Patientinnen, die nach einer Lungenembolie schwanger werden, hilfreich, um schwangerschaftsbedingte Komplikationen zu minimieren
- bei Therapie mit Antikoagulanzien aufgrund einer Präeklampsie oder einem Risiko für abnorme Uterusblutungen, ist es sinnvoll, medikamentöse Maßnahmen (z.B. Hormontherapien), alternative Antikoagulationsstrategien und gynäkologische Interventionen zur Risikominderung abnormer Uterusblutungen zu erörtern, anstatt die Antikoagulation abzubrechen
- Fortsetzung oder Beginn einer Hormontherapie bei akuter Präeklampsie erwägen, wenn das Nutzen-Risiko-Verhältnis günstig ist und die Patientin weiterhin Antikoagulanzien einnimmt
Patient*innenaktivitäten und Reisen
- Förderung der frühzeitigen Mobilisierung anstelle von Bettruhe bei Erholung nach akuter LAE, um das Komplikationsrisiko zu senken
- Tragen von Kompressionsstrümpfen während Langstreckenreisen (≥ 5 h) hilfreich bei Patient*innen mit akuter LAE in der Anamnese, um das TVT-Risiko zu minimieren
- einmalige prophylaktische Gabe eines oralen Antikoagulans oder von parenteralem NMH am Tag der Langstreckenreise ggf. sinnvoll, um das Risiko einer erneuten venösen Thromboembolie (VTE) zu reduzieren
- bei Z.n. akuter LAE der Kategorien C2 bis E kann es sinnvoll sein, Langstreckenreisen für 4 Wochen nach Behandlungsbeginn oder nach Abklingen der Symptome zu vermeiden, um das Risiko von Nebenwirkungen zu reduzieren
Antikoagulationstherapie nach Rezidivrisiko
- Fortsetzung der Antikoagulation über die initiale Behandlungsphase (3 – 6 Monate) hinaus in die verlängerte Behandlungsphase bei erstmaliger akuter LAE ohne wesentliche reversible Risikofaktoren vorteilhaft
- bei erstmaliger akuter LAE aufgrund eines wesentlichen reversiblen Risikofaktors Antikoagulation nach initialer Behandlungsphase (3 – 6 Monate) beenden, anstatt sie in die verlängerte Behandlungsphase fortzusetzen
- Fortsetzung der Antikoagulation von der initialen Behandlungsphase (3 – 6 Monate) bis in die verlängerte Behandlungsphase bei erstmaliger LAE aufgrund eines persistierenden Risikofaktors sinnvoll
- DOAK-Therapie ggü. VKA-Therapie, wenn eine Antikoagulation über die initiale Behandlungsphase (3 – 6 Monate) hinaus in die verlängerte Behandlungsphase angeboten wird und keine Kontraindikationen bestehen
- DOAK oder LMWH bei LAE und Krebs empfohlen, bei der über die initiale Behandlungsphase (3 – 6 Monate) hinaus eine Antikoagulation in der verlängerten Behandlungsphase angeboten wird
- VKA anstelle von Aspirin oder keiner Therapie bei Patient*innen mit LAE ohne Krebs, denen über die initiale Behandlungsphase (3 – 6 Monate) hinaus eine Antikoagulation in der verlängerten Behandlungsphase angeboten wird
- Behandlung mit Apixaban oder Rivaroxaban mit halber Dosis bei Patient*innen mit LAE, denen über die initiale Behandlungsphase (3 – 6 Monate) hinaus eine Antikoagulation in der verlängerten Behandlungsphase angeboten wird
- gemeinsame Entscheidungsfindung hinsichtlich des Absetzens der Antikoagulation nach initialer Behandlungsphase (3 – 6 Monate) oder Fortsetzung in die verlängerte Behandlungsphase bei Patient*innen mit erster akuter LAE aufgrund eines geringfügigen, reversiblen Risikofaktors sinnvoll
- Gabe von niedrig dosiertem Aspirin ggü. keiner Therapie sinnvoll bei Patient*innen, denen eine Antikoagulation über die initiale Behandlungsphase (3 – 6 Monate) hinaus in der verlängerten Behandlungsphase angeboten wird
Risikofaktoren für venöse Thromboembolien
| schwerwiegende reversible Risikofaktoren | geringfügige reversible Risikofaktoren | anhaltende Risikofaktoren |
|---|---|---|
| – Operation unter Vollnarkose (≥ 30 Minuten) – Krankenhausaufenthalt aufgrund einer akuten Erkrankung (≥ 72 Stunden) mit Bettlägerigkeit – Kaiserschnitt – Unterschenkelfraktur | – Operation unter Vollnarkose < 30 Minuten – Krankenhausaufenthalt aufgrund einer akuten Erkrankung < 72 Stunden – akute Erkrankung außerhalb des Krankenhauses ≥ 72 Stunden mit Bettlägerigkeit – Östrogentherapie (Hormonersatz oder Kontrazeption) – Peripartale Phase – Trauma mit eingeschränkter Mobilität ≥ 72 Stunden | – aktive Kreberkrankung mit oder ohne laufende Behandlung – Autoimmunerkrankung (z. B. rheumatoide Arthritis, systemischer Lupus erythematodes) – chronisch-entzündliche Darmerkrankung – chronische Immobilität |
rezidivierende Lungenembolie
- Empfehlung für radiologische Bildgebung mittels CTPA oder V/Q-Scan bei Patient*innen mit LAE in der Anamnese, die neue Symptome/Anzeichen einer rezidivierenden oder Durchbruchs-Lungenembolie (Lungenembolie trotz laufender, therapeutisch korrekter Antikoagulation) aufweisen
- Empfehlung für Abklärung bei Patient*innen mit LAE in der Anamnese und dokumentierter rezidivierender LAE trotz Antikoagulationstherapie, um klinische und pharmakologische Faktoren zu identifizieren, die zu einer rezidivierenden Lungenembolie beitragen können
- Wechsel der Therapie auf eine andere Wirkstoffklasse anstelle der Fortsetzung der Therapie mit derselben Wirkstoffklasse bei Patient*innen mit rezidivierender Lungenembolie, die die verordnete Antikoagulation in der richtigen therapeutischer Intensität einhalten
- Antikoagulation mit DOAK in voller Dosis innerhalb derselben Klasse bei Patient*innen mit dokumentierter rezidivierender akuter LAE unter Einhaltung der Antikoagulation mit DOAK in reduzierter Dosis
- Dosiserhöhung von NMH um 20 – 25 % bei Krebspatient*innen mit rezidivierender LAE trotz therapeutischer Antikoagulation mit NMH
Komplikationen und Folgeschäden
Patient*innen mit anhaltenden Symptomen nach akuter LAE
Evaluation
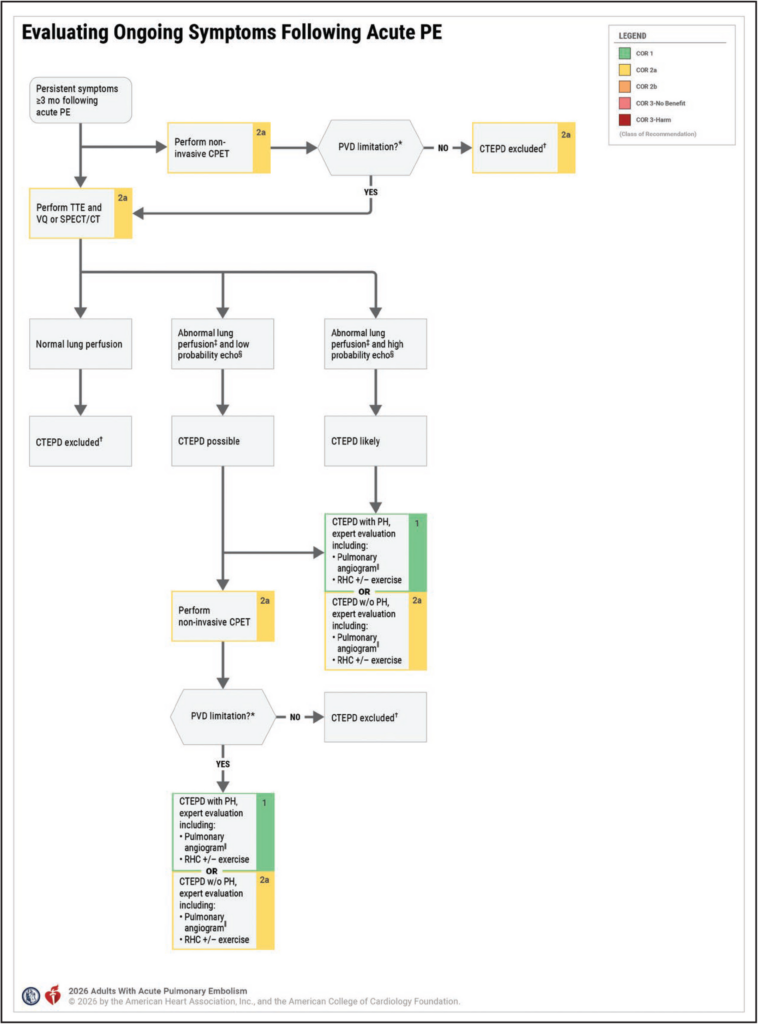
- diagnostische Abklärung zur Beurteilung einer CTEPD bei Patient*innen mit anhaltender Dyspnoe und/oder funktioneller Einschränkung nach mind. dreimonatiger therapeutischer Antikoagulation nach akuter LAE
- TTE und Lungenperfusionsszintigraphie (planare V/Q-Szintigraphie oder V/Q-SPECT, SPECT/CT) zusätzlich zur alleinigen Echokardiographie bei Patient*innen, die sich einer diagnostischen Abklärung bzgl. einer CTEPD unterziehen
- kardiopulmonaler Belastungstest (CPET) zur Abklärung einer CTEPD sinvoll bei Patient*innen, die sich einer diagnostischen Abklärung einer CTEPD unterziehen
- Kontroll-CTPA oder Lungenperfusionsszintigraphie (planare V/Q-Szintigraphie, V/Q-SPECT, SPECT/CT) zur Beurteilung des Ausmaßes der Thrombusauflösung nicht hilfreich bei Patient*innen mit akuter LAE in der Anamnese, deren Symptome abgeklungen sind und bei denen kein V.a. CTEPD besteht
Management
- Antikoagulation bis zum Abschluss der Abklärung einer CTEPD fortsetzen, sofern keine Kontraindikation aufgrund eines hohen Blutungsrisikos besteht
- pulmonales Rehabilitationsprogramm zur Verbesserung der Symptome und der Belastbarkeit sinnvoll bei Patient*innen, bei denen eine CTEPD ausgeschlossen wurde, die aber trotz mind. dreimonatiger therapeutischer Antikoagulation nach akuten LAE weiterhin unter Dyspnoe und/oder funktionellen Einschränkungen leiden
- Überweisung an ein spezialisiertes Zentrum für die Behandlung von CTEPD bei bestätigter CTEPD und pulmonaler Hypertonie, um Diagnostik und Therapie zu optimieren
- Überweisung an ein spezialisiertes Zentrum für die Behandlung von CTEPD bei ausgewählten Patient*innen mit CTEPD-Diagnose ohne PH ggf. von Vorteil


Sei der Erste der einen Kommentar abgibt