veröffentlichende Fachgesellschaft: Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin (DGP)
Klassifikation gemäß AWMF: S2k
Datum der Veröffentlichung: 28.05.2024
Ablaufdatum: 27.05.2029
Quelle/Quelllink: https://register.awmf.org/de/leitlinien/detail/020-030
Grundsätzliches
- Bronchiektasen-Prävalenz nimmt weltweit seit einigen Jahren stetig zu
- zw. 2009 und 2017 kontinuierliche jährliche Zunahme der Diagnoseprävalenz unter gesetzlich Krankenversicherten um ca. 10 % in Deutschland
- Prävalenzrate: ca. 120/100.000 (also > 100.000 Menschen mit Bronchiektasen in BRD)
- Prävalenz zw. 36 und 566 pro 100.000 Einwohner in Europa
- Betroffenen in Europa im Durchschnitt 67 Jahre alt und in 61% weiblich (ca. 60 Jahre in BRD)
- auf die Erkrankung zurückzuführende, jährliche direkte und indirekte Ausgaben für das Jahr 2018 beliefen sich auf mehr als 38.500.000 €
- gezielte Therapie der Grunderkrankung stellt die effektive kausale Therapie dar und weist i.d.R. den höchsten Effizienzgrad zur Verbesserung der Lebensqualität der Betroffenen auf
Definitionen
- Begriff „Bronchiektasen“ oder „Bronchiektasie“ wird sowohl für die vergleichsweise charakteristische Erkrankung, als auch den radiologischen Befund verwendet
- Bronchiektasen = irreversible Schädigung der großen Atemwege aufgrund narbigen Umbaus
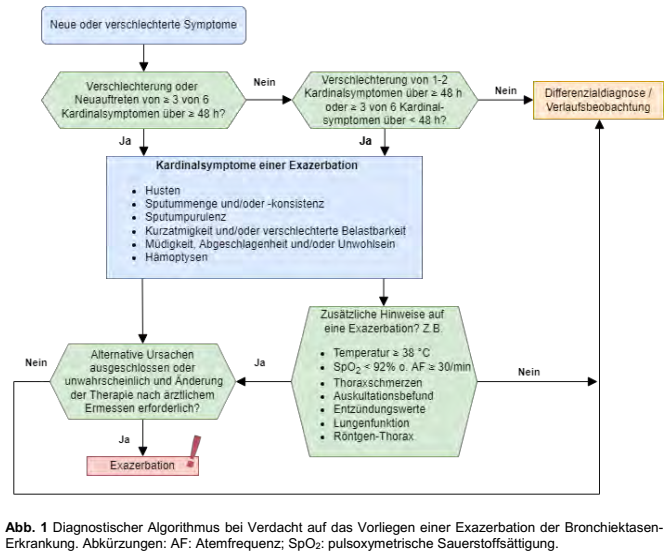
- Exazerbation = Verschlechterung von min. 3 der folgenden 6 Kardinalsymptome über min. 48 h nach Ausschluss alternativer Ursachen mit nachfolgenden Symptomen
- neuer oder vermehrter Husten
- Zunahme von Sputummenge und/oder -konsistenz
- Neuauftreten oder Zunahme der Sputumpurulenz
- neue oder vermehrte Kurzatmigkeit und/oder verschlechterte Belastbarkeit
- Müdigkeit, Abgeschlagenheit und/oder Unwohlsein (Malaise)
- neu aufgetretene oder vermehrte Hämoptysen
- chronische bakterielle Infektion = Infektion, bei der das gleiche Pathogen mithilfe mikrobiologischer Standardkulturmethoden zweimal oder häufiger aufeinanderfolgend im Abstand von min. 3 Monaten innerhalb eines Jahres in respiratorischem Material nachgewiesen wurde
- Nutzung des Begriffs „Bronchiektasen-Erkrankung“ für klinisch relevante Bronchiektasen zur klaren Abgrenzung gegenüber dem alleinigen radiologischen Befund von Bronchiektasen ohne assoziierte Symptome
Ätiologie
Bronchiektasen-Erkrankung ist ätiologisch äußerst heterogen
- 36 % = Idiopathisch
- 21 % = Postinfektiös, einschließlich posttuberkulös
- 15 % = COPD
- 11 % = Asthma
- 9 % = PCD bzw. Kartagener Syndrom
- 1 – 5 %
- allergische bronchopulmonale Aspergillose (ABPA)
- Alpha-1-Antitrypsinmangel
- Autoimmunerkrankungen, v.a. rheumatoide Arthritis, Kollagenosen und Vaskulitiden
- Chronisch entzündliche Darmerkrankung
- Gastroösophageale Refluxerkrankung
- Immundefekte, primär und sekundär (inkl. CVID)
- NTM-Lungenerkrankung (NTM: nichttuberkulöse Mykobakterien)
- Rezidivierende Aspiration
- <1 %
- Cystische Fibrose (CF) oder CFTR-assoziierte Erkrankung (bis dato nicht bekannt)
- ENaC-Kanalopathie
- Fremdkörperaspiration
- HIV-Infektion
- Marfan-Syndrom
- Mounier-Kuhn-Syndrom
- Swyer-James-Syndrom
- Yellow-Nail-Syndrom
- Young-Syndrom
Symptomatik bzw. Befunde
Symptomatik klinisch relevanter Bronchiektasen ist keinesfalls spezifisch, weist eine große interindividuelle Variabilität auf und überlappt sich mit anderen chronischen Atemwegs- und Lungenerkrankungen (i.d.R. min. 2 der ersten 3 Symptome vorliegend)
- Husten: täglicher produktiver Husten bis gelegentlicher trockener Husten während einer Woche
- Auswurf (Sputum): täglicher mukopurulenter oder purulenter Auswurf bis Auswurf nur bei Exazerbationen
- Exazerbationen: mehrere Exazerbationen im letzten Jahr bis keine Exazerbation im letzten Jahr, aber in der Vorgeschichte
- Hämoptysen: rezidivierende Hämoptysen im letzten Jahr bis keine Hämoptysen im letzten Jahr, aber in der Vorgeschichte (bei ca. 20 – 37 % der Betroffenen)
- Dyspnoe: Ruhedyspnoe bis geringe Belastungsdyspnoe oder wenig eingeschränkte körperliche Belastbarkeit
- Mikrobiologie: Nachweis von Pseudomonas aeruginosa in respiratorischem Material bis Nachweis pathogener Mikroorganismen in respiratorischem Material in der Vorgeschichte
- weitere Symptome: Chronische Fatigue-Symptomatik, Abgeschlagenheit und Müdigkeit (Malaise); Thoraxschmerzen; auffällige Auskultation; Chronische Rhinosinusitis mit Nasenpolypen; rezidivierende Pneumonien; eingeschränkte Lungenfunktion oder obstruktive Ventilationsstörung; „clubbing“ oder hypertrophe Osteoarthropathie; (Z.n.) Pneumotzhorax; respiratorische Insuffizienz
Anamnese
- aktuelle Situation der Patient*innen und im Vordergrund stehende Probleme, z.B. Exazerbationen mit oder ohne antibiotische Therapie in den letzten 12 Monaten (mit Datum und eingesetzten Präparaten), Krankenhausbehandlungen in den letzten 2 Jahren, notfallmäßige Arztbesuche, Behandlung auf ITS, Husten, geschätzte Auswurfmenge & -farbe, Hämoptysen mit Menge und Häufigkeit, Thoraxschmerzen, Pneumothorax
- objektivierte Einschränkungen der körperlichen Belastbarkeit anhand einer Dyspnoeskala, z.B. Medical Research Council Dyspnea scale (MRCD)
- (Verlauf seit) Einsetzen der Beschwerden
- Besonderheiten bei Geburt (soweit bekannt) sowie in Kindheit und Adoleszenz
- Symptomatik an den oberen Atemwegen, rezidivierende Cephalgie
- Sozialanamnese (inkl. Berufs- & Rentenanamnese, Arbeitsunfähigkeit, Schwerbehinderung)
- Familienanamnese (inkl. Blutsverwandschaft der Eltern, weitere betroffene Familienmitglieder)
- frühere Tuberkulose/Mykobakteriose (ggf. Exposition im Haushalt)
- Impfungen
- Allergien und Unverträglichkeiten
- Rauchen, Alkohol und sonstige Genuss-/Suchtmittel
- bisherige Therapien, vorhandene Vernebler und Hilfsmittel
- regelmäßiger Sport / Training, frühere Rehabilitationsbehandlung und ggf. Gründe für ausbleibende Rehabilitation
Diagnostik
- mikrobiologische Diagnostik von Atemwegsmaterial (primär Sputum; Entnahme vor Antibiotikatherapie, soll diese aber nicht verzögern) bzgl. möglicher Pathogene
- thorakale Bildgebung mittels CT zur Bestätigung der Diagnose und weiteren differentialdiagnostischen Abklärung bei klinischem Verdacht
- Diagnosestellung mittels CT bei folgenden Punkten (min. 1 Kriterium erfüllt)
- bronchoarterielle Ratio ≥ 1 UND/ODER
- fehlende Verjüngung des Bronchus nach peripher UND/ODER
- Sichtbarkeit eines Bronchus mit Abstand ≤ 1 cm von der viszeralen Pleura
- Diagnosestellung einer Bronchiektasen-Erkrankung soll sowohl klinische als auch radiologische Kriterien beinhalten
- Identifikation behandelbarer (Teil-)Ursachen („treatable traits“) einer Bronchiektasen-Erkrankung ist von wesentlicher Bedeutung hinsichtlich des klinischen Managements
- Diagnosestellung einer Exazerbation der Bronchiektasen-Erkrankung erfolgt nach Ausschluss entsprechender Differentialdiagnosen anhand klinischer Kriterien
- unauffällige Biomarker und/oder apparative Untersuchungsbefunde bei Patient*innen, die die klinischen Kriterien erfüllen, schließen Exazerbation nicht aus und sollen nicht zum Verwerfen der Diagnose führen
- Schweregrad einer Exazerbation anhand klinischer Einschätzung
- leichte Exazerbation: ambulante Therapie und kein Antibiotikum
- moderate Exazerbation: ambulante Therapie und orales Antibiotikum
- schwere Exazerbation: stationäre und/oder parenterale antibiotische Therapie
- CT-Angiografie des Thorax bei klinisch signifikanten Hämoptysen zur Lokalisation und Bestimmung der Ätiologie der Blutung
Therapie
- Standardtherapie der Exazerbation einer Bronchiektasen-Erkrankung ist die antibiotische-empirische Therapie nach Diagnosestellung
- antibiotische Therapie der Exazerbation bei Nachweis von Pseudomonas aeruginosa oder bekannter chronischer Infektion über min. 14 Tage (bei anderen Erregern ggf. kürzer)
- NIV nur bei ausgewählten Patient*innen mit Bronchiektasen-Erkrankung und akuter ventilatorischer Insuffizienz im Rahmen einer Exazerbation (Vorgehen gemäß den jeweiligen nationalen Leitlinien und nach sorgfältiger Bewertung der auslösenden Faktoren)
- CAVE: endotracheale Intubation mit invasiver mechanischer Beatmung ist bei akuter ventilatorischer Insuffizienz im Rahmen einer Exazerbation mit einer erhöhten Morbidität und Mortalität vergesellschaftet
- Verlegung in Zentrum mit Möglichkeit zur Bronchialarterienembolisation und Thoraxchirurgie bei refraktären und/oder massiven Hämoptysen/Hämoptoe
Therapie von Hämoptysen/Hämoptoe
Hämoptysen mit einer Blutmenge 240 ml/Tag oder > 100 ml/Tag über mehrere Tage werden als Hämoptoe bezeichnet (Mortalität bei > 50%)
| Schweregrad | Definition | Maßnahmen |
|---|---|---|
| leicht | Blutspuren | irritierende Inhalationen (hypertone Kochsalzlösung) pausieren und ggf. – Tranexamsäure 3 x 500-1000 mg p.o. – Inhalation mit Tranexamsäure 3 x 500 mg/5 mL + 5 mL Aqua ad inj. (CAVE: Off-Label-Use, strenge Risiko-Nutzen-Abwägung, Bronchospasmus bzw. Blutdrucksteigerung und/oder verstärkte Blutung sind möglich, weshalb bei Erstanwendung eine vorsichtige Dosistitration ratsam ist.) – Inhalation mit Epinephrin (4 mg/mL) 7-14 Hub (ca. 1-2 mL) in 2,5-5 mL NaCl 0,9% (CAVE: Off-Label-Use, strenge Risiko-Nutzen-Abwägung, Bronchospasmus bzw. Blutdrucksteigerung und/oder verstärkte Blutung sind möglich, weshalb bei Erstanwendung eine vorsichtige Dosistitration ratsam ist.) |
| mittel | jedes Erstereignis; > 100 mL/d, persistierend über 3 Tage | stationäre Überwachung + Diagnostik (CT-Angiografie, ggf. Bronchoskopie) + Maßnahmen wie bei leichter Blutung |
| schwer | > 200 mL/d; Bewusstseinsstörung; kompromittierte Hämodynamik | stationäre Verlegung in ein Zentrum; Indikation für Bronchialarterienembolisation prüfen – ggf. Bronchoskopie auf Intensivstation – ggf. Thoraxchirurgie |
palliativmedizinische Aspekte
- Bronchiektasen-Erkrankung hat oftmals einen überJahre oder Jahrzehnte bestehenden und langsam progredienten chronischen Verlauf
- Therapieziel ist oftmals auch „nur“ die Linderung der Symptomlast und nicht die Behebung der Ursache, ohne das Vorliegen einer palliativen Lebenssituation im engeren Sinne
- palliative Lebenssituationen treten v.a. im Rahmen einer rasch progredienten Verschlechterung, schweren Exazerbation oder einer kritischen Dekompensation instabiler Komorbiditäten auf
- Symptomatik im Rahmen einer endgradigen/palliativen Bronchiektasen-Erkrankung
- Atemnot durch Abnahme der Husteneffizienz und Zunahme der bronchialen Sekretretention
- quälender Husten
- atem- und hustenabhängige Thoraxschmerzen durch entzündliche pleurale Affektionen
- thorakales Engegefühl durch pulmonale Überblähung
- Verschlechterung vorbestehenden Fatigue-Symptomatik, Angst/Panik & ggf. Depression
- Therapie der Atemnot bei Hypoxämie (pO2 < 55 mmHg): O2-Gabe, vorsichtig titrierte Opiat-Gabe sowie in Einzelfällen High-flow-Sauerstofftherapie oder NIV (CAVE: antitussive Wirkung der Opiate kann Suppression des Hustenstoßes mit konsekutiver Zunahme des Sekretverhaltes und dadurch zu einer Verschlechterung der Atemnot bewirken)


Sei der Erste der einen Kommentar abgibt