veröffentlichende Fachgesellschaft: Deutsche Sepsis-Gesellschaft (DSG)
Klassifikation gemäß AWMF: S3
Datum der Veröffentlichung: 30.04.2025
Ablaufdatum: 29.04.2030
Quelle/Quelllink: https://www.awmf.org/leitlinien/detail/ll/079-001.html
Grundsätzliches
- Definition „Sepsis“: Sepsis ist eine akut lebensbedrohliche Organdysfunktion, hervorgerufen durch eine inadäquate Wirtsantwort auf eine Infektion (für die Diagnose einer Sepsis-assoziierten Organdysfunktion ist ein Anstieg des Sequential Organ Failure Assessment (SOFA) Score um ≥ 2 Punkte zu verwenden)
- Definition „septischer Schock“: eine trotz adäquater Volumentherapie persistierende arterielle Hypotension mit der Notwendigkeit einer Therapie mit Vasopressoren, um einen mittleren arteriellen Blutdruck von ≥ 65 mmHg zu erreichen, sowie ein gleichzeitig bestehender Laktatwert im Blut von > 2 mmol/L
Screening und Erstmaßnahmen
- Krankenhäusern sollen ein Qualitätssicherungsprogramm zum Thema Sepsis, inkl. eines Sepsis-Screenings für akut erkrankte Hochrisikopatient*innen und Standardarbeitsanweisungen (SOPs) für die Behandlung, durchführen
- bei Patient*innen außerhalb der Intensivstation, bei denen der Verdacht auf eine Infektion besteht, soll regelmäßig ein geeignetes Screeninginstrument angewendet werden, um eine Sepsis frühzeitig zu erkennen (für häufig verwendete Sepsis-Screening-Tools siehe Bild)
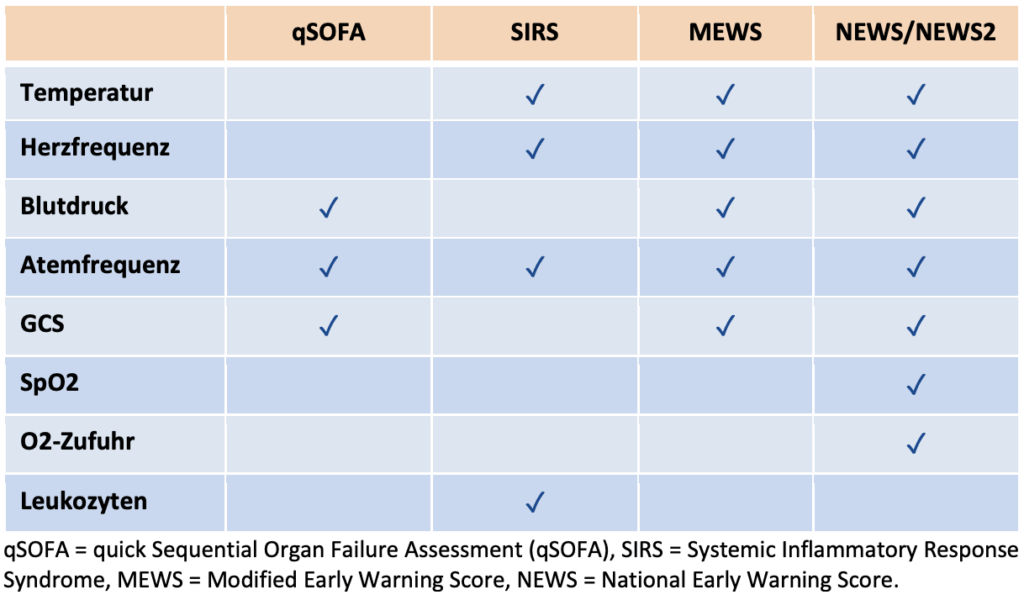
- Messung des Laktats im Blut bei Erwachsenen mit Verdacht auf Sepsis
- Sepsis und septischer Schock sind medizinische Notfälle, daher wird empfohlen, dass mit der Behandlung und der hämodynamischen Stabilisierung unverzüglich begonnen wird
- bei Patient*innen mit Sepsis-induzierter Hypoperfusion oder septischem Schock innerhalb der ersten 3 h als Richtwert 30 mL/kg intravenöse kristalloide Lösung verabreichen
- bei Patient*innen mit septischem Schock, die Vasopressoren benötigen, für den mittleren arteriellen Druck (MAP) einen anfänglichen Zielwert in Höhe von 65 mmHg wählen (im Vergleich zu höheren Werten)
- bei Patient*innen mit Sepsis oder septischem Schock, Vasopressoren auch periphervenös applizieren, um den MAP auf ≥ 65 mmHg anzuheben und dabei nicht auf die Anlage eines ZVK warten
- bei Patient*innen mit Sepsis oder septischem Schock, Flüssigkeitsgaben nach dem initialen Bolus durch wiederholte Kontrollen des hämodynamischen Status begleiten und nur fortsetzen, wenn weiterhin Zeichen einer Hypoperfusion vorliegen
- bei Patient*innen mit Sepsis oder septischem Schock, die Flüssigkeitstherapie mit dem Ziel steuern, eine erhöhte Laktatkonzentration im Blut zu senken
- bei Patient*innen mit septischem Schock die Rekapillarisierungszeit zur Beurteilung der Gewebeperfusion nutzen
- bei Patient*innen mit Sepsis oder septischem Schock, bevorzugt dynamische ggü. statischen Variablen verwenden, um die Flüssigkeitstherapie zu steuern
- bei Patient*innen mit Sepsis oder septischem Schock eine Echokardiographie zur Beurteilung der Herzfunktion und des Volumenstatus durchführen
Infektion und antimikrobielle Therapie
- bei Patient*innen mit Sepsis oder septischem Schock vor Beginn der Antibiotikatherapie mindestens 2 Blutkultur-Sets entnehmen (CAVE: gilt auch für Patienten, die bereits eine antibiotische Vorbehandlung erhalten haben)
- Gewinnung von weiteren Probenmaterialien von möglichen Infektionsfoci, z.B. Abstrich, Punktat, Biopsie etc. (CAVE: keine wesentliche zeitliche Verzögerung der antiinfektiven Therapie)
- Verabreichung von intravenösen Antiinfektiva bei Patient*innen mit Sepsis so schnell wie möglich, bei Patient*innen mit septischem Schock idealerweise innerhalb einer Stunde
- bei Verdacht auf Sepsis ohne Schocksymptomatik zunächst zeitnahe weitere Diagnostik durchführen –> falls der Verdacht auf zugrundeliegende Infektion weiter besteht, Verabreichung der antiinfektiven Therapie innerhalb von 3 h
- bei Patient*innen mit Sepsis oder septischem Schock initiale antiinfektive Therapie mit einem Antibiotikum oder mehreren Antibiotika durchführen, um alle wesentlichen Bakterien zu erfassen (antiinfektive Therapie nach dem vermuteten Infektionsfokus, MRE-Besiedlung und Anamnese ausrichten)
- bei Patient*innen mit Sepsis oder septischem Schock ohne erhöhtes Risiko für multiresistente Erreger KEINE routinemäßige, initiale Therapie mit zwei verschiedenen gegen gramnegative Erreger wirksamen Substanzen („double gramnegative coverage“) durchführen
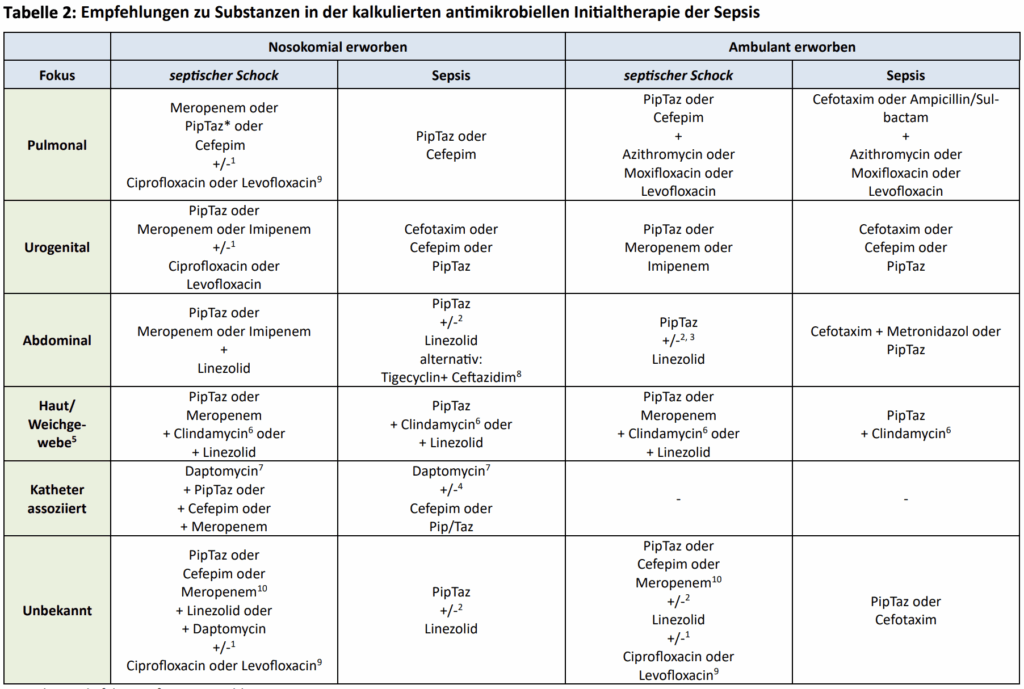
- bei Patient*innen mit Sepsis oder septischem Schock mit niedrigem Risiko für eine Pilzinfektion KEINE antimykotische Therapie durchführen
- bei Patient*innen mit Sepsis oder septischem Schock mit hohem Risiko für eine Pilzinfektion eine empirische antimykotische Therapie durchführen
- Risikofaktoren für Candida-Sepsis
- Candida-Besiedlung an mehreren Stellen, Surrogatmarker wie der Serum-BetaD-Glucan-Assay, Neutropenie, Immunsuppression, Schwere der Erkrankung (hoher APACHE-Score), längere Verweildauer auf der Intensivstation, zentrale Venenkatheter und andere intravaskuläre devices, Drogenabusus (Injektion), vollständige parenterale Ernährung, Breitbandantibiotika, Perforationen des Gastrointestinaltrakts und Anastomosenlecks, gastrointestinale oder hepatobiliäre Notoperationen, akutes Nierenversagen und Hämodialyse, schwere thermische Verletzungen, vorausgegangene Operationen
- Risikofaktor für invasive Schimmelpilzinfektionen
- Neutropenie, Surrogatmarker wie Serum oder Bronchoalveoläre Lavage Galactomannan
Assay, hämatopoetische Stammzelltransplantation, Organtransplantation, hochdosierte Kortikosteroidtherapie, Immun-Modifier, Influenza, COVID-19, moderate bis schwere HIV Infektion mit CD4-Zellen < 200/µL, solide Tumoren
- Neutropenie, Surrogatmarker wie Serum oder Bronchoalveoläre Lavage Galactomannan
- bei Patient*innen mit Sepsis oder septischem Schock Beta-Laktam-Antibiotika als prolongierte oder kontinuierliche Infusion (nach initialem Bolus) verabreichen (bei kontinuierlicher Infusion ist auf physikalisch-chemische Stabilität des Wirkstoffs zu achten)
- bei Patient*innen mit Sepsis oder septischem Schock antiinfektive Therapie täglich evaluieren und die Therapie anpassen, sobald ein plausibler Erregernachweis geführt werden konnte, und die Antiinfektiva-Empfindlichkeit bekannt ist
Kreislauftherapie
- bei Patient*innen mit Sepsis oder septischem Schock sind balancierte Kristalloide die Flüssigkeitstherapie der ersten Wahl
- bei Patient*innen mit Sepsis oder septischem Schock Albumin additiv zu balancierten Kristalloiden verabreichen, wenn große Mengen an Flüssigkeit benötigt werden, um eine hämodynamische Stabilität zu erreichen
- bei Patient*innen mit Sepsis oder septischem Schock Hydroxyethylstärke NICHT zur Flüssigkeitstherapie anwenden
- bei Patient*innen mit Sepsis und septischem Schock Gelatine NICHT anwenden
- bei Patient*innen mit Sepsis oder septischem Schock ist Noradrenalin der Vasopressor der ersten Wahl
- bei Patient*innen mit septischem Schock Vasopressin ergänzend, wenn mit Noradrenalin alleine kein ausreichender Blutdruck erzielt werden kann
- aufgrund aktueller Datenlage keine Empfehlung für noch gegen den Einsatz von Methylenblau bei Patient*innen mit septischem Schock
- bei Patient*innen mit septischem Schock Terlipressin NICHT anwenden
- bei Patient*innen mit Sepsis oder septischem Schock, bei denen Hinweise für eine kardiale Dysfunktion mit persistierender Hypoperfusion trotz angemessenem Flüssigkeitsstatus und arteriellem Blutdruck bestehen, Dobutamin verwenden
- bei Patient*innen mit septischem Schock Levosimendan NICHT einsetzen
- Einsatz einer veno-arteriellen ECMO bei Patient*innen mit therapierefraktären septischem Schock ohne zusätzlichen kardiogenen Schock kann NICHT empfohlen werden
- aufgrund der aktuellen Datenlage keine Empfehlung für noch gegen den Einsatz einer veno-arteriellen ECMO bei Patient*innen mit therapierefraktärem septischen und zusätzlichen kardiogenen Schock
- bei Patient*innen mit septischem Schock β-Blocker zur Herzfrequenzsenkung NICHT routinemäßig anwenden
Beatmungstherapie
- Patient*innen mit Sepsis oder septischem Schock und ARDS mit Tidalvolumen um 6 mL/kg IBW (4 – 8 mL/kg IBW) beatmen
- Patient*innen mit Sepsis oder septischem Schock ohne ARDS mit einem mit VT von 6 – 8 mL/kg IBW beatmen
- bei invasiver Beatmung von Patient*innen mit Sepsis oder septischem Schock und akuter respiratorischer Insuffizienz Plateaudruck (Pplat) ≤ 30 cmH2O halten
- bei invasiver Beatmung von Patient*innen mit Sepsis oder septischem Schock und ARDS inspiratorische Druckdifferenz von ≤ 14 cmH2O anzustreben
- bei Patient*innen mit Sepsis oder septischem Schock und mildem ARDS orientierende Einstellung des PEEP mithilfe der FiO2/niedrig-PEEP-Tabelle des ARDS-Netzwerks erwägen
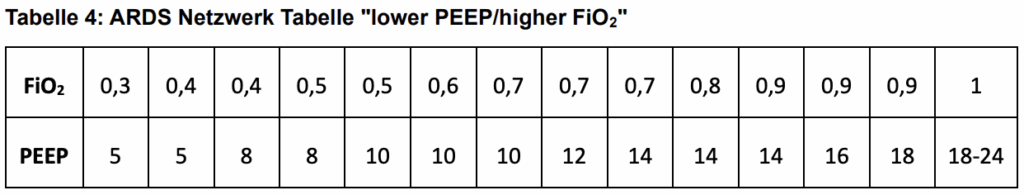
- bei Patient*innen mit Sepsis oder septischem Schock und moderatem oder schwerem ARDS Anwendung eines höheren PEEP
- bei invasiv beatmeten Patient*innen mit Sepsis oder septischem Schock eine SaO2 bzw. SpO2 von 92 – 96 % bzw. eine paO2 zwischen 70 – 90 mmHg (9,3 – 12 kPa) anstreben
- bei Patient*innen mit Sepsis oder septischem Schock frühzeitig (innerhalb der ersten 48 h nach Intubation) unterstützende Beatmung zur Ermöglichung von Spontanatmung unabhängig von Ursache und Art der zugrundeliegenden respiratorischen Insuffizienz einsetzen
- bei Patient*innen mit Sepsis oder septischem Schock und milder bis moderater akuter hypoxämischer respiratorischer Insuffizienz (PaO2/FiO2 100 – 300) primär nichtinvasive Atmungsunterstützung (NIV, CPAP oder HFNO) anwenden
- Einsatz einer veno-venösen ECMO bei Patient*innen mit Sepsis oder septischem Schock und schwerem ARDS nur nach Ausschöpfen der konservativen Therapiemaßnahmen, einschließlich der Durchführung einer Bauchlagerung und fortbestehender schwerer Gasaustauschstörung erwägen
Nierenersatztherapie
- extrakorporale Nierenersatzverfahren auf Intensivstationen ausschließlich durch Fachärzt*innen mit der Zusatzbezeichnung „Intensivmedizin“ und/oder Nephrolog*innen indizieren und durchführen
- Start der Nierenersatztherapie bei AKI in der Intensivmedizin – absolute Indikationen
- Hyperkaliämie (> 6.0 mmol/L)
- Azidose (pH < 7,2)
- Volumenüberladung (Ödeme, pulmonalvenöse Stauung)
- Urämie (Klinik, u. a. Bewusstseinsstörungen)
- bei Patient*innen mit Sepsis oder septischem Schock und lebensbedrohlichen Veränderungen des Flüssigkeits-, Säure-Basen- oder Elektrolythaushaltes unverzüglich mit Nierenersatztherapie beginnen
- bei Patient*innen mit Sepsis oder septischem Schock ein Nierenersatzverfahren ohne weiteres Zuwarten beginnen, wenn aufgrund der klinischen Situation, des Krankheitsverlaufes und/oder der Vorerkrankungen eine Nierenersatztherapie bei AKI zu erwarten ist
- bei nicht-lebensbedrohlichen Veränderungen und Unklarheit, ob eine Nierenersatztherapie zu erwarten ist, konservative Maßnahmen zur Vermeidung eines Nierenersatzverfahrens unter regelmäßiger Reevaluation durchführen
- bei Patient*innen mit Sepsis und Indikation zur Nierenersatztherapie diffusive Nierenersatzverfahren oder konvektive Verfahren bzw. Kombination aus diffusiven und konvektiven Verfahren gleichwertig einsetzen
- zur Nierensatztherapie der AKI bei Patient*innen mit Sepsis kontinuierliche oder intermittierende Verfahren gleichwertig einsetzen (CAVE: bei der Auswahl des Verfahrens jedoch die individuelle klinische Situation der Patient*innen berücksichtigen, die zu einer Bevorzugung eines kontinuierlichen oder intermittierenden Verfahrens führen kann)
- bei hämodynamisch instabilen Patient*innen mit Sepsis und Nierenersatztherapie bei AKI ein kontinuierliches oder verlängert intermittierendes Verfahren einsetzen
- bei Patient*innen mit Sepsis oder septischem Schock eine regionale Citrat-Antikoagulation oder eine systemische Heparin-Antikoagulation des extrakorporalen Blutkreislaufs gleichwertig einsetzen
- bei Patient*innen mit Sepsis oder septischem Schock für ein kontinuierliches Nierenersatzverfahren eine mittlere Dosis von 20 – 25 mL/kg/h über die geplante Behandlungsdauer verabreichen
- bei Patient*innen mit Sepsis oder septischem Schock keine kontinuierliche hochvolumige (high-volume) Hämofiltration anwenden
weitere Maßnahmen
- Hydrokortison mit oder ohne Fludrokortison bei Patient*innen mit septischem Schock mit anhaltendem Vasopressorbedarf trotz ausreichender Volumengabe einsetzen (empfohlene Dosierung für Hydrokortison beträgt 200 mg/d i.v., für Fludrokortison 1 x 50 µg/d enteral; als „anhaltender Vasopressorbedarf“ wird die Gabe von Noradrenalin ≥ 0,25 µg∙kg-1min-1 über mindestens 4 h bezeichnet)
- bei Patient*innen mit Sepsis oder septischem Schock Indikationstellung zur Gabe von Erythrozytenkonzentraten bei Hb-Wert von < 4,34 mmol/L (< 7.0 g/dl) oder beim Vorliegen physiologischer Transfusionskriterien
- bei Patient*innen mit Sepsis oder septischem Schock therapeutisches Plasma NICHT zur Behandlung eines Volumenmangels, sondern ausschließlich entsprechend den Indikationen der „Querschnitts-Leitlinien zur Therapie mit Blut-komponenten und Plasmaderivaten“ der BÄK einsetzen
- bei Patient*innen mit Sepsis oder septischem Schock KEINE Thrombozytentransfusion durchführen, es sei denn, es liegt eine relevante Blutung oder eine schwere Thrombozytopenie vor (< 10.000/µL)
- bei Patient*innen mit Sepsis oder septischem Schock keine intravenösen Immunglobuline anwenden
- bei Patient*innen mit Sepsis oder septischem Schock KEINE unselektiven Adsorptionsverfahren einsetzen
- keine Empfehlung für noch gegen den Einsatz einer Polymyxin-B-Hämoperfusion bei Patient*innen mit Sepsis oder septischem Schock
- keine Empfehlung für noch gegen den Einsatz einer Plasmapherese bei Patient*innen mit Sepsis oder septischem Schock
- bei Patient*innen mit Sepsis oder septischem Schock pharmakologische Prophylaxe einer venösen Thromboembolie (VTE) mittels niedermolekularen Heparins (NMH) durchführen
- bei hochgradig eingeschränkter Nierenfunktion und/oder septischem Schock mit hohem Vasopressorbedarf entweder niedermolekulares Heparin (NMH) unter engmaschigen anti-Xa Kontrollen oder unfraktioniertes Heparin (UFH) einsetzen
- bei Patient*innen mit Sepsis oder septischem Schock bezüglich der Analgesie und Sedierung den Empfehlungen der DAS-Leitlinie folgen
- bei Patient*innen mit Sepsis oder septischem Schock Beginn einer Insulintherapie bei einem oberen Blutzuckerspiegel von ≥ 180 mg/dL (≥ 10 mmol/L)
- bei Patient*innen mit septischem Schock KEIN Natriumbicarbonat alleinig zum Zwecke einer Verbesserung der Hämodynamik verwenden


Sei der Erste der einen Kommentar abgibt