veröffentlichende Fachgesellschaft: Italian Society of Cardiology (SIC) & Italian Society of Medical and Interventional Radiology (SIRM)
Klassifikation gemäß AWMF:
Datum der Veröffentlichung: 23.09.2025
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.1007/s11547-025-02076-x
Grundsätzliches
- Definition „akuter Brustschmerz“: nicht-traumatische Brustschmerzen, die neu auftreten oder sich akut in ihrem Beginn, ihrer Intensität oder Dauer verändern
- Begriff „akuter Brustschmerz“ umfasst breites Spektrum an thorakalen Symptomen, darunter echte präkordiale Schmerzen oder Empfindungen wie Druck, Engegefühl, Schweregefühl, Quetschgefühl oder Brennen
- Schmerz auch außerhalb des Thoraxbereiches auftreten und in andere Körperregionen wie Schulter, Arm, Hals, Oberbauch oder Kiefer ausstrahlen
- akuter Brustschmerz macht etwa 8 – 10 % der jährlichen Notaufnahme-Patient*innen > 18 Jahren aus (etwa 5 % davon haben ACS)
Anamnese & Diagnostik
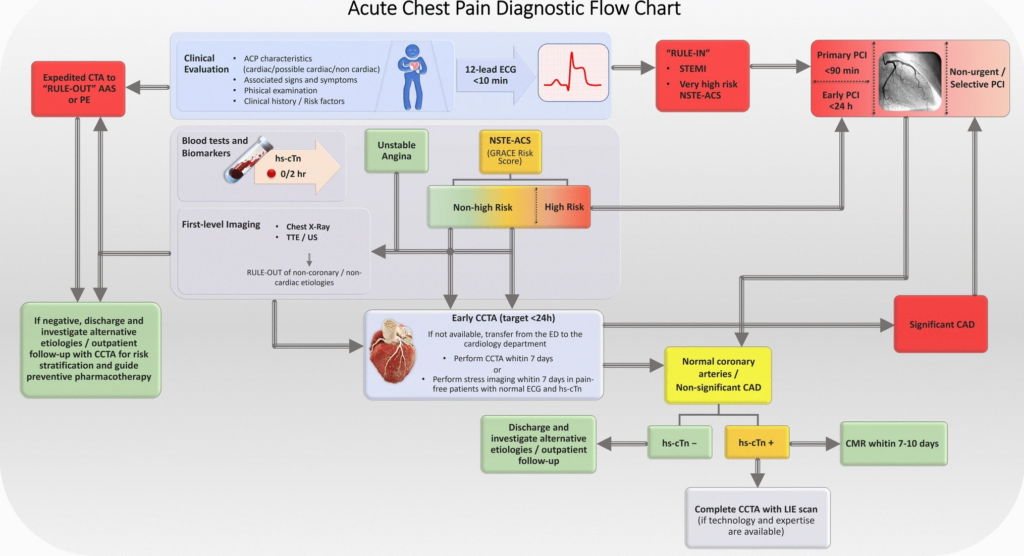
- erste klinische Beurteilung zielt auf die schnelle Erkennung und Behandlung potenziell lebensbedrohlicher Zustände wie ACS, Aortendissektion, Lungenembolie und infarktähnliche Myokarditis ab
- mögliche Begleitsymptome sind Atemnot, Übelkeit, Erbrechen, Schwitzen, Müdigkeit oder Bewusstseinsstörungen, die mitunter das Hauptsymptom darstellen können
- CAVE: hyperakute, flüchtige, atemabhängige (pleuritische) oder lageabhängige sowie punktuell lokalisierte Symptome wahrscheinlich nicht auf eine Myokardischämie zurückzuführen
- klinische Untersuchung sollte detaillierte Beschreibung der Brustschmerzen und der Begleitsymptome umfassen, inkl. Beginn, Dauer, Lokalisation, Ausstrahlung sowie lindernder oder verschlimmernder Faktoren
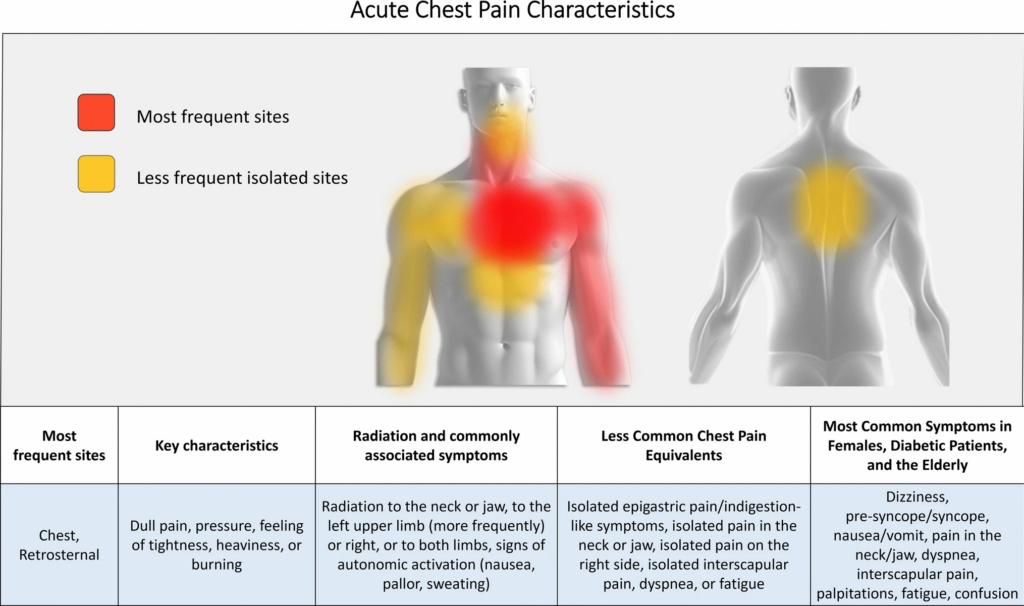
- klinische Beurteilung sollte darauf abzielen, Anzeichen zu identifizieren, die mit einem hohen Morbiditäts- und Mortalitätsrisiko verbunden sind, z.B.
- Anzeichen einer verminderten Herzleistung (z. B. Tachykardie, Hypotonie, kalte Extremitäten, geringe Urinausscheidung, veränderter Bewusstseinszustand)
- Anzeichen einer Herzinsuffizienz (z. B. Lungenödem, erhöhter Jugularvenendruck, periphere Ödeme)
- neu aufgetretenes systolisches Herzgeräusch, das auf akute Mitralklappeninsuffizienz oder Ventrikelseptumdefekt hindeutet
- Anzeichen, die auf alternative Ursachen für ACS hindeuten
- Fieber (Endokarditis oder Lungenentzündung)
- Blutdruckdifferenz zwischen Pulsen (Aortendissektion)
- Lungenanomalien, die bei Auskultation oder im Thorax-Röntgenfestgestellt wurden (Lungenentzündung oder Pneumothorax)
- Perikardreiben (Perikarditis)
- andere Herzgeräusche (z. B. Aortenstenose, Endokarditis)
- Troponin
- hochsensitives kardiales Troponin T (hs-cTnT) und hochsensitives kardiales Troponin I (hs-cTnI) sind die bevorzugten Serum-Biomarker zur Beurteilung bei V.a. ACS
- Troponinkonzentrationen als ganze Zahlen in Nanogramm pro Liter (ng/L) angeben
- geschlechtsspezifische Grenzwerte des 99. Perzentils empfohlen, um diagnostische Sensitivität bei Frauen und Spezifität bei Männern zu erhöhen
- serielle Messungen mittels 0h/1h- oder 0h/2h-Algorithmen für zeitnahen Nachweis bzw. Ausschluss eines ACS empfohlen
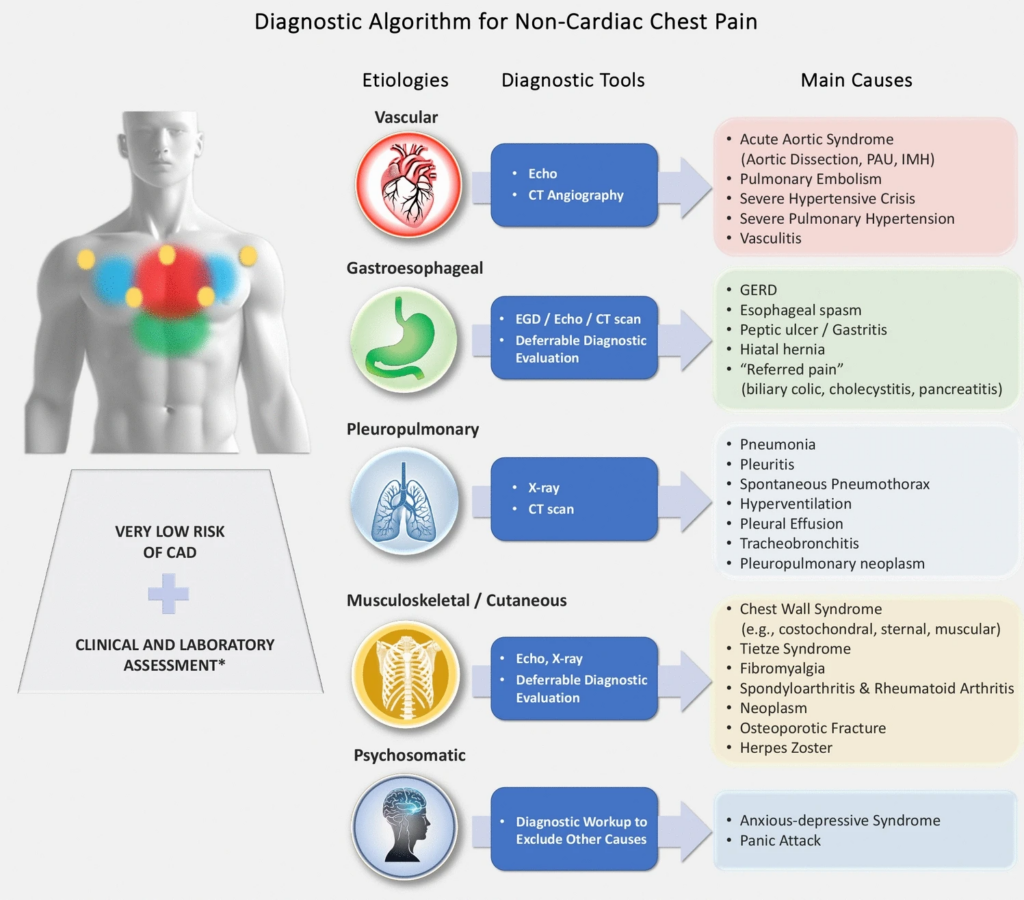
- Bildgebung
- sowohl Thorax-Röntgen als auch Echokardiographie sind kostengünstige und weit verbreitete bildgebende Verfahren der 1. Wahl, v.a. bei Patient*innen mit akuter zerebraler Peritonitis
- Koronar-CT-Angiographie (CCTA) ist klinischer Goldstandard für Ausschluss einer obstruktiven KHK
Elektrokardiogramm (EKG)
- Eckpfeiler der Erstbeurteilung und Behandlung von Patienten mit akutem Koronarsyndrom (ACS)
- EKGs können in drei Kategorien eingeteilt werden
- STEMI oder STEMI-Äquivalent
- ischämische ST-Strecken- oder T-Wellen-Anomalien
- nicht-ischämische Muster, zu denen normale EKGs, unspezifische Befunde, linksventrikuläre Hypertrophie (mit oder ohne ST-Streckenveränderungen), Links- oder Rechtsschenkelblock oder ventrikulärer Schrittmacherrhythmus gehören, die die Sgarbossa-Kriterien oder modifizierten Sgarbossa-Kriterien für akuten Myokardinfarkt nicht erfüllen
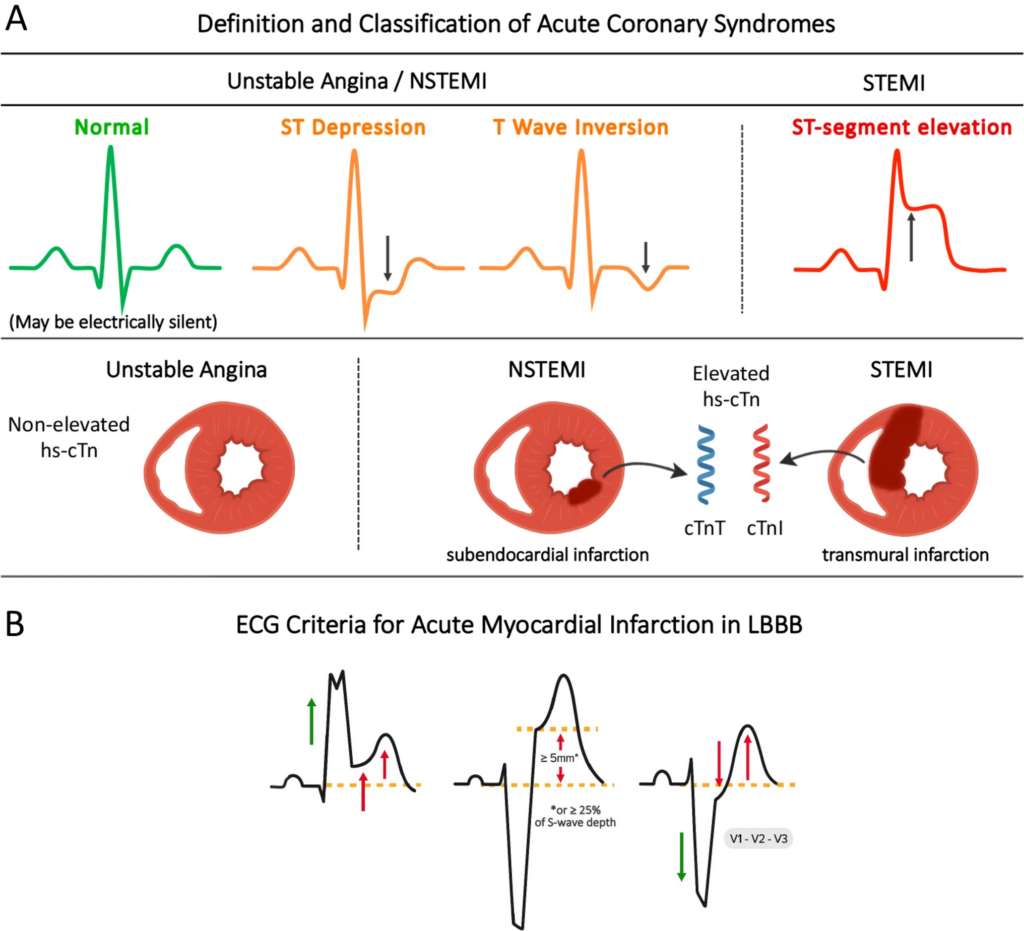
- instabiler Angina pectoris (UA) bzw. NSTEMI
- Diagnose basiert auf neu aufgetretenen, sich verschlimmernden Brustschmerzen in Ruhe oder bei geringer Belastung, ohne dass Biomarker für Myokardschädigung oder -nekrose erhöht sind
- EKG-Veränderungen erhöhen Wahrscheinlichkeit der Diagnose, allerdings können EKG-Veränderungen bei mehr als einem Drittel der NSTEMI-Patient*innen vollständig fehlen
- prognostische Aussagekraft von T-Wellen-Inversionen ist geringer als die von ST-Strecken-Senkungen (ST-Strecken-Senkungen dienen zudem als quantitativer prognostischer Risikomarker)
- bei STEMI ist die Summe der ST-Streckenhebungen über alle Ableitungen ein klinischer Marker für ischämisches Myokard und gefährdetes Myokard
Risikostratifizierung & -klassifizierung
- Kategorisierung bei V.a. ACS anhand initialem EKG und Biomarker
- Patient*innen mit akutem Brustschmerz (oder gleichwertigen Symptomen) und persistierender ST-Streckenhebung (oder gleichwertigen ST-Streckenhebungsmustern) im EKG –> STEMI
- Patient*innen mit akutem Brustschmerz (oder gleichwertigen Symptomen), aber ohne persistierende ST-Streckenhebung (oder gleichwertige ST-Streckenhebungsmuster) im EKG, mit erhöhten und/oder erniedrigten cTn-Werten (CAVE: mind. ein Wert> 99. Perzentil der oberen Referenzgrenze) –> NSTEMI
- Patient*innen mit akutem Brustschmerz ohne Anzeichen einer akuten Kardiomyozytenschädigung/Nekrose, begleitet von spezifischen klinischen Symptomen wie verlängerte Angina pectoris (> 20 min) in Ruhe, neu aufgetretene schwere Angina pectoris, zunehmende Häufigkeit oder Dauer der Angina pectoris oder Angina pectoris bei minimaler Anstrengung oder Angina pectoris nach kürzlich aufgetretenem AMI –> instabile AP
Risikokriterien für NSTEMI
- NSTEMI mit sehr hohem Risiko
- hämodynamische Instabilität oder kardiogener Schock
- wiederkehrende/anhaltende Brustschmerzen, die nicht auf medikamentöse Therapie ansprechen
- Herzstillstand nach Vorstellung oder lebensbedrohliche Herzrhythmusstörungen
- mechanische Komplikationen
- akutes Herzversagen aufgrund anhaltender Ischämie
- wiederkehrende dynamische EKG-Veränderungen, die auf eine Ischämie hindeuten, v.a. intermittierende ST-Streckenhebungen
- NSTEMI mit hohem Risiko
- NSTEMI durch empfohlene hs-cTn-Algorithmen bestätigt
- dynamische ST-Strecken- und T-Wellen-Veränderungen
- vorübergehende ST-Streckenhebung
- GRACE-Risikoscore > 140
organisatorische und logistische Aspekte
- Zusammenarbeit verschiedener Disziplinen, v.a. Kardiologie und Radiologie, ist unerlässlich
- gemeinsame Diagnosepfade, die in der klinischen Praxis umgesetzt werden sollen
- Verfügbarkeit moderner radiologischerBildgebung, v.a. CCTA, spielt Schlüsselrolle in der Behandlung der Untergruppe von Patient*innen, die sich mit akutem Aortensyndrom (AAS) in der Notaufnahme vorstellen
- alle Strategien werden durch die angemessene Ausbildung in kardiovaskulärer Bildgebung und durch verfügbare kontinuierliche Weiterbildungsinitiativen unterstützt
- Realisierung spezifischer ambulanter Behandlungspfade für erweiterte kardiale Bildgebung (verzögerte Nachuntersuchung mittels erweiterter kardialer Bildgebung nach Entlassung)


Sei der Erste der einen Kommentar abgibt