veröffentlichende Fachgesellschaft: Österreichische Gesellschaft für Nephrologie (ÖGN)
Klassifikation gemäß AWMF:
Datum der Veröffentlichung: 12.03.2026
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.1007/s00508-026-02708-w
Grundsätzliches
- Definition „Hyperkaliämie“ (angelehnt an Definition der Kidney Disease Improving Global Outcomes, KDIGO): Wert über dem oberen Referenzwert für die Kaliumkonzentration im Plasma oder Serum [S‑K+]
- entsprechende Referenzwert für [S‑K+] kann von Labor zu Labor variieren, wird aber oft mit 3,5 – 5,0 mmol/L angegeben (für Plasma-Kaliumkonzentration bei ca. 3,4 – 4,5 mmol/L)
- Prävalenz der Hyperkaliämie in breiter Allgemeinpopulation: 1,5 – 2,5 % ([S‑K+]-Grenze von ≥ 5,0 mmol/L)
- Prävalenz bei Notfallpatient*innen bei gleicher Definition: 3,6 %
- Medikamente mit einem erhöhten Risiko
| Klasse | Mechanismus | Beispiel |
|---|---|---|
| ACEi | Hemmung der AT-II und damit der Aldosteronproduktion | Lisinopril, Ramipril, Zilebesiran |
| ARB | Hemmung der AT-II-Wirkung und damit der Aldosteronproduktion | Candesartan, Valsartan, Telmisartan |
| Aldosteronsynthasehemmer | Hemmung der Aldosteronproduktion | Baxdrostat, Lorundrostat |
| Heparin, Antimykotika | Hemmung der Aldosteronproduktion | Ketokonazol, Fluconazol, Itraconazol |
| Steroidale und ns-MRA | Hemmung der Wirkung von Aldosteron am Mineralokortikoidrezeptors | Spironolacton, Eplerenon bzw. Finerenon |
| K‑sparende Diuretika | Hemmung des ENaC | Amilorid, Triamteren |
| Antibiotika | Hemmung des ENaC | Trimethoprim, Pentamidin |
| nichtselektive Betablocker | Hemmung der Reninfreisetzung und des K‑Shifts | Metoprolol, Atenolol |
| NSAR | Hemmung der Reninfreisetzung | Ibuprofen, Diclofenac |
| Calcineurininhibitoren | multiple Mechanismenstörung der tubulären K‑Sekretion | Cyclosporin A, Tacrolimus |
| Digitalisglykoside | Hemmung der NaKATPase – Störung der tubulären K‑Sekretion + K-Shift | Digoxin, Digitoxin |
| Kaliumsupplemente | Kaliumbelastung | KCl-Diätsalz, Konservierungsmittel |
- Risiko einer Hyperkaliämie in Abhängigkeit von unterschiedlichen Risikofaktoren
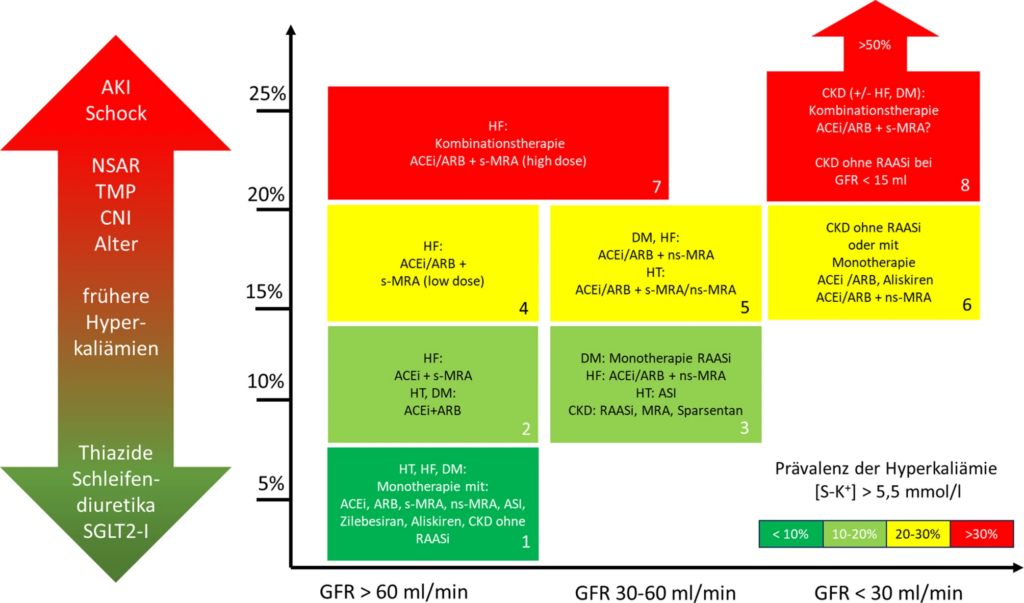
Klassifikation
- Einteilung basiert einerseits auf absoluter Höhe der [S‑K+] und andererseits auf Vorliegen von Hyperkaliämie-assoziierten EKG-Veränderungen als Ausdruck einer schweren Gesundheitsgefährdung
- CAVE: Einteilung unterliegt erheblichen Limitationen aufgrund der geringen Sensitivität der EKG-Veränderungen
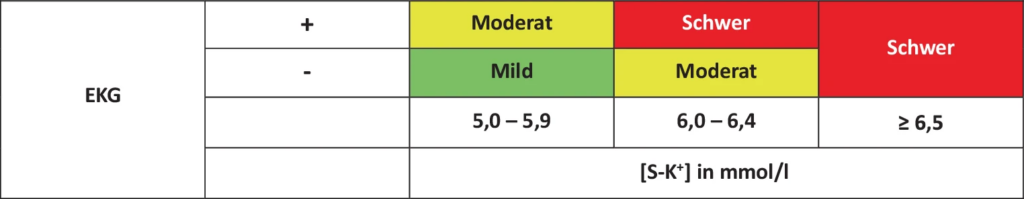
Symptomatik
- klinische Manifestationen einer Hyperkaliämie betreffen Herz- und Skelettmuskulatur
- CAVE: schwere Hyperkaliämie ist medizinischer Notfall aufgrund der Gefahr des Herztods durch Arrhythmien
- viele Patient*innen mit Hyperkaliämie erscheinen klinisch asymptomatisch oder weisen nur subtile Symptome auf, wie z.B. allgemeine Schwäche
- Hyperkaliämie kann zu schwerer, typischerweise aszendierender Muskelschwäche führen, die letztlich auf Stamm und obere Extremität übergreifen kann
- potenziell unmittelbar vital bedrohliche Auswirkungen einer Hyperkaliämie sind jene auf das Myokard
- Anstieg der [S‑K+] führt initial zu Beschleunigung der kardialen Reizleitung durch ein Anheben des kardialen Ruhemembranpotenzials (−90 mV → −80 mV, nähert sich an das Schwellenpotenzial –> verursacht leichter Tachykardien)
- Aktivierung von Kaliumkanälen –> Beschleunigung der kardialen Repolarisation –> Verkürzung des Aktionspotenzials
- i.d.R. hohe T‑Wellen mit schmaler Basis als EKG-Veränderungen in der Frühphase
- EKG ist unverlässlicher Parameter zur Detektion einer Hyperkaliämie, auch weil Schweregrad der Hyperkaliämie nicht mit den EKG-Veränderungen korreliert
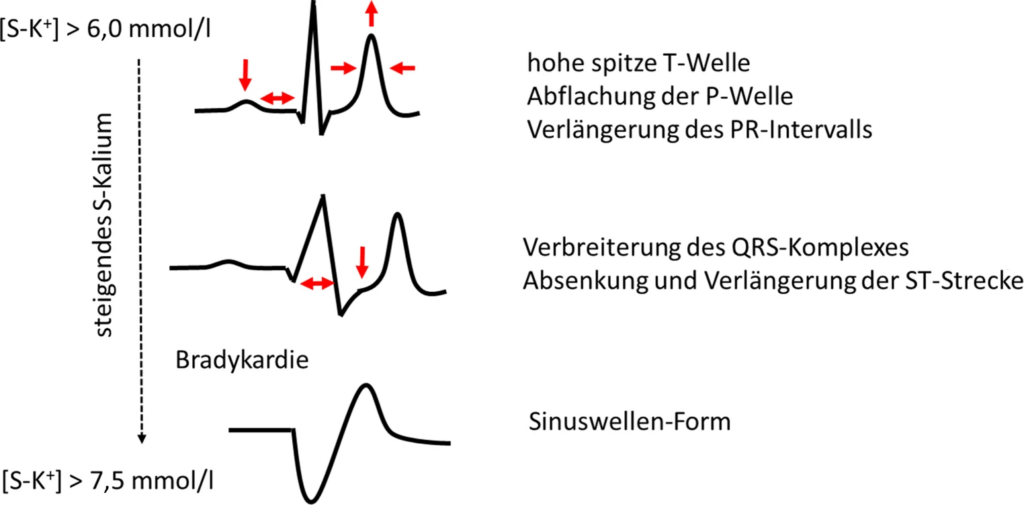
Diagnostik
- Messung der Kaliumkonzentration
- Blutabnahme sollte möglichst ohne Stauung –> danach rasche Probenverarbeitung
- wird Hyperkaliämie festgestellt –> zweite Bestimmung, am besten durch BGA bestätigt
- zur Kontrolle bei fraglich erhöhten Kaliumwerten kann die Analyse mittels Point-of-Care-Geräten eine wertvolle und rasche Hilfe darstellen
- erweiterte Labordiagnostik zur Abklärung der Ursachen einer Hyperkaliämie
- Erhebung von Anamnese (Risikofaktoren für Hyperkaliämie, Ernährung, Medikamente) und Klinik sowie erweiterte Labordiagnostik für Differenzialdiagnostik
- initial Bestimmung der Nierenfunktion (Serum-Kreatinin, eGFR) erforderlich
- liegt eGFR über 20 – 30 mL/min/1,73 m2, gewinnen andere bzw. zusätzliche Ursachen der Hyperkaliämie an Bedeutung – deshalb als Nächstes die renale Kaliumelimination beurteilen
- Goldstandard wäre die Messung der Kaliumausscheidung im 24-h-Harn (CAVE: Test eignet sich naturgemäß nur für die Abklärung einer chronischen Hyperkaliämie)
- Hyperkaliämie ist starker Stimulus für Aldosteron-Produktion: bereits bei [S‑K+] > 5,5 mmol/L ist Verdopplung der Plasma-Aldosteronkonzentration zu erwarten, steigt [S‑K+] weiter an, kommt es zu einer Erhöhung um das 5‑ bis 10-Fache (Referenzwerte für Aldosteron und Renin können zw. unterschiedlichen Laborinstituten schwanken)
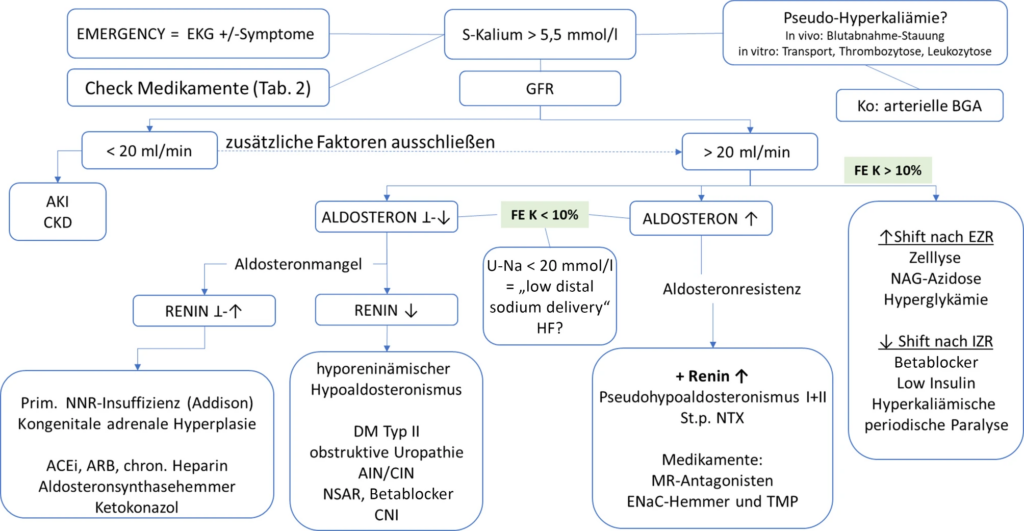
Differenzialdiagnose der Hyperkaliämie – Algorithmus
1. Besteht Notfallsituation (symptomatische Hyperkaliämie)?
2. Ausschluss einer Pseudohyperkaliämie
- Pseudohyperkaliämie: artifizielle Erhöhung der [S‑K+] ohne klinische Symptomatik oder EKG-Veränderungen
- häufigste Ursache ist Hämolyse bei Blutabnahme (langes Stauen, heftiges Pumpen mit der Hand, starke Sogwirkung bei Blutabnahme), welche von LDH-Erhöhung begleitet wird und im Labor durch Bestimmung des freien Hämoglobins nachgewiesen werden kann
- irrtümliche Verwendung von K+-EDTA-beschichteten Blutröhrchen oder Blutabnahme bei laufender Infusion einer kaliumhaltigen Lösung erhöht ebenfalls die Kaliumkonzentration
- auch tageszeitliche Schwankungen der [S‑K+] mgl. (nachts um ca. 0,3–0,4 mmol/l niedriger als am Tag, aber immer im Normbereich)
3. Wie ist die Nierenfunktion?
- eGFR < 20 – 30 mL/min/1,73 m2
- hochgradig reduzierte exkretorische Nierenfunktion (akut oder chronisch) kann Hyperkaliämie per se erklären (in vielen Fällen aber zusätzliche Faktoren relevant)
- in der Praxis deshalb auch bei diesen Patient*innen an andere Ursache für Hyperkaliämie denken, z. B. neu eingeleitete Therapie mit RAASi, kaliumreiche Kost, Kaliumshift, Zelllyse etc.
- eGFR > 20 – 30 mL/min/1,73 m2
- normale oder nicht hochgradig eingeschränkte Nierenfunktion sollte [S‑K+] stabil halten können
- für Differentialdiagnostik siehe Schritt 4
4. Wie ist die renale Kaliumelimination?
- FeK+ > 10 %
- renale Kaliumelimination ist adäquat, kann aber durch Shiftbewegungen zw. EZR & IZR [S‑K+] erhöht sein
- FeK+ < 10 %
- renale Kaliumelimination ist gestört –-> weiter mit Schritt 5
- vermehrter Ausstrom von Kalium aus der Zelle in den EZR
- Zellzerfall bei Tumorlysesyndrom oder Rhabdomyolyse können schwere Hyperkaliämien verursachen
- Diagnosen ergeben sich üblicherweise aus klinischem Kontext
- verminderte Aufnahme von Kalium in die Zelle
- Betablocker oder zu niedrige Insulinkonzentration hemmen postprandialen Kaliumtransport in die Zelle
- auch hyperkaliämische periodische Paralyse ist durch Störung des Natrium-vermittelten Kaliumtransports (SCN4A) in die Muskelzelle charakterisiert
- Hyperkaliämien sind getriggert durch Kälte, Hunger und Kaliumzufuhr bzw. nach körperlicher Anstrengung
5. Messung von Renin und Aldosteron (wenn keine RAASi eingenommen werden)
- Hypoaldosteronismus ist bei gering eingeschränkter Nierenfunktion die wichtigste Ursache für eine Hyperkaliämie mit verminderter renaler Kaliumelimination (CAVE: Unterscheidung zw. Aldosteronresistenz und Aldosteronmangel)
- beide Formen sind mit metaboler Azidose assoziiert und werden entsprechend auch als RTA Typ IV bezeichnet
- Aldosteronresistenz (Renin ↑, Aldosteron ↑)
- initial medikamentöse Ursachen ausschließen (z.B. MRA, kaliumsparende Diuretika, Trimethoprim), sonst an tubulointerstitielle Nierenerkrankungen denken
- viel seltener sind angeborene Loss-of-Function-Mutationen des ENaC oder MR (Pseudohypoaldosteronismus Typ Ia/Ib)
- wichtig ist der Ausschluss, dass geringer Anstrom von Na+ an das Sammelrohr die Kaliumsekretion hemmt ([Harn-Na+] < 20 mmol/L): Mechanismus kann bei Hypovolämie oder kardialer Dekompensation die Ursache für Hyperkaliämie sein, z.B BRASH-Syndrom
- Aldosteronmangel, bedingt durch direkte Störung der Aldosteronproduktion der Nebenniere (Renin ↑, Aldosteron ⊥–↓), oder indirekt durch verminderte Reninproduktion (Renin ↓, Aldosteron ⊥–↓)
- direkte Störung der Aldosteronproduktion (Renin ↑, Aldosteron ⊥–↓)
- primäre Nebennierenrindeninsuffizienz
- isolierter Hypoaldosteronismus
- indirekte Störung der Aldosteronproduktion (Renin ↓, Aldosteron ⊥–↓)
- hyporeninämischer Hypoaldosteronismus (mit normalem oder erhöhtem Blutdruck)
- Pseudohypoaldosteronismus Typ II (Gordon-Syndrom)
- direkte Störung der Aldosteronproduktion (Renin ↑, Aldosteron ⊥–↓)
Risikofaktoren
- gestörte Nierenfunktion (z.B. Hämodialyse)
- Einnahme von Risiko-Medikamenten, die die renale Kaliumelimination beeinflussen
- Komorbiditäten wie Herzinsuffizienz, Diabetes und Hypertonie
- zu hohe Kaliumzufuhr in Kombination mit anderen Risikofaktoren (CKD, Medikamente)
- frühere Episoden einer Hyperkaliämie
- höheres Alter
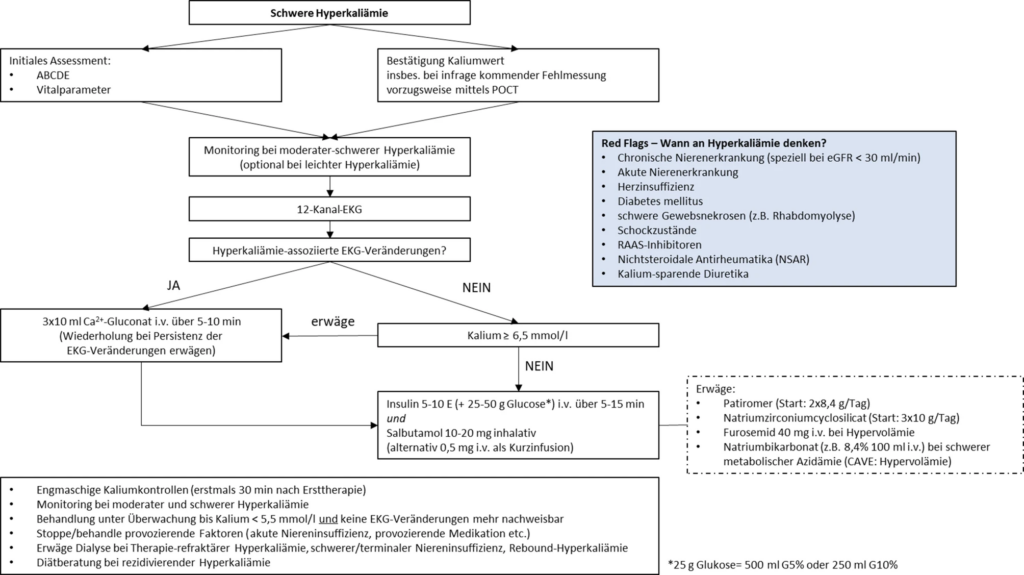
Management der schweren Hyperkaliämie
Grundsätzlich gilt: Eine akute Störung ist bedrohlicher als eine chronische!
Basismanagement der schweren Hyperkaliämie
- zügige Ersteinschätzung durch Messung der Vitalparameter, fokussierte Anamnese inkl. sorgfältiger Medikamentenanamnese und körperlicher Untersuchung bei Vorliegen einer schweren Hyperkaliämie, um akute vitale Bedrohung auszuschließen
- Red Flags für das Vorliegen einer schweren Hyperkaliämie
- CKD (speziell bei eGFR < 30 ml/min/1,73 m2)
- akute Nierenerkrankung
- Herzinsuffizienz
- Diabetes mellitus
- schwere Gewebsnekrosen (z. B. Rhabdomyolyse)
- Schockzustände
- RAASi, NSAR, kaliumsparende Diuretika
- zügige Bestimmung der [K+] anstreben (Analyse des Kaliums aus Vollblut mittels Point-of-Care-Geräten präferieren) –> Bestätigung einer Hyperkaliämie durch Bestimmung der [S‑K+] im Zentrallabor oder durch BGA ist anstreben
- Anfertigung eines 12-Kanal-EKGs so rasch wie möglich in jedem Fall einer [S‑K+] > 6,0 mmol/L –> sofortige Therapie-Einleitung bei EKG-Veränderungen (CAVE: auch sehr hohe [S‑K+] (> 7,0 mmol/L) resultieren mitunter nicht in (typischen) EKG-Veränderungen)
- Überwachung mit kontinuierlichem EKG-Monitoring, nicht-invasive Intervallmessung des Blutdruckes sowie SpO2-Messung sind bei moderater bis schwerer Hyperkaliämie
Therapie einer schweren Hyperkaliämie
- Therapie von Arrhythmien mittels Kalziumsalzen
- Gabe von Kalziumsalzen (3x 10 mL Calciumgluconat 10 % i.v. über 5 – 10 min bei moderater bis schwerer Hyperkaliämie und lebensbedrohlichen-EKG-Veränderungen (Verlust von P‑Wellen, verbreiterter QRS-Komplex, Sinuswellenform, Bradykardie)
- bei Persistenz der EKG-Veränderungen 5 min nach Gabe wiederholte Gabe erwägen
- Verabreichung soll zeitgleich von anderen Maßnahmen zur Kaliumsenkung begleitet werden
- wahrscheinlich auch sinnvoll, i.v.-Kalzium bei extremer Hyperkaliämie ([S-K+] > 7,0 mmol/L) ohne EKG-Veränderungen zu verabreichen, wenn Risikofaktoren für weiteren Kaliumanstieg oder Arrhythmien vorhanden sind
- andersherum bei typischen EKG-Veränderungen für schwere Hyperkaliämie (schwere Bradykardie, Sinuswellen-EKG), aber [S‑K+]-Bestimmung noch nicht möglich, auch i.v.-Kalzium-Gabe
- Kaliumshift
- Insulin
- Gabe von 5 Einheiten Insulin i.v. mit zeitgleicher Gabe von 25 g Glukose bei [S‑K+] > 6,5 mmol/L (alternativ 10 Einheiten Insulin mit 50 g Glukose i.v. über 5 – 15 min)
- Verzicht der Glukosegabe bei relevanter Hyperglykämie (> 200 mg/dL) erwägen
- anschließend engmaschiges Glukosemonitoring (alle 30 min)
- Betamimetika
- Gabe von 10 – 20 mg Salbutamol inhalativ oder alternativ 0,5 mg i.v. als Kurzinfusion bei [S‑K+] > 6,0–6,5 mmol/L unter Abwägung etwaiger Kontraindikationen (Tachykardie, Arrhythmien, koronare Herzkrankheit) zur Senkung der [S‑K+]
- Therapie kann mit Gabe von Insulin (und Glukose) kombiniert werden
- zeitgleiches kardiales Monitoring aufgrund des potenziellen Nebenwirkungsprofils bei Risikopatient*innen
- alternativ auch 0,5 mg Terbutalin als Bolus (CAVE: nur 0,25 mg Sultanol/Terbutalin in 10 mL NaCl langsam i.v. oder als Injektion mit 0,5 mg Sultanol/Terbutalin s.c.; kaliumsenkende Wirkung setzt nach ca. 30 min ein und hält mind. 2 h an)
- CAVE: nichtselektive Betablocker reduzieren kaliumsenkende Wirkung deutlich
- Bikarbonat
- Gabe von Natriumbikarbonat ausschließlich bei schwerer Hyperkaliämie und konkomitanter schwerer hyperchloridämischer metabolischer Azidämie (pH < 7,2) als zusätzliche Therapie erwägen
- Insulin
- Kaliumelimination
- Diuretika
- Einsatz von Diuretika, v.a. i.v.-Schleifendiuretika, in der Therapie der schweren Hyperkaliämie erwoägen, aber auf Patient*innen ohne zeitgleiche Hypovolämie beschränken
- Kaliumbinder
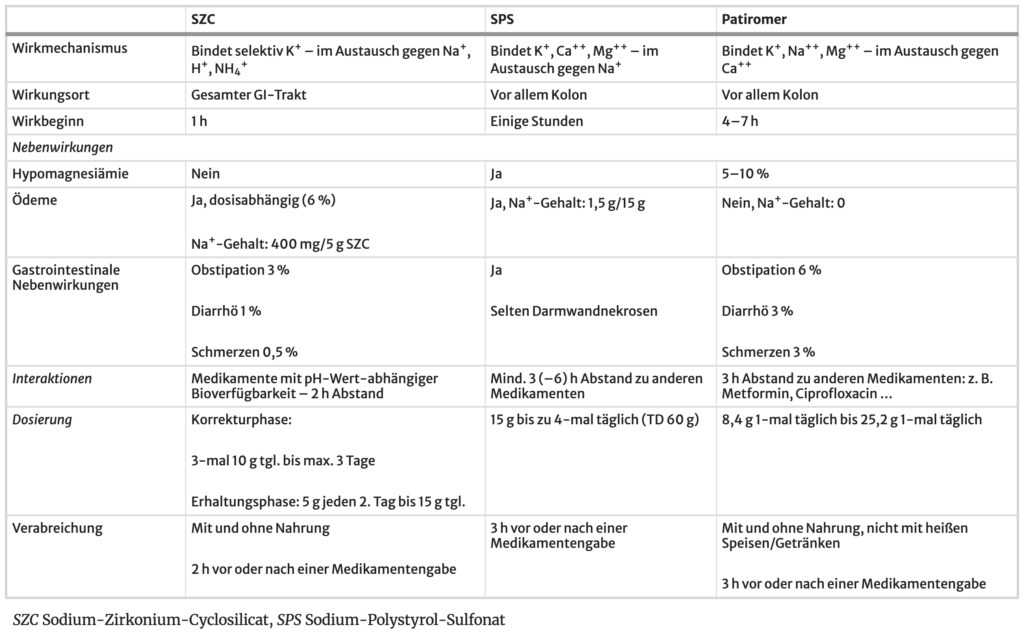
- Patiromer und Natrium-Zirkonium-Cyclosilicat (SZC) ausschließlich als Zusatz zu den oben genannten Maßnahmen in der Behandlung einer schweren Hyperkaliämie (CAVE: verzögerter Wirkung und mutmaßlich interindividuell schwer abschätzbarer Effekt; Kaliumrebound n der weiterführenden Therapie verhindern)
- Dosierungen, Wirkung und Nebenwirkungen für intestinale Kaliumbinder (s. Tabelle)
- Diuretika
- Therapie von Risikofaktoren
- Suche nach provozierenden Faktoren (Medikamente, Diät, Komorbiditäten, Kaliumsupplemente) bei allen Patient*innen mit schwerer Hyperkaliämie (auch zur Reduktion des Risikos einer nochmaligen Hyperkaliämie)
- Indikation zur Nierenersatztherapie
- Hämodialyse bei allen Patient*innen mit terminaler Nierenerkrankung unter chronischer Nierenersatztherapie mit schwerer Hyperkaliämie
- Hämodialyse bei Patient*innen mit therapierefraktärer (inklusive Rebound‑)Hyperkaliämie
- Hämodialyse im Kontext mit schwerer akuter Nierenerkrankung (z. B. Anurie)
- Indikation zur Nierenersatztherapie mit Fachärzti*innen für Nephrologie absprechen
- Monitoring bei schwerer Hyperkaliämie
- Monitoring mit EKG, Herzfrequenz, Blutdruck & SpO2 bis Hyperkaliämie normalisiert oder deutlich rückläufig ist, v.a. bei initialem Vorhandensein von EKG-Veränderungen
- engmaschige Kontrolle der Kaliumkonzentration bei jeder moderaten und schweren Hyperkaliämie
- bei Gabe von Insulin Kontrolle der Blutglukose zur Vermeidung einer Hypoglykämie
Therapie bei milder bis moderater Hyperkaliämie
- Adaptierung der Medikation
- Medikamente ohne prognostischen Benefit, welche Kaliumspiegel anheben (z. B. NSAR, Trimethoprim, Kaliumsupplemente), absetzen
- Absetzen der RAASi-Therapie aufgrund Hyperkaliämie ausschließlich bei persistierender [S‑K+] > 6,0 mmol/L trotz Ausschöpfung kaliumsenkender Therapieoptionen indiziert
- Kaliumelimination
- Kaliumbinder (Patiromer oder SZC) bei CKD + [S‑K+] > 6,0 mmol/L einsetzen, v. a. um Einsatz bzw. maximale Dosierung einer nephroprotektiven RAASi-Therapie zu ermöglichen
- Schleifen- und Thiaziddiuretika zur Senkung der [S‑K+] einsetzen, wenn primär bereits Indikation dafür besteht (Hypervolämie, Hypertonie, Proteinurie), ebenso SGLT‑2-Hemmer
- Laxanzien zur Stuhlregulation bei Obstipation können [S‑K+] ebenfalls senken
- keine Empfehlung für Einsatz von Puffersubstanzen (wie Natriumhydrogenkarbonat) zur Senkung der [S‑K+] aufgrund der geringen Wirkung und des Risikos der Natriumbelastung
- Kaliumbinder
- Kaliumbinder (Patiromer oder SZC) bei Patient:innen mit NET + [S‑K+] > 6,0 mmol/L einsetzen
- Diuretika
- keine offizielle Empfehlung durch ÖGN
- Thiaziddiuretika (v. a. Chlortalidon) und Schleifendiuretika können bei guter Restnierenfunktion die renale Kaliumelimination erhöhen
- kaliuretische Effekt von Schleifendiuretika besser als der von Thiaziddiuretika
- Laxanzien
- keine offizielle Empfehlung durch ÖGN
- Einsatz von Laxanzien ist mit niedrigeren Kaliumwerten assoziiert, was Einsatz von Laxanzien bei CKD-assoziierter Hyperkaliämie und Obstipation sinnvoll macht
- Puffertherapie
- keine offizielle Empfehlung durch ÖGN
- Einsatz zur Behandlung der Hyperkaliämie bei Serum-Bikarbonat > 18 mmol/L primär nicht zu empfehlen
- Nierenersatztherapie
- bei chronischer Hämodialyse bis zu prädialytischer [S‑K+] von 8,0 mmol/L die Dialysat-Kaliumkonzentration nicht auf < 2,0 mmol/L absenken
- bei Peritonealdialyse kann Intensivierung der Behandlung (mehr Behandlungsvolumen) die Kaliumelimination erhöhen
- Ernährungsempfehlungen
- Erhebung der aktuellen Kaliumzufuhr im Rahmen einer professionellen Ernährungsberatung („food record“)
- Reduktion der Kaliumzufuhr bei hoher Kaliumzufuhr > 100 mmol/d (gleiche Diätempfehlungen bezüglich der Art und Menge der Kaliumzufuhr wie bei CKD ohne Dialyse)
Therapie der Hyperkaliämie unter RAAS-Blockade
- Kaliumbinder (Patiromer oder SZC) bei Patient*innen unter RAASi + [S‑K+] > 5,5 mmol/L einsetzen, v. a. um den Einsatz bzw. die maximale Dosierung einer kardio- und nephroprotektiven RAASi-Therapie zu ermöglichen
- liegt [S‑K+] unter Ausschöpfung der K+-senkenden Therapie aber bei > 6,0 mmol/L, RAASi in der Dosis passager reduzieren oder pausieren
- Schleifen- und Thiaziddiuretika können ebenso wie SGLT-2-Hemmer zur Senkung der [K+] eingesetzt werden, wenn primär bereits Indikation dafür besteht (Hypervolämie, Proteinurie etc.)
chronische Therapie der Hyperkaliämie bei Herzinsuffizienz
- Herzinsuffizienztherapie (RAASi, Betablocker, MRA) möglichst aufrechterhalten
- liegt die [S‑K+] unter Ausschöpfung der kaliumsenkenden Therapie aber > 6,0 mmol/L, RAASi in der Dosis reduzieren oder absetzen.
- natriumfreie Kaliumbinder (z. B. Patiromer) bei Patient*innen unter RAASi + [S‑K+] > 5,5 mmol/l einsetzen, v. a. um Einsatz bzw. maximale Dosierung einer nephroprotektiven RAASi-Therapie zu ermöglichen
- SGLT-2-Hemmer können [S‑K+] senken; als Teil der Herzinsuffizienztherapie einsetzen
- Schleifen- und Thiaziddiuretika zur Senkung der [K+] einsetzen, wenn primär bereits Indikation dafür besteht (Hypervolämie, Proteinurie etc.)
chronische Therapie der Hyperkaliämie bei Diabetes
- kardio- und nephroprotektive Therapie mit RAASi bei Diabetes mellitus Typ 2 möglichst aufrechterhalten
- liegt [S‑K+] unter Ausschöpfung der kaliumsenkenden Therapie aber > 6,0 mmol/L, RAASi in der Dosis reduzieren oder absetzen
- Kaliumbinder (Patiromer oder SZC) bei Patient*innen unter RAASi + [S‑K+] > 5,5 mmol/L einsetzen, v. a. um Einsatz bzw. maximale Dosierung einer nephroprotektiven RAASi-Therapie zu ermöglichen
- SGLT-2-Hemmer können [S‑K+] senken; als Teil der Herzinsuffizienztherapie einsetzen
- Schleifen- und Thiaziddiuretika zur Senkung der [K+] einsetzen, wenn primär bereits Indikation dafür besteht (Hypervolämie, Proteinurie etc.)


Sei der Erste der einen Kommentar abgibt