veröffentlichende Fachgesellschaft: European Society of Cardiology (ESC)
Klassifikation gemäß AWMF:
Datum der Veröffentlichung: 30.08.2024
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.1093/eurheartj/ehae179
Grundsätzliches
- periphere arterielle Verschlusskrankheit (pAVK)
- weltweit verbreitet und betrifft 113.000.000 Menschen im Alter ≥ 40 Jahren
- 42,6 % der Betroffenen leben in Ländern mit niedriger bis mittlerer Soziodemografie
- globale Prävalenz: 1,52 % (mit dem Alter zunehmend; 14,91 % bei 80 – 84-Jährigen)
- Frauen häufiger betroffen (18,03 % vs. 10,56 % in gleiche Altersgruppe)
- pAVK-Prävalenz ist von 1990 bis 2019 um 72 % gestiegen (CAVE: Wachstumsrate der Weltbevölkerung von 45 % berücksichtigen)
- weltweite altersstandardisierte Gesamtprävalenz: ca. 1470 pro 100.000 Personen
- Aortenerkrankungen (inkl. Aneurysmen & Dissektionen)
- geschätzte Prävalenz in der Allgemeinbevölkerung: etwa 1 – 3 % (bis zu 10 % in älteren Altersgruppen)
- 2019 weltweit 172.000 Todesfälle im Zusammenhang mit Aortenaneurysmen (Anstieg um 82,1 % ggü. 1990)
- Prävalenz von Bauchaortenaneurysmen (BAA) bei Männern im Alter > 65 Jahre von 1,3 – 3,3 %
- klassische akute Aortendissektion macht etwa 80 – 90 % der AAS mit einer Inzidenz von 2,6 – 3,5 Fällen pro 100 000 Patient*innenjahre
- akute Aortendissektion betrifft v.a. Männern (∼ 65 %) und tritt v.a. im siebten Lebensjahrzehnt (∼ 63 Jahre) auf
- Schwangerschaft erhöht das Risiko für ein akutes Aortensyndrom, v.a. im letzten Trimester (50 %) oder nach der Geburt (33 %)
periphere arterielle Verschlusskrankheit
Symptomatik
- abrupte Verschlechterung der arteriellen Extremitätenperfusion, z.B. durch fortschreitende pAVK, Embolie, Aortendissektion, Transplantatthrombose, Aneurysmathrombose, Trauma etc.
- Schmerzen
- Funktionseinbußen (je länger, desto stärker und desto unwahrscheinlicher ist Rettung der Extremität)
- klinische Einteilung
| Grad | Kategorie | sensorische Störungen | motorisches Defizit | arterielles Doppler-Signal | venöses Doppler-Signal | Rekap-Zeit | Biomarker | Prognose |
|---|---|---|---|---|---|---|---|---|
| I | keine Einschränkung | keine | kein | Ja | Nein | Ja | nicht erhöht | keine unmittelbare Gefährdung |
| IIa | geringfügige Einschränkung | keine oder minimal (an den Zehen) | kein | Nein | Nein | rettbar bei sofortiger Behandlung | ||
| IIb | schwer umkehrbar | mehr als Zehen | mild bis mittelschwer | Nein | Nein | rettbar bei sofortiger Revaskularisierung | ||
| III | irreversibel | tiefgreifend, betäubtes Gefühl | ausgeprägte Lähmung (Rigor) | Nein | Ja | Nein | stark erhöht | großer Gewebeverlust, bleibende Nervenschäden unvermeidlich |
Klassifikation
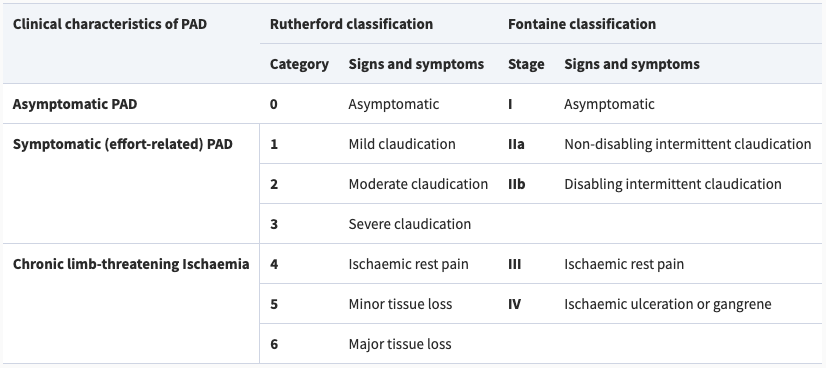
Anamnese & Diagnostik
- umfassende Anamnese erheben, um Ursache der Thrombose und/oder Embolie zu ermitteln
- RR-Messung an beiden Armen
- Laborparameter-Bestimmung (Lipide, Nüchtern-BZ & HbA1c, Nieren- & Leberwerte, großes Blutbild, Gerinnungsparameter, Elektrolyte und Entzündungsmarker wie CRP sowie ggf. Schilddrüsenwerte
- Bildgebung mittels digitaler Subtraktionsangiographie, CT-Angiographie, Duplex-Sono und/oder kontrastverstärkte Magnetresonanzangiographie, v.a. bei schwieriger Beurteilung von neurologischen Defiziten
- Biomarker-Bestimmung (z.B. Kreatininkinase & Myoglobin bzgl. Rhabdomyolyse)
Risikofaktoren
- modifizierbare Risikofaktoren
- Tabakkonsum
- Diabetes
- Lipide
- Bluthochdruck
- nicht-modifizierbare Risikofaktoren
- Alter
- Geschlecht
- Polygene und familiäre Vererbung
- sonstige Risikofaktoren
- Übergewicht
- Bewegungsarmut
- Schlafstörungen
- Stressiger Lebensstil
- Alkoholkonsum
- Diät
- Entzündungen
- Apolipoproteine
- Autoimmunerkrankung
- Umweltverschmutzung
- Sozioökonomischer Status
- bei Frauen: Menopause und schwangerschaftsbedingter Bluthochdruck/Diabetes
Therapie
- Transport in spezialisierte Klinik (Zeitraum, in dem Skelettmuskulatur und Nerven Ischämie tolerieren: ca. 4 – 6 h)
- Analgesie
- Antikoagulation: Gabe von Heparin als Bolus mit 5000 I.E. oder 70 – 100 I.E./kgKG i.v., gefolgt von kontinuierlicher Infusion mit Dosisanpassung
- Flüssigkeitstherapie i.v.
- chirurgische & interventionelle Behandlung (dringende Revaskularisierung), v.a. bei neurolog. Defiziten
- nach Revaskularisation auf Kompartmentsyndrom achten und dieses gg. behandeln (Fasziotomie)
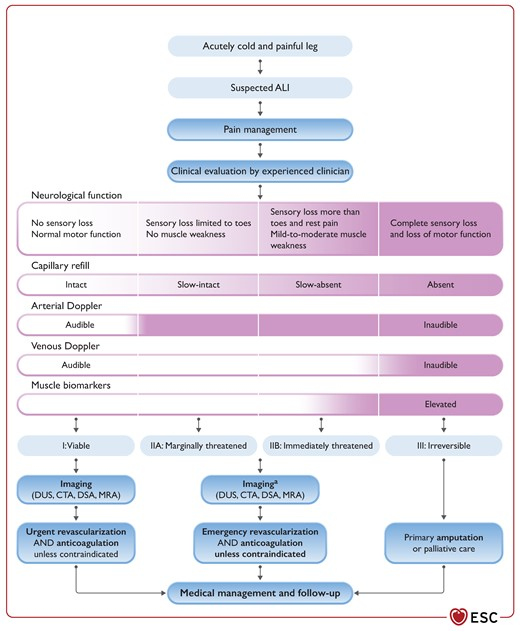
akute thorakale Aortensyndrome
- akutes Aortensyndrom (AAS): lebensbedrohliche Notfälle wie akute Aortendissektion (AAD), intramurales Hämatom (IMH), penetrierender Aortenulkus (PAU) & traumatische Aortenverletzungen (TAI)
- Stanford- & DeBakey-Klassifikation für das AAS
- Aorta ascendens betroffen (Stanford A oder DeBakey Typ I & Typ II)
- Aorta ascendens nicht betroffen (Stanford B oder DeBakey Typ IIIa & Typ IIIb)
- unabhängig von Entstehungsstelle des Intimarisses
- Klassifizierung berücksichtigt nicht nur anatomische und Therapieaspekte, sondern auch prognostische Auswirkungen
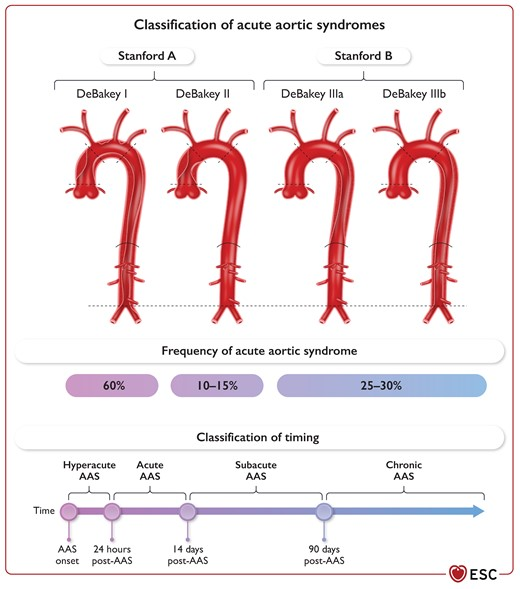
Symptomatik
- plötzliche, starke Brust-/Rückenschmerzen (oft als „stechend“ beschrieben)
- i.d.R. Vorgeschichte mit arterieller Hypertonie
- bei etwa 6,4 % der Patient*innen treten keine Schmerzen
- häufig Hypotonie und Schock
- bei Typ A Aortendissektion zusätzlich Perikarderguss, Aortenregurgitation und Beteiligung der Koronararterien mit Möglichkeit eines ACS (v.a. rechte Koronararterien)
- ggf. Komplikationen wie Querschnittslähmung (infolge Ischämie der Wirbelsäule), akute Nierenschädigung, Darmischämie oder Ischämie der Gliedmaßen
Diagnostik
- neurologische Beurteilung
- Herz- & Lungenauskultation (diastolisches Aortengeräusch, Perikardreiben usw.)
- abdominalen Palpation (Empfindlichkeit usw.)
- Beurteilung der peripheren Pulse (v.a. bzgl. Pulsdefizit)
- Beurteilung der Mobilität & Sensibilität der oberen und unteren Gliedmaßen
- routinemäßiges Thorax-Röntgen und EKG (CAVE: Fehlen von Befunden sollte weitere Untersuchungen nicht verzögern)
- Blutuntersuchung (häufigster Befund ist D-Dimer-Anstieg, bei < 500 ng/mL ist AAS unwahrscheinlich)
- EKG-gesteuertes Kardio-CT als Diagnostik der 1. Wahl
- transthorakale Echokardiographie, um Perikarderguss, Wandbewegungsstörungen, Aortenregurgitation und Aortendurchmesser zu beurteilen (v.a. wenn Kardio-CT nicht möglich)
- alternativ kardiales MRT erwägen, wenn Kardio-CT nicht möglich
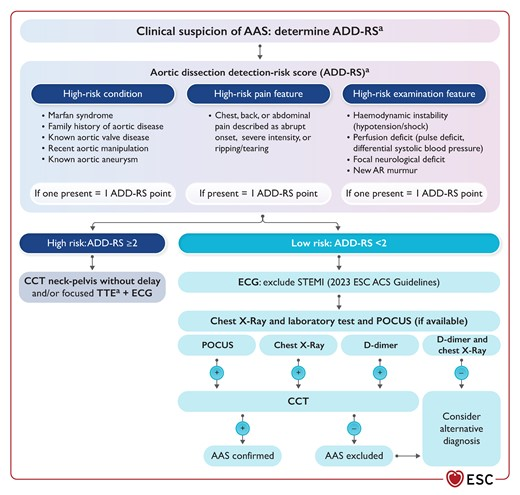
- typische Komplikationen
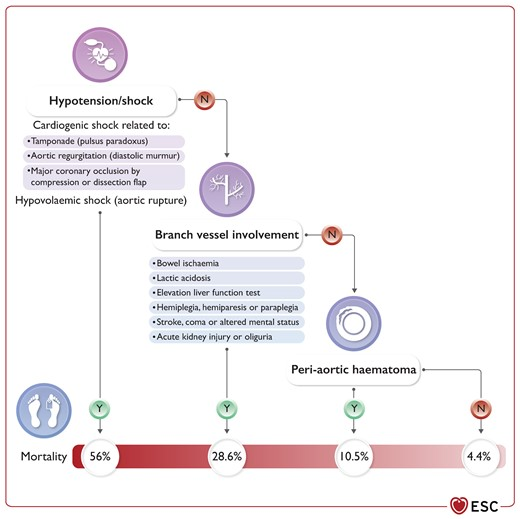
Therapie
- Transport auf ITS in Klinik mit Spezialisierung
- titrierte Senkung auf RRsys < 120 mmHg (ggf. Tolerierung höherer Werte bei Malperfusion, z.B. spinaler Ischämie oder begleitenden Hirnverletzungen) und HF < 60/min
- Gabe von Betablocker i.v. (Labetalol als Mittel der 1. Wahl, alternativ Esmolol)
- Gabe von Nitraten oder Calciumantagonisten wie Dihydropyridine (z. B. Nicardipin), wenn Ziel-RR mit Betablockern nicht erreicht
- frühzeitige Anlage von invasiver RR-Messung
- ggf. zur Analgesie titrierte Gabe von Morphin


Sei der Erste der einen Kommentar abgibt