veröffentlichende Fachgesellschaft: Surviving Sepsis Campaign (SSC) der Society of Critical Care Medicine (SCCM) & European Society of Intensive Care Medicine (ESICM)
Datum der Veröffentlichung: 23.03.2026
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.1007/s00134-026-08361-1
Terminologie
- eindeutige Sepsis: Sepsis wird anhand von Anamnese, klinischer Untersuchung und diagnostischer Tests bestätigt (alternative Diagnose sehr unwahrscheinlich)
- wahrscheinliche Sepsis (hoher Verdacht auf Sepsis): Sepsis ist anhand von Anamnese, klinischer Untersuchung und diagnostischer Tests die wahrscheinlichste Diagnose (alternative Diagnose weniger wahrscheinlich)
- mögliche Sepsis (mäßiger Verdacht auf Sepsis): Sepsis ist mögliche Diagnose, jedoch auf Grundlage von Anamnese, klinischer Untersuchung und diagnostischer Tests auch alternative Diagnose wahrscheinlich
- unwahrscheinliche Sepsis (geringer Verdacht auf Sepsis): klinische Beurteilung passt nicht zum Bild einer Sepsis (alternative Diagnose ist auf Grundlage von Anamnese, klinischer Untersuchung und diagnostischer Tests wahrscheinlicher)
Früherkennung und initiale Behandlung
Screening
- Einführung von Programmen zur Leistungsverbesserung im Bereich Sepsis, die ein Sepsis-Screening bei akut erkrankten Hochrisikopatienten, standardisierte Behandlungsabläufe sowie die Umsetzung von Strategien zur Qualitätsverbesserung bei Sepsis umfassen
- Nutzung von „Code-Sepsis“- oder „Sepsis-Huddle“-Protokoll (Protokolle umfasst Besprechung im multidisziplinären Teams am Krankenbett, um nach positivem Sepsis-Screening Diagnose und Behandlung zu besprechen und zu beschleunigen)
- Verwendung von Standard-Sepsis-Screening-Tools bei akut erkrankten Erwachsenen, die mit RTW oder RTH ins KH transportiert werden
- Verwendung von NEWS, NEW2, MEWS oder SIRS anstelle von qSOFA als einziges Instrument zur Sepsis-Screening
Diagnostik
- Sepsis ist klinische Diagnose und die nicht anhand eines einzigen Biomarkers oder diagnostischen Tests bestätigt oder ausgeschlossen werden sollte
- unzureichende Belege für Empfehlung bzgl. Verwendung neuartiger Schnelldiagnostik-Tests zur Erfassung der Wirtsreaktion
- Entnahme von Blutkulturen so bald wie möglich und idealerweise vor Einleitung der Antibiotika-Therapie bei möglicher, wahrscheinlicher oder definitiver Sepsis oder septischem Schock
- Messung des Blutlaktat bei möglicher, wahrscheinlicher oder definitiver Sepsis oder septischem Schock
initiales Management
- Flüssigkeitstherapie
- Sepsis und septischer Schock sind medizinische Notfälle bei denen die Behandlung und Wiederbelebung unverzüglich beginnen sollte
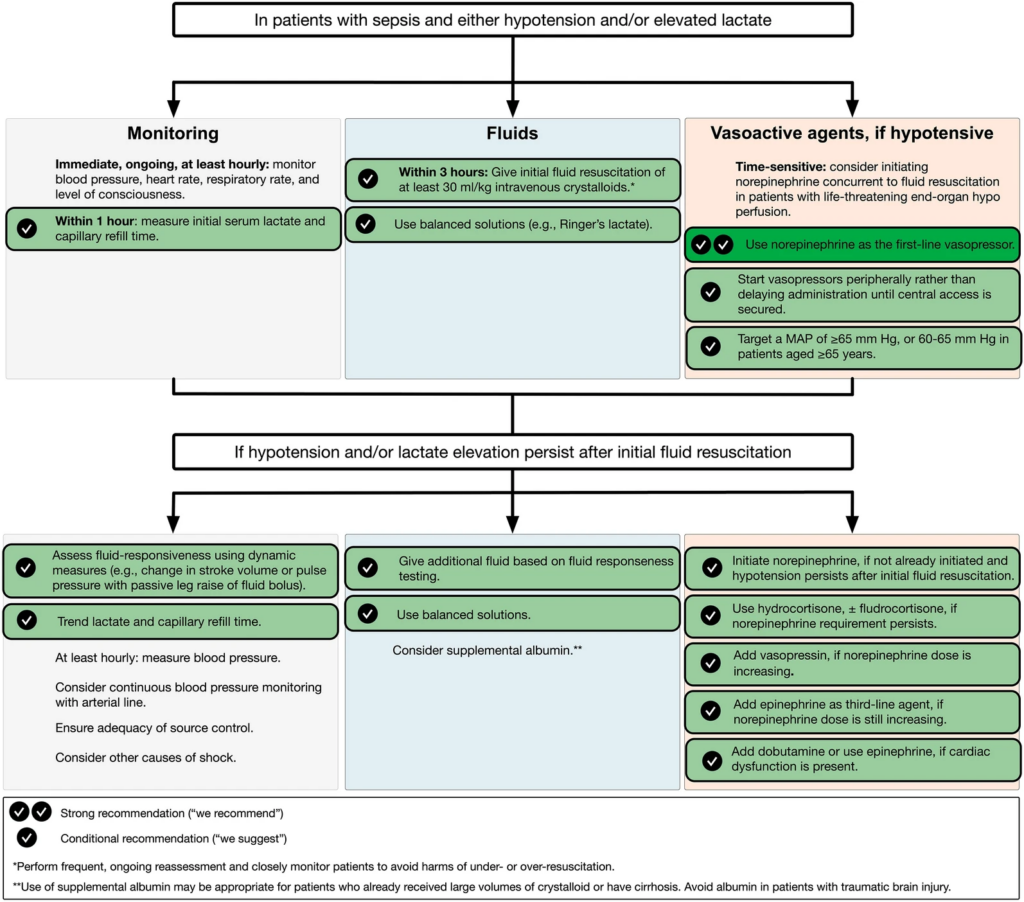
- Gabe von mind. 30 mL/kg Kristalloide i.v. in den ersten 3 h bei sepsisbedingter Hypoperfusion oder septischem Schock
- individuellen Patient*innenmerkmale und jeweiligen Kontext berücksichtigen
- häufige, fortlaufende Neubewertung und engmaschige Überwachung, um Schäden durch Unter- oder Überinfundierung zu vermeiden
- gewichtsabhängiges Flüssigkeitsvolumen auf Grundlage des tatsächlichen Körpergewichts oder – bei Patient*innen mit BMI > 30 kg/m² – anhand des angepassten oder idealen Körpergewichts berechnen (siehe Tabelle)
| Gewicht (kg) | Größe (1,5 m) | Größe (1,7 m) | Größe (1,9 m) |
|---|---|---|---|
| 50 | 1,5 L | 1,5 L | 1,5 L |
| 60 | 1,8 L | 1,8 L | 1,8 L |
| 70 | 2,1 L | 2,1 L | 2,1 L |
| 80 | 1,9 L | 2,4 L | 2,4 L |
| 90 | 2,0 L | 2,4 L | 2,7 L |
| 100 | 2,1 L | 2,5 L | 3,0 L |
| 110 | 2,2 L | 2,6 L | 3,3 L |
| 120 | 2,3 L | 2,7 L | 3,0 L |
| 130 | 2,5 L | 2,8 L | 3,1 L |
| 140 | 2,6 L | 3,0 L | 3,2 L |
| 150 | 2,7 L | 3,1 L | 3,3 L |
| 160 | 2,8 L | 3,2 L | 3,4 L |
- Vasopressoren
- initiale Flüssigkeitstherapie mit Kristalloiden als Bolus, gefolgt von Unterstützung durch Vasopressoren, falls Hypotonie anhält
- sofortige & gleichzeitige Vasopressoren-Gabe bei instabilem septischem Schock ggf. gerechtfertigt (klinische Zeichen: stark gesunkener RR, marmorierte Haut, aschfahles Aussehen, Zyanose/stark gesunkener Blutdruck, fleckige Haut, aschfahles Aussehen, Zyanose/verminderte SpO2, Tachykardie & Bewusstseinsstörungen)
- periphere Gabe von Vasopressoren, um MAD wiederherzustellen (kein Warten bis Anlage von ZVK)
- keine ausreichenden Daten für Empfehlung bzgl. Anwendungsdauer, Dosierung oder Zugangsart (pvK-Größe oder anatomische Lage); keine Empfehlung für Midline-Katheter
- initiale Flüssigkeitstherapie mit Kristalloiden als Bolus, gefolgt von Unterstützung durch Vasopressoren, falls Hypotonie anhält
- Ziele für mittleren arteriellen Druck (MAD)
- initialer MAD-Zielwert von 65 mmHg ggü. höheren MAP-Zielwerten beim septischen Schock (+/- 5 mmHg; Vasopressoren so titrieren, dass MAD innerhalb dieses Bereichs liegt)
- initialer MAD-Zielwert von 60 – 65 mmHg bei Erwachsenen mit septischem Schock > 65 Jahre
- Einweisung auf ITS
- bei Sepsis oder septischem Schock Aufnahme auf ITS innerhalb von 6 h, falls notwendig
Infektion
Zeitpunkt für Beginns der Antibiotikatherapie im KH
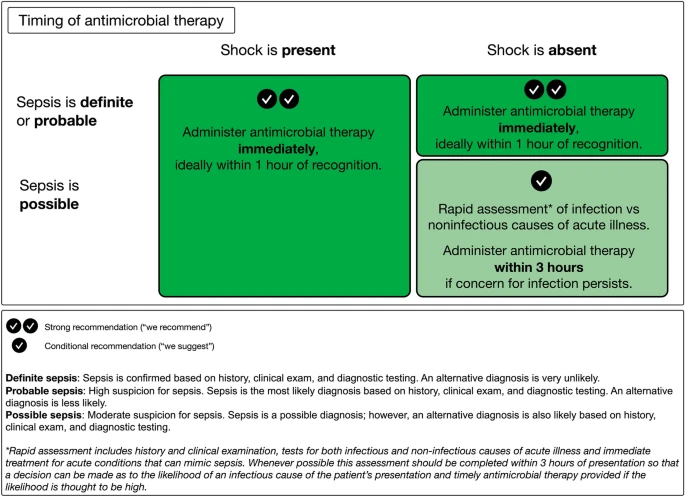
- sofortige Antibiotikatherapie, idealerweise in < 1 h nach Diagnosestellung, bei möglichem, wahrscheinlichem oder sicherem septischen Schock
- sofortige Antibiotikatherapie, idealerweise in < 1 h nach Diagnosestellung, bei wahrscheinlicher oder gesicherter Sepsis ohne Schock
- zeitlich begrenzte Reihe von Schnelluntersuchungen bei möglicher Sepsis ohne Schock (Antibiotikatherapie so schnell wie möglich nach angemessener Beurteilung, wenn sich der V.a. Sepsis bestätigt, am besten in < 3 h nach Diagnosestellung)
- schnelle Beurteilung der Wahrscheinlichkeit infektiöser ggü. nicht-infektiösen Ursachen für akute Erkrankung bei möglicher Sepsis ohne Schock
- Aufschieben der Antibiotikatherapie und engmaschige Überwachung bei Erwachsenen mit geringer Infektionswahrscheinlichkeit und ohne Schock
Zeitpunkt für Beginns der Antibiotikagabe auf dem Weg ins KH
- Einleitung der Antibiotikatherapie bereits im RTW oder RTH bei gesicherter oder wahrscheinlicher Sepsis und Hypotonie (d. h. septischem Schock), bei denen die voraussichtliche Wartezeit bis zur medizinischen Behandlung im KH > 60 min beträgt (CAVE: Blutkulturen nach Möglichkeit vor Antibiotika-Gabe entnehmen).
- präklinische Antibiotikatherapie sollte erst dann erfolgen, wenn strukturiertes Verfahren zur Sepsis-Erkennung vorhanden ist
Biomarker-gesteuerte Einleitung der Antibiotikatherapie
- bei möglicher oder wahrscheinlicher Sepsis oder septischem Schock bei der Entscheidung über Beginn der Antibiotikatherapie allein auf klinische Beurteilung zurückzugreifen, anstatt Procalcitonin in Kombination mit klinischer Beurteilung heranzuziehen
Infektionsfokus-Kontrolle
- bei Sepsis oder septischem Schock umgehende Untersuchung auf spezifische anatomische Diagnosen oder Infektionsherde, die sofortige Bekämpfung des Infektionsherdes erfordern
- frühzeitige Bekämpfung des Infektionsherdes ggü. späterer Therapie bei Sepsis oder septischem Schock und spezifischer anatomischer Diagnose oder Infektionsherd, der eine Behandlung erfordert (idealerweise in < 6 h nach Diagnosestellung von Sepsis oder septischem Schock)
Abdeckung durch empirisch Medikamente gegen multiresistente Erreger
- empirische Antibiotikatherapie, die gegen multiresistente Erreger wirksam ist, bei Sepsis oder septischem Schock mit hohen Risiko für Infektion mit bestimmtem multiresistenten Erreger
- Risikofaktoren: Besiedlung mit betreffenden multiresistenten Erregern, frühere Infektion mit betreffenden multiresistenten Erregern, längere Anwendung von Breitbandantibiotika sowie längerer Krankenhausaufenthalt in Abteilung mit hoher Prävalenz des betreffenden multiresistenten Erregers
- keine empirische Antibiotikatherapie, die gegen multiresistente Erreger wirksam ist, bei Sepsis oder septischem Schock mit geringem Risiko für Infektion mit bestimmtem multiresistenten Erreger
empirische antimykotische Abdeckung
- keine empirische Antimykotika-Therapie bei Sepsis oder septischem Schock
empirische anaerobe Abdeckung
- empirischen Antibiotikatherapie ohne Abdeckung anaerober Erreger bei Sepsis oder septischem Schock ohne Risikofaktoren für anaerobe Infektion
- wenn Abdeckung potenziell multiresistenter Erreger erforderlich ist, sind Wirkstoffe mit anaerober Wirksamkeit (z.B. Piperacillin-Tazobactam oder Carbapeneme) geeignet, wenn alternative Wirkstoffe ohne anaerobe Abdeckung unzureichend wirken
- empirischen Antibiotikatherapie mit Abdeckung anaerober Erreger bei Sepsis oder septischem Schock mit spezifischen Risikofaktoren für anaerobe Infektion
- Risikofaktoren: intraabdominale oder tiefsitzende gynäkologische/geburtshilfliche Infektionsherde, nekrotisierende Weichteilinfektionen, Infektionen im Kopf- und Halsbereich sowie Abszesse oder Empyeme des Zentralnervensystems
mikrobiologische Überwachung als Grundlage für empirische Antibiotikatherapie
- keine ausreichenden Belege für Empfehlung bzgl. der Verwendung von mikrobiologischen Proben aus den oberen Atemwegen auf Abteilungsebene (d.h. auf der gesamten ITS) als Grundlage für empirische Antibiotikatherapie
erregerspezifische Schnelltests
- Einsatz pathogen-spezifischer Schnelltests auf Einzelfallbasis bei ausgewählten Patient*innen mit Sepsis oder septischem Schock unter Berücksichtigung klinischer Merkmale, lokaler Erreger- und Resistenzmuster, saisonaler Schwankungen sowie Verfügbarkeit von Tests und Leitlinien zum verantwortungsvollen Umgang mit Antibiotika
Biomarker für Candida-Pilzinfektionen als Orientierungshilfe für Beginn der antimykotischen Therapie
- keine Verwendung von Candida-Biomarkern zur Einleitung einer empirischen Antimykotika-Therapie bei Sepsis oder septischem Schock
- Verwendung von Candida-Biomarkern als Richtwert für Beginn einer empirischen Antimykotika-Therapie kann bei ausgewählten Patient*innen mit hohem Risiko für Candida-Infektion, z.B. Patient*innen mit Immunsuppression, längerer Antibiotikaexposition, längerem KH-Aufenthalt und intraabdominaler Infektionsquelle, von Fall zu Fall in Betracht ziehen
Langzeitinfusion von β-Lactam-Antibiotika
- Anwendung einer verlängerten Beta-Laktamen-Infusionstherapie zur Erhaltungstherapie (nach einer initialen Aufsättigungsdosis) ggü. Bolusgaben bei Sepsis oder septischem Schock
therapeutisches Drug-Monitoring (TDM) der antimikrobiellen Therapie
- Anwendung des antimikrobiellen therapeutischen Drug-Monitorings (TDM) im Einzelfall bei ausgewählten Patient*innen mit Sepsis oder septischem Schock, basierend auf klinischen Merkmalen, lokalen Erreger- und Resistenzmustern, Arzneimittelklasse und Verfügbarkeit von TDM
Deeskalation und Absetzen von Antibiotika
- Patient*innen kontinuierlich neu bewerten, nach alternativen Diagnosen suchen und empirische antimikrobielle Therapie abbrechen, wenn bei V.a. Sepsis oder septischen Schock, aber unbestätigter Infektion, alternative Krankheitsursache nachgewiesen oder stark vermutet wird
- Deeskalation der antimikrobiellen Therapie, wenn bestätigte mikrobiologische Diagnose und Resistenzprofil vorliegen (Deeskalation: unnötige antimikrobielle Therapien abbrechen oder, falls angebracht, Spektrum der antimikrobiellen Wirkstoffe einengen)
- Deeskalation der antimikrobiellen Therapie, wenn in den abschließenden Kulturergebnissen keine Krankheitserreger identifiziert wurden
Biomarker-Leitlinien für Abbruch der Antimykotika-Therapie
- keine Empfehlung für Verwendung von Candida -Pilzbiomarkern zur Steuerung des Abbruchs der empirischen Antimykotika-Therapie bei Sepsis oder septischem Schock und empirischer Antimykotika-Therapie
- Einsatz von Candida -Biomarkern zur Steuerung des Abbruchs der empirischen Antimykotika-Therapie im Einzelfall bei sich klinisch verbesserten, ausgewählten Patient*innen mit hohem Risiko für Candida- Infektion erwägen (v.a. Patient*innen mit Immunsuppression, Langzeitanwendung von Antibiotika, längerem Krankenhausaufenthalt und intraabdomineller Infektionsquelle)
Dauer der antimikrobiellen Therapie
- Empfehlung für kürzere ggü. längerer Dauer der antimikrobiellen Therapie bei Erstdiagnose einer Sepsis oder eines septischen Schocks und adäquater Herdkontrolle
Biomarker-Leitlinien für Absetzen von Antibiotika
- zur Entscheidung über Abbruch der antimikrobiellen Therapie sowohl Procalcitonin als auch klinische Beurteilung heranziehen anstatt der alleinigen klinischen Beurteilung bei Erstdiagnose von Sepsis oder septischem Schock und adäquater Herdkontrolle, bei denen die optimale Therapiedauer unklar ist
selektive Dekontamination des Verdauungstrakts
- selektive Dekontamination des Verdauungstrakts bei beatmeten Erwachsenen mit Sepsis oder septischem Schock in Kliniken mit geringer Prävalenz von Antibiotikaresistenzen
hämodynamisches Management
Flüssigkeitstyp
- Verwendung von Kristalloiden als Volumentyp der 1. Wahl bei Sepsis oder septischem Schock
- Verwendung von balancierten Kristalloiden ggü. NaCl 0,9% bei Sepsis oder septischem Schock (NaCl 0,9% bei Sepsis und SHT)
- alleinige Anwendung von Kristalloiden ggü. Kristalloiden mit Albumin bei Sepsis oder septischem Schock (zusätzliche Gabe von Albumin kann bei Patient*innen, die bereits große Kristalloid-Mengen erhalten haben oder an Leberzirrhose leiden, indiziert sein; kein zusätzliches Albumin bei SHT)
- kein HES bei Sepsis oder septischem Schock
- keine Gelantine bei Sepsis oder septischem Schock
liberaler vs. konservativer Ansatz der Flüssigkeitstherapie
- Anwendung einer liberalen oder restriktiven Flüssigkeitstherapie auf Grundlage individueller Patient*innen- und Gesundheitssystemfaktoren bei Erwachsenen mit Sepsis oder septischem Schock, die bereits 30 mL/kg erhalten haben und weiterhin eine Hypoperfusion aufweisen
- Faktoren sind u.a. aktueller klinischer Zustand, chronische Erkrankungen (z.B. Herzinsuffizienz) und Verfügbarkeit von Überwachungsbetten (d.h., ob restriktiver Ansatz den Einsatz von Vasopressoren erfordert)
Flüssigkeitstherapie gesteuert durch dynamische Maßnahmen
- dynamische Maßnahmen zur Steuerung der Flüssigkeitstherapie der rein körperlichen Untersuchung oder statischen Maßnahmen vorziehen (dynamische Messgrößen sind u.a. die Reaktion auf passives Anheben der Beine oder Flüssigkeitsbolus unter Verwendung des Schlagvolumens, der Schlagvolumenvariation, des Pulsdrucks oder der Pulsdruckvariation)
Geräte zur Überwachung des Herzzeitvolumens
- unzureichende Belege für Empfehlung bzgl. der Anwendung von minimalinvasiver oder nichtinvasiver HZV-Überwachung zusätzlich zur üblichen Behandlung
- minimalinvasive HZV-Messung: Geräte, die arteriellen Katheter erfordern
- nichtinvasive HZV-Messung: Geräte, die Bioreaktanz nutzen
- Standardversorgung bezeichnet Versorgung ohne Pulmonalarterienkatheter
- Einsatz von Ultraschall in der Intensivmedizin nicht evaluiert
serielle Laktatmessung
- serielle Laktatmessungen zur Steuerung der Therapie bei Sepsis und erhöhtem Laktatwert oder septischem Schock
- Flüssigkeitszufuhr nach initialer Flüssigkeitsgabe und Überwachung des Laktatabfalls individuell anpassen, anstatt Flüssigkeitszufuhr bis zur Normalisierung des Laktatwerts fortzusetzen
Rekap-Zeit
- Verwendung der Rekap-Zeit zur Steuerung der Reanimation als Ergänzung zu anderen Perfusionsmessungen bei Sepsis oder septischem Schock
Vasopressoren i.v.
- Anwendung von Noradrenalin als Vasopressor der 1. Wahl ggü. Dopamin, Epinephrin oder Selepressin beim septischen Schock
- kein Terlipressin beim septischen Schock
- Noradrenalin als Vasopressor der 1. Wahl ggü. Vasopressin oder Angiotensin II beim septischen Schock
- zusätzliche Gabe von Vasopressin beim septischen Schock unter eskalierender Noradrenalin-Dosis
- zusätzliche Gabe von Epinephrin bei septischem Schock und unzureichendem MAD trotz Noradrenalin und Vasopressin (alternativ Adrenalin, wenn Vasopressin nicht verfügbar)
- Anwendung von Noradrenalin oder Adrenalin als Vasopressor der 1. Wahl bei septischem Schock und gleichzeitiger Herzfunktionsstörung
- bei Tachyarrhythmie oder signifikanter Sinustachykardie Noradrenalin bevorzugen
- bei Bradyarrhythmie oder signifikanter Sinusbradykardie Adrenalin bevorzugen
Methylenblau
- unzureichende Belege für Empfehlung bzgl. Methylenblau i.v. bei refraktärem septischem Schock und steigendem Bedarf an Vasopressoren
Inotropika
- Inotropika-Gabe bei septischem Schock und kardialer Dysfunktion mit persistierender Hypoperfusion trotz ausreichendem Flüssigkeitsstatus und arteriellem Blutdruck
- zusätzlich Inotropika, bei Patient*innen, die Vasopressoren benötigen, um MAD auf Zielwert zu halten
- zusätzliche Gabe von Dobutamin zu Noradrenalin oder alleinige Anwendung von Adrenalin bei septischem Schock, der trotz adäquater Flüssigkeitszufuhr und normalem arteriellen Blutdruck weiterhin eine Hypoperfusion und kardiale Dysfunktion aufweist
- keine Gabe von Levosimendan bei septischem Schock und kardialer Dysfunktion mit persistierender Hypoperfusion trotz adäquatem Volumenstatus und arteriellem Blutdruck
Midodrin
- unzureichende Belege für Empfehlung bzgl. Midodrin oral bei septischem Schock und fortgesetztem Bedarf an Vasopressoren
Beta-Blocker
- keine Beta-Blocker bei septischem Schock (mpfehlung basiert auf Erkenntnissen zur Wirksamkeit kurzwirksamer, intravenöser Betablocker wieEsmolol und Landiolol bei der Behandlung des septischen Schocks)
Beatmung & Atemunterstützung
Überwachung der Hypoxämie
- Messung der Sauerstoffsättigung mittels Pulsoximetrie (SpO2) oder arterieller Blutgasanalyse (SaO2) in Verbindung mit körperlicher Untersuchung und klinischer Expertise
- BGA (art.) ist Goldstandard zur Beurteilung der Oxygenierung
- CAVE: SpO2/FiO2-Verhältnis gemessen mittels Pulsoximetrie ist bei Patient*innen im Schockzustand, mit dunklerer Hautfarbe und/oder Sauerstoffsättigung < 90 % oder > 97 % weniger genau
Sauerstoffziele
- bei Sepsis und akutem hypoxämischem Lungenversagen FiO2-Wert so einstellen, dass je nach Patient*innenfaktoren & Ressourcenbeschränkungen entweder höhere, liberalere Sauerstoffwerte oder niedrigere, konservativere Sauerstoffwerte angestrebt werden (i.d.R. SpO2 zw. 90 – 96 %)
Nichtinvasive Atemunterstützung
- High-Flow-Nasenkanülen-Therapie (HFNC) ggü. konventioneller Sauerstofftherapie bei Sepsis und akutem hypoxämischem Atemversagen bevorzugen (Empfehlung gilt für Patient*innen mit PaO2/FiO2-Verhältnis < 200 oder SpO2/FiO2-Verhältnis < 235)
- HFNC als initiale Therapie ggü. nichtinvasiver positiver Druckbeatmung bei Sepsis und akutem hypoxämischem Atemversagen bevorzugen
- HFNC gegenüber abwechselnder Anwendung von High-Flow-Beatmung und nichtinvasiver positiver Druckbeatmung bei Sepsis und akutem hypoxämischem Atemversagen bevorzugen bevorzugen
wache Patient*innen in Bauchlage
- Therapieversuch in Bauchlage bei Sepsis und akutem hypoxämischem Atemversagen
- Dauer und Häufigkeit der Bauchlagerung hängen von Toleranz der Patient*innen ab
- bei nicht intubierten Patient*innen keine Sedierung zur Förderung der Toleranz einer Bauchlagerung
invasive mechanische Beatmung
- Anwendung einer Beatmungsstrategie mit niedrigem Tidalvolumen (6 mL/kg) ggü. Strategie mit hohem Tidalvolumen (> 10 mL/kg) bei Sepsis und ARDS
- Verwendung eines AZV von 6 – 8 mL/kg Idealgewicht ggü. niedrigeren AZV (4 bis < 6 mL/kg Idealgewicht)
- Patient*innen regelmäßig auf Entwicklung eines ARDS untersuchen, da ARDS-Diagnose in der klinischen Praxis häufig übersehen oder verzögert wird
- Plateau-Druck von 30 cmH2O bei Sepsis und ARDS
- Anwendung eines höheren PEEP ggü. niedrigerem PEEP bei Sepsis und mittelschwerem bis schwerem ARDS
- keine Anwendung einer inkrementellen PEEP-Titrationsstrategie bei Sepsis und mittelschwerem bis schwerem ARDS
- Anwendung der Bauchlagebeatmung für > 12 h tgl. bei Sepsis und mittelschwerem bis schwerem ARDS
- Anwendung intermittierender Muskelrelaxanzien-Bolusgaben ggü. kontinuierlichen Muskelrelaxanzien-Infusion
veno-venöse ECMO
- Einsatz der veno-venösen ECMO bei schwerem ARDS aufgrund einer Sepsis, wenn konventionelle mechanische Beatmung in erfahrenem Zentrum mit entsprechender Infrastruktur versagt
Begleittherapien zur Behandlung der Sepsis
- Anwendung von Kortikosteroiden i.v. bei septischem Schock
- keine fiebersenkende Therapie zur Verbesserung der klinischen Outcomes bei Sepsis oder septischem Schock, egal ob medikamentös oder durch Oberflächenkühlung
- CAVE: Empfehlung gilt nicht für Anwendung fiebersenkender Mitteln zur Schmerzkontrolle, zur Linderung von Symptomen oder bei Patient*innen mit anderen Indikationen zur Temperaturkontrolle (z.B. neurointensivmedizinischen Patient*innen oder Patient*innen nach einem Herzstillstand)
- kein Vitamin C i.v. bei Sepsis oder septischem Schock
- keine Immunglobuline i.v. bei Sepsis oder septischem Schock
- Blutreinigung
- keine Anwendung von Blutreinigungsverfahren, inkl. Hämoperfusion, Hochdosis-Hämofiltration oder Plasmaaustausch, bei Sepsis oder septischem Schock
- keine Polymyxin-B-Hämoperfusion bei Sepsis oder septischem Schock
- kein Vitamin D bei Sepsis oder septischem Schock
- kein XueBiJing i.v. bei Sepsis oder septischem Schock (Ausnahme: Länder mit behördlicher Zulassung)
zusätzliche unterstützende Therapien bei Sepsis
- Stressulkusprophylaxe mit Protonenpumpenhemmern bei Risikofaktoren für GI-Blutungen
- keine Probiotika bei Sepsis oder septischem Schock
- aktive Flüssigkeitsentfernung bei septischem Schock nach akuter initialer Flüssigkeitstherapie (akuter initiale Flüssigkeitstherapie = Steigerung der Vasopressor-Dosis, die fortgesetzte Gabe hoher Vasopressor-Dosen oder die Notwendigkeit einer fortlaufenden Volumensubstitution)
- aktive Flüssigkeitsentfernung umfasst Diuretika und, falls dies nicht ausreichend, Ultrafiltration oder extrakorporale Flüssigkeitsentfernung
- Faktoren, die bei der Entscheidung für aktive Flüssigkeitsentfernung zu berücksichtigen sind: kardiorespiratorische Funktion, Vasopressor-Dosis, klinischer Verlauf, periphere Ödeme, Körpergewicht und Flüssigkeitshaushalt
- Anwendung einer restriktiven Transfusionsstrategie bei Sepsis oder septischem Schock
- frühzeitige Einleitung der enteralen Ernährung (innerhalb von 72 h) bei Sepsis oder septischem Schock
- Einleitung einer Insulintherapie bei BZ-Werten von ≥ 180 mg/dL (10 mmol/L) bei Sepsis oder septischem Schock
- Nierenersatztherapie
- keine Nierenersatztherapie bei Sepsis oder septischem Schock und akutem Nierenversagen ohne eindeutige Indikation für Nierenersatztherapie
- kontinuierliche oder intermittierende Nierenersatztherapie bei Sepsis oder septischem Schock und akutem Nierenversagen mit Indikation für Nierenersatztherapie
- Natriumbicarbonat
- keine Natriumbicarbonattherapie zur Verbesserung der Hämodynamik oder zur Reduzierung des Bedarfs an Vasopressoren bei septischem Schock und hypoperfusionsbedingter Laktatazidose
- Natriumbicarbonattherapie bei septischem Schock, schwerer metabolischer Azidose (pH ≤ 7,2) und akutem Nierenversagen (AKIN-Score 2 oder 3)
- Prophylaxe von venösen Thromboembolien
- medikamentöse Prophylaxe gegen venöse Thromboembolien (VTE) bei Sepsis oder septischem Schock, sofern keine Kontraindikation vorliegt
- Anwendung von niedermolekularem Heparin ggü. unfraktioniertem Heparin zur VTE-Prophylaxe bei Sepsis oder septischem Schock vorziehen
- alleinige Anwendung einer pharmakologischen VTE-Prophylaxe ggü. Kombination aus pharmakologischer und mechanischer VTE-Prophylaxe bei Sepsis oder septischem Schock vorziehen
Behandlungsziele
Gespräche über Behandlungsziele
- Behandlungsziele und Prognose mit Patient*innen und/oder deren Familien besprechen
- Behandlungsziele frühzeitig (innerhalb von 72 h) anstatt spät (> 72 h) besprechen
standardisierte Kriterien zur Auslösung von Gesprächen über Behandlungsziele
- unzureichende Belege für Empfehlung bzgl. der Verwendung eines spezifischen standardisierten Kriteriums zur Identifizierung von Patient*innen für Gespräche über Behandlungsziele
Patient*innenverfügung
- Strategien umsetzen, um sicherzustellen, dass Patient*innen, die nach Sepsis oder septischem Schock aus dem KH entlassen werden, die Möglichkeit haben, eine Patientenverfügung zu erlassen
- unzureichende Belege für Empfehlung bzgl. der systematischen Erstellung von Patientenverfügungen vor KH-Entlassung
zeitlich begrenzte Studien
- unzureichende Belege für Empfehlung bzgl. formal zeitlich begrenzter Therapieversuche auf der Intensivstation
- formal zeitlich begrenzter Therapieversuch = gemeinsamer Plan zur Anwendung lebenserhaltender Maßnahmen über einen festgelegten Zeitraum
Palliativpflege
- Grundsätze der Palliativmedizin (einschließlich einer palliativmedizinischen Beratung nach ärztlicher Beurteilung) ggf. in Behandlungsplan integrieren, um Symptome und Leiden der Patient*innen und ihrer Familie zu lindern
- keine routinemäßige formelle Palliativberatung für alle Patient*innen –> stattdessen Palliativberatung auf Grundlage der klinischen Beurteilung


Sei der Erste der einen Kommentar abgibt