veröffentlichende Fachgesellschaft: Österreichische Gesellschaft für Neurologie (ÖGN)
Klassifikation gemäß AWMF:
Datum der Veröffentlichung: 07.03.2024
Ablaufdatum:
Quelle/Quelllink: https://www.xn--gsf-rna.at/wp-content/uploads/2024/04/Positionspapier_OeGSF_Tenecteplase_Maerz2024.pdf
Grundsätzliches
- Tenecteplase = genetisch modifizierte Variante des gewebsspezifischen Plasminogen-Aktivators
- Tenecteplase führt über Aktivierung von Plasminogen zu Plasmin zur Aufspaltung von Fibrinstrukturen und schlussendlich zur Auflösung von Thromben
- längere HWZ der Tenecteplase macht nur eine alleinige Bolusgabe ohne anschließende Infusion notwendig (CAVE: Nachteil ist, dass es keine Möglichkeit der Unterbrechung der Therapie bei unerwünschten Nebenwirkungen gibt)
| Alteplase | Tenecteplase | |
|---|---|---|
| Halbwertszeit | 4 min | 20 min |
| Resistenz gegenüber Plasminogen- Aktivator-Inhibitor Typ 1 | niedrig | mittelgradig |
| Fibrinogen-Spezifität | mittelgradig | hoch |
| Fibrinogen-Depletion | mittelgradig | niedrig |
Empfehlungen
- Gabe von 0,25 mg/kgKG Tenecteplase (max. 25 mg) bei Patient*innen mit akutem ischämischen Schlaganfall, die im Zeitfenster von < 4,5 h nach Symptombeginn vorstellig werden
- Bevorzugung von 0,25 mg/kgKG Tenecteplase ggü. Alteplase bei Patient*innen mit akutem ischämischen Schlaganfall und nachgewiesenem proximalem Gefäßverschluss (A. carotis interna, M1- und M2-Segment der A. cerebri media, A. basilaris), die sich im Zeitfenster von < 4,5 h nach Symptombeginn mittels Thrombolyse befinden
- keine Empfehlung für Dosierung von 0,4 mg/kgKG Tenecteplase für die Akuttherapie des ischämischen Schlaganfalls (CAVE: potenziell höheres Blutungsrisiko)
- keine klare Empfehlung für 0,25 mg/kgKG Tenecteplase alternativ zur Alteplase bei spez. Patient*innengruppen wie Patient*innen mit Präsentation im erweiterten Zeitfenster von > 4,5 h, Patient*innen mit einem Wake-up Stroke und nachgewiesenem FLAIR-DWI-Mismatch und Patient*innen mit Minor Stroke (Studiendaten zeigen aber vergleichbaren Effektivität und Sicherheit)
- unzureichende Datenlage für Empfehlung bzgl. der Therapie von Patient*innen < 18 Jahren (CAVE: Alteplase ist für Patient*innen > 16 Jahren explizit zugelassen)
Kontraindikationen
- Symptome einer ischämischen Attacke, die mehr als 4,5 Stunden vor der Injektion einsetzten, oder Symptome, bei denen der Zeitpunkt des erstmaligen Auftretens unbekannt ist und mehr als 4,5 Stunden zurückliegen könnte
- akuter ischämischer Schlaganfall ohne einschränkende neurologische Defizite oder mit rascher Besserung der Symptome vor der Injektion
- schwerer Schlaganfall laut klinischer Beurteilung (z. B. NIHSS > 25) und/oder geeignetem bildgebendem Verfahren
- vorausgegangener Schlaganfall in den letzten 3 Monaten
- Patient*innen mit Vorgeschichte eines früheren Schlaganfalls und begleitendem Diabetes
- Krampfanfall bei Einsetzen des Schlaganfalls
- anamnestisch bekannte oder Verdacht auf intrakranielle Blutung
- Symptome, die eine Subarachnoidalblutung vermuten lassen, auch wenn der CT-Scan keine Auffälligkeiten zeigt
- bekannte hämorrhagische Diathese
- schwerwiegende Blutung (akut oder innerhalb der vergangenen 6 Monate)
- große Operation, Biopsie eines parenchymatösen Organs oder schweres Trauma in den letzten 2 Monaten
- kürzlich erlittene Kopf- oder Schädelverletzung
- länger andauernde Wiederbelebungsmaßnahmen (> 2 Minuten) in den letzten 2 Wochen
- Patient*innen mit wirksamer Antikoagulation (z. B. INR > 1,3)
- Gabe von Heparin in den vorangegangenen 48 Stunden und eine Thromboplastinzeit, die den oberen Labornormalwert überschreitet
- Thrombozytenzahl von weniger als 100.000/mm3
- schwere, nichtkontrollierbare arterielle Hypertonie
- Neoplasma mit erhöhtem Blutungsrisiko
- schwere Leberfunktionsstörung einschließlich Leberversagen, Zirrhose, Pfortaderhochdruck (Ösophagusvarizen) und aktive Hepatitis
- aktive peptische Ulzera
- arterielles Aneurysma und bekannte arteriovenöse Missbildungen systolischer Blutdruck > 185 mmHg oder diastolischer Blutdruck 110 mmHg, oder es ist eine forcierte Behandlung (intravenöse Pharmakotherapie) erforderlich, um den Blutdruck unter diese Werte zu senken
- jede Erkrankung des zentralen Nervensystems (z. B. Neoplasma, Aneurysma, intrakranielle oder intraspinale Operation) in der Anamnese
- akute Perikarditis und/oder subakute bakterielle Endokarditis
- akute Pankreatitis
- Blutzucker < 50 mg/dl oder > 400 mg/dl (< 2,8 mM oder > 22,2 mM)
Lyseprotokoll
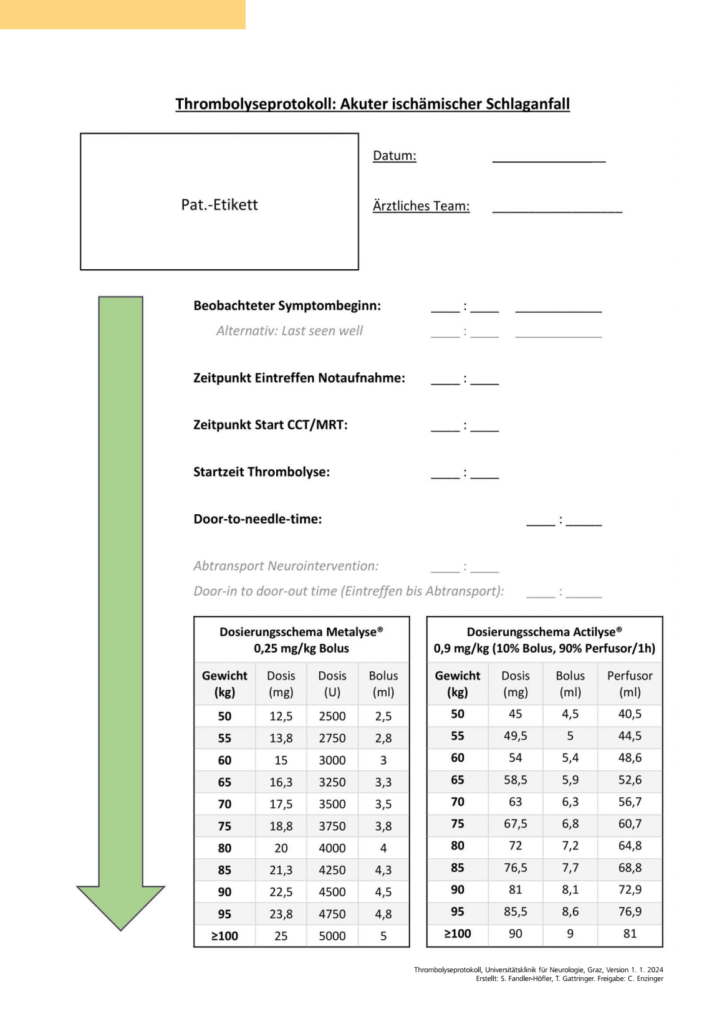

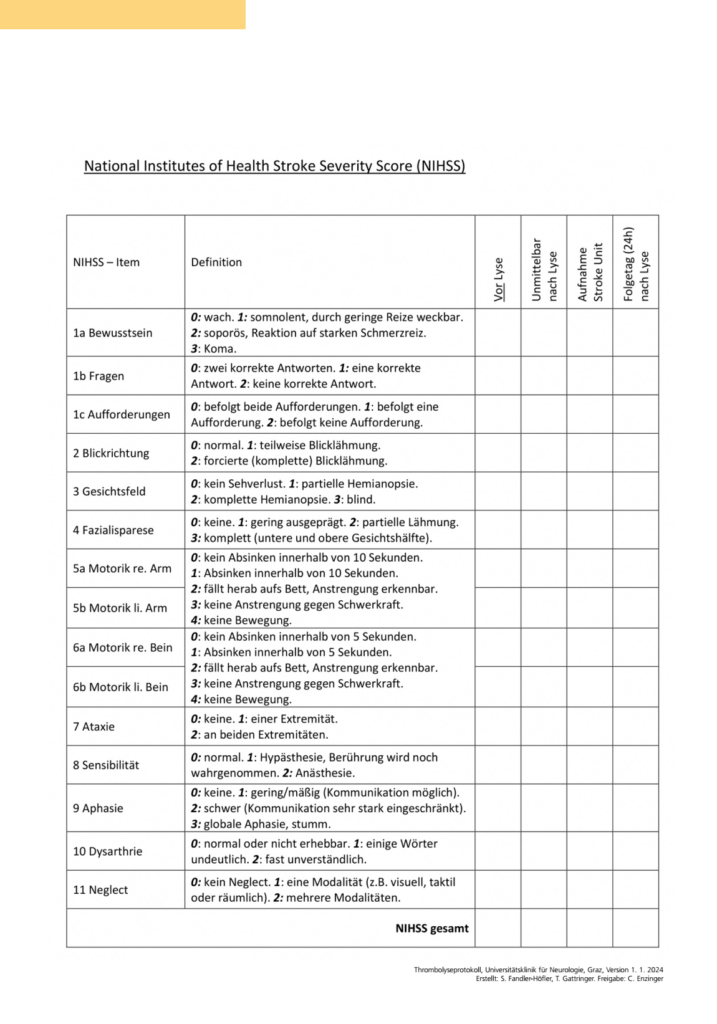



Sei der Erste der einen Kommentar abgibt