veröffentlichende Fachgesellschaft: Deutsche Gesellschaft für Pneumologie und Beatmungsmedizin (DGP)
Klassifikation gemäß AWMF: S2k
Datum der Veröffentlichung: 09.02.2026
Ablaufdatum: 08.02.2029
Quelle/Quelllink: https://register.awmf.org/de/leitlinien/detail/020-006
Diagnostik und Monitoring
- umfassende Anamnese bei COPD-Erstdiagnose, die auch versucht, die Ätiologie der Erkrankung zu erfassen
Aspekte der strukturierten Anamnese
– Exposition ggü. Tabakrauch, aktueller Raucherstatus, Art der
verwendeten Tabakprodukte, detaillierte Konsumanamnese zur Erfassung der
Belastung in Packungsjahren (“packyears“)
– Exposition ggü. diversen inhalativen Noxen, wie Arbeitsplatznoxen, Umweltnoxen, Biomasseexposition, oder auch Putz- und Reinigungsmitteln
– andere Risikofaktoren
– strukturierte Erfassung der Symptome, z.B. anhand des Chronic Airways Assessment Test CAAT™ (COPD Assessment-Test CAT™ und CAAT™ sind gleichwertig und die Ergebnisse sind untereinander austauschbar; alternativ die Modified Medical Research Council-Skala)
– Erfassung der B-Symptome Fieber, Nachtschweiß und Gewichtsverlust
– strukturierte Erfassung der Exazerbationsanamnese, z.B. mittels
des Monitoring of Exacerbation Probability (MEP)-Fragebogens
– Erfassung der Familienanamnese hinsichtlich relevanter Vorerkrankungen der
Lunge
– Erfassung der Frühgeburtlichkeit und gehäufter Infekte in der Kindheit als
potentieller Risikofaktor für eine COPD
– zur Erfassung der Differentialdiagnose bzw. eines komorbiden Asthma bronchiale sollten der Allergiestatus, eine Asthmadiagnose in der Kindheit und im frühen Erwachsenenalter, sowie relevante Komorbiditäten, wie beispielsweise Nasenpolypen, erfragt werden. Ferner sollten nächtliche oder saisonale Beschwerden, Ansprechen auf Kortikosteroide, Variabilität der Beschwerden sowie die Sputumproduktion erfasst werden
– Erfassung der medikamentösen Dauertherapie
– Erfassung des Impfstatus, insbesondere Pneumokokken, Influenza, RSV, COVID-19, Pertussis, Herpes Zoster
– Erfassung der Komorbiditäten
– spezifische Erfassung des kardiovaskulären Risikoprofils
– Erfassung der körperlichen Belastbarkeit und der aktuellen körperlichen Aktivität
- Arbeitsanamnese hinsichtlich irritativer Dämpfe, Gase, Stäube und Rauche bei allen Patient*innen mit einer COPD (z.B. retrospektiv, um begründeten V.a. Berufskrankheit nicht zu übersehen, und zum anderen prospektiv, um ungünstige Arbeitseinflüsse auf Krankheitsverlauf zu vermeiden)
- Messung der peripheren Sauerstoffsättigung bei V.a. COPD (kapilläre BGA vorrangig bei nachgewiesener peripherer Hypoxämie, V.a. Überlastung der Atemmuskelpumpe, sowie grundsätzlich bei höherem Schweregrad der COPD sinnvoll)
- Differentialblutbild bei V.a. COPD
- Messung des FeNO erwägen bei schwerer COPD oder COPD-Mischform mit Überlappung
- risikostratifiziert kardiovaskuläre Abklärung bei COPD-Erstdiagnose sowie im Verlauf
- CT-Thorax bei Diskrepanz zwischen Symptomatik und Lungenfunktion sowie bei häufigen Exazerbationen oder chronischer Mucusproduktion zur Differenzialdiagnostik
- konventionelle Thoraxröntgenaufnahme in zwei Ebenen oder natives low-dose CT-Thorax bei COPD-Erstdiagnostik
Schweregradeinteilung der COPD
- Symptomerfassung bei COPD soll die Inhalte validierter Fragebögen (CAAT, mMRC) enthalten
- Exazerbationshistorie anamnestisch erfassen –> strukturierte Erfassung (MEP-Fragebogen) sinnvoll und kann bei Identifikation von Exazerbationen helfen
- vierstufige COPD-Schweregradeinteilung (1 – 4) anhand spirometrischer FEV1-Werte in % des mittleren Sollwertes gemäß den GOLD-Kriterien von GOLD
- Symptomlast und Exazerbationshistorie zur Risikostratifizierung in drei Gruppen (A, B & E) unterteilen
Therapie
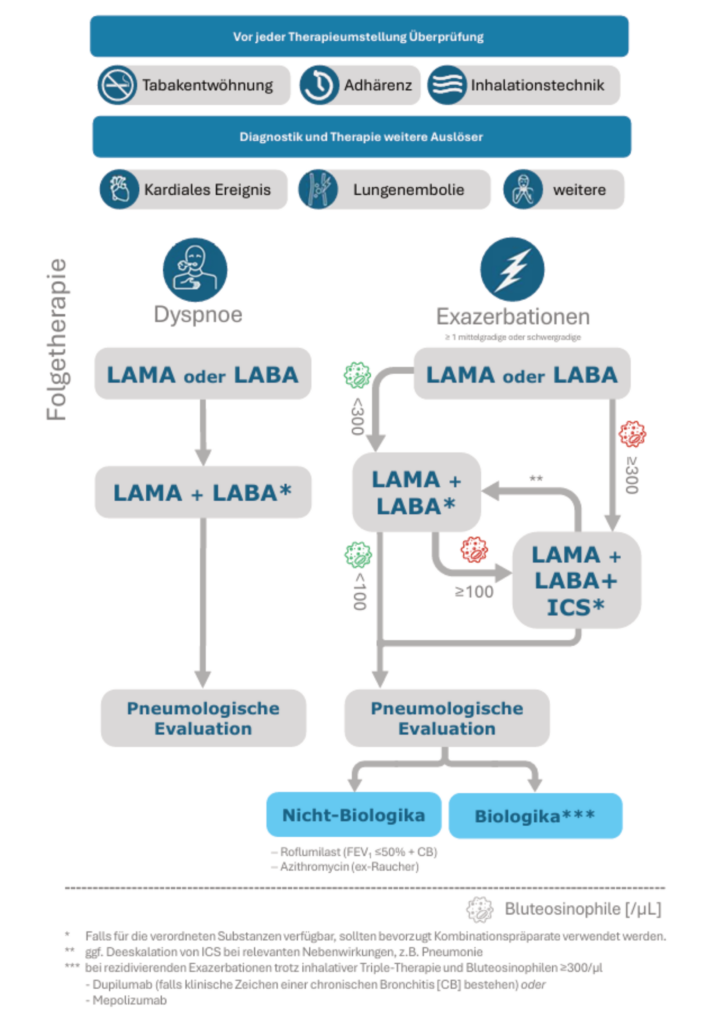
- fortbestehende Symptome trotz inhalativer Therapie
- bei fortbestehenden Symptomen unter Monotherapie mit langwirksamen Bronchodilatatoren (LAMA oder LABA) inhalative Therapie auf duale Bronchodilatation umstellen
- bei Patient*innen mit fortbestehenden Symptomen, die ICS/LABA-Therapie erhalten und bislang keine Exazerbationshistorie aufweisen, Wechsel auf LABA/LAMA-Kombinationstherapie
- fortbestehende Exazerbationen trotz inhalativer Therapie
- bei fortbestehenden Exazerbationen unter Monotherapie mit LAMA oder LABA und Bluteosinophilien < 300/µL Therapie auf duale Bronchodilatation (LAMA/LABA) eskalieren (CAVE: alleinige ICS/LABA-Kombinationstherapie bei COPD nicht empfohlen)
- bei fortbestehenden Exazerbationen unter dualer Bronchodilatation (LAMA/LABA) und Bluteosinophilen ≥ 100/µL inhalative Therapie auf Triple-Therapie (LAMA/LABA/ICS) eskalieren
- bei Verordnung einer inhalativen Triple-Therapie Kombinationspräparat (Single-Inhaler-Triple-Therapie, SITT) verordnen
akute COPD-Exazerbation und deren Management
- Definition „COPD-Exazerbation“: vermehrte Atemnot und/oder Husten und Auswurf, welche sich innerhalb 14 Tagen verschlechtert haben, ggf. begleitet von Tachypnoe und/oder Tachykardie
- Definition des Schweregrads der Exazerbation
- Klassifikation des Schweregrads einer COPD-Exazerbation weiterhin anhand der Inanspruchnahme medizinischer Versorgungsstrukturen in leichtgradig, mittelgradig, schwergradig und sehr schwer
- standardisierte Schweregradeinteilung bei stationärer Aufnahme
- arterielle/kapilläre Blutgasanalyse bei stationärer Aufnahme
Schweregradeinteilung
– leichtgradige Exazerbation: zusätzliche Gabe von kurzwirksamen Bronchodilatatoren, oft eigenständige Behandlung durch Patient:*innen selbst; häufig werden diese Informationen nicht an Behandelnde übermittelt
– mittelgradige Exazerbation: zusätzliche Therapie mit systemischen Glukokortikosteroiden und/oder Antibiotikum
– schwergradige Exazerbation: stationäre Behandlung
– sehr schwere Exazerbation: intensivmedizinische Behandlung erforderlich
- Indikationen für Eskalation der Behandlung (intensivmedizinische Überwachung)
- progredienter Hyperkapnie mit respiratorischer Azidose (pH <7,35)
- Kreislaufinsuffizienz
- engmaschige klinische Evaluation ist indiziert bei
- schwerer Dyspnoe, nicht korrigierbar durch Akuttherapie
- persistierender Hypoxämie (PaO₂ <55mmHg) trotz Sauerstoffgabe
- potentiell instabilen Komorbiditäten
- standardisierte Schweregradeinteilung der COPD-Exazerbation
| Schweregrad | Parameter |
|---|---|
| leichtgradig | – Atemnot VAS <5 – AF <24/min – HF <95/min – SpO2 in Ruhe und nativ (oder basierend auf der bestehenden Langzeitsauerstofftherapie) ≥ 92 % und Änderung ≤ 3 % wenn vorbekannt – CRP < 10 mg/L (wenn gemessen) – BGA falls durchgeführt: Hypoxämie (PaO2 < 60 mmHg) und/oder Hyperkapnie (PaCO2 45 mmHg) aber ohne Azidose |
| mittelgradig (mind. 3 von 5 Kriterien erfüllt) | – Atemnot VAS >5 – AF >24/min – HF >95/min – SpO2 <92 % in Ruhe und nativ (oder unter bestehender Langzeitsauerstofftherapie) < 92 % und/oder Änderung < 3 % wenn vorbekannt – CRP > 10 mg/L (wenn gemessen) – BGA falls durchgeführt: Hypoxämie (PaO2 < 60 mmHG) und/oder Hyperkapnie (PaCO2 45 mmHg) aber ohne Azidose |
| schwergradig | – Atemnot, AF, HF, SpO2 und CRP wie bei mittelgradig, – BGA zeigt jedoch Neuauftreten/Verschlechterung einer Hyperkapnie und Azidose (PaCO2 >45 mmHg und pH <7,35) |
- erweiterte diagnostische Abklärung bei schweren Exazerbationen im stationären Setting
| Diagnostik im stationären Setting | Befund | Konsequenz |
|---|---|---|
| Blutgasanalyse (obligat) | respiratorische Insuffizienz Typ I oder Typ II | Sauerstofftherapie, nicht-invasive Beatmung, invasive Beatmung |
| klinische Zeichen für LAE oder Wells-Score und/ oder D-Dimer | erhöhtes Risiko | CT-Thorax mit Pulmonalisangiographie |
| CRP-Wert | CRP > 50 mg/dL | antibiotische Therapie |
| Procalcitonin (optional) | PCT < 0,1 ng/mL (keine Antibiotika Therapie) PCT > 0,5 ng/mL (Antibiotika empfohlen) | klinische Einschätzung (Sepsis), keine Nutzung zur Steuerung der Antibiotikadauer |
| BNP/NT-proBNP | erhöht | Abklärung Herzinsuffizienz |
| Routinelaborparameter | großes Blutbild, Nierenwerte, Leberwerte, Elektrolyte, ggf. Gerinnungsstatus | Identifikation von relevanten Komorbiditäten bsp. Niereninsuffizienz, Endotyp der Exazerbation |
| klinische Zeichen für ACS und/oder Troponin-Erhöhung | erhöht | Abklärung ACS |
| EKG | Rhythmusstörungen, pathologische ST-Streckenveränderungen | Identifikation von relevanten Rhythmusstörungen oder kardialen Begleiterkrankungen |
| Echokardiographie (wenn mgl.) | V.a. kardiale Komorbidität | Identifikation von Vitien, Herzinsuffizienz, Rechtsherzbelastung, Perikarderguss |
| thorakale Bildgebung (Röntgen Thorax oder natives low-dose CT Thorax; CT als bevorzugtes Verfahren, falls verfügbar) | Infiltrate, Raumforderung, Pneumothorax, kardiopulmonale Stauung | Identifikation von Differentialdiagnosen Pneumonie, Pneumothorax, Lungenkarzinom etc. |
| Sputum | Erfassung Keimspektrum | resistenzgerechte antibiotische Therapie |
- medikamentöse Therapie der stationär behandelten COPD-Exazerbation
- SABA und SAMA entweder als Mono- oder als Kombinationstherapie in der Akuttherapie (Wahl des Inhalationssystems richtet sich nach klinischem Zustand; inhalative Dauertherapie fortführen und ggf. anpassen)
- 100 – 200 µg SABA initial über Dosieraerosol oder Pulverinhalator –> bei ausbleibender Besserung Gabe nach 10 – 15 min wiederholen
- SAMA wie Ipratropiumbromid (20 µg pro Sprühstoß; 2 – 4 Sprühstöße) oder in Dosierung von 250 – 500 µg über Vernebler
- 40 mg Prednisolon-Äquivalent oral für 5 Tage (morgendliche Gabe, 1x täglich) zur Behandlung der akuten COPD-Exazerbation (in Einzelfällen ggf. individuelle Verlängerung/höhere Dosierung notwendig)
- Antibiotika
- antibiotische Therapie bei CRP-Erhöhung (> 50 mg/dL) oder eindeutiger Sputumpurulenz
- antibiotische Therapie bei intensivmedizinischer Betreuung auch ohne Sputumpurulenz oder erhöhte Entzündungswerte bei hospitalisierten Patient*innen
- Therapiedauer sollte 5 – 7 Tage betragen
- SABA und SAMA entweder als Mono- oder als Kombinationstherapie in der Akuttherapie (Wahl des Inhalationssystems richtet sich nach klinischem Zustand; inhalative Dauertherapie fortführen und ggf. anpassen)


Sei der Erste der einen Kommentar abgibt