veröffentlichende Fachgesellschaft: European Society of Cardiology (ESC)
Klassifikation gemäß AWMF:
Datum der Veröffentlichung: 27.09.2025
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.1093/ehjacc/zuaf125
Grundsätzliches
- Definition „Hypotonie nach Herzstillstand“: RRsys < 90 mmHg oder MAD < 65 mmHg
- wenn Hypotonie mit Anzeichen und Symptomen einer Organhypoperfusion einhergeht, kann Aufrechterhaltung eines adäquaten RR entscheidend sein, um die Organperfusion zu optimieren, die neurologische Erholung zu unterstützen und das Risiko eines Multiorganversagens nach OHCA zu reduzieren
- primäre Ursache des OHCA ist kardiale Ursache, wobei die ischämische Herzkrankheit in bis zu 70 % aller Fälle häufiger Auslöser plötzlicher Herzrhythmusstörungen ist
- OHCA-Inzidenz in Europa bei jährlich zw. 67 – 170 Fällen pro 100.000 Einwohner*innen
Pathophysiologie des Post-Reanimations-Syndroms
- Krankenhaussterblichkeit nach OHCA resultiert häufig aus systemischen Folgen einer Ganzkörperischämie vor Reperfusion bei ROSC
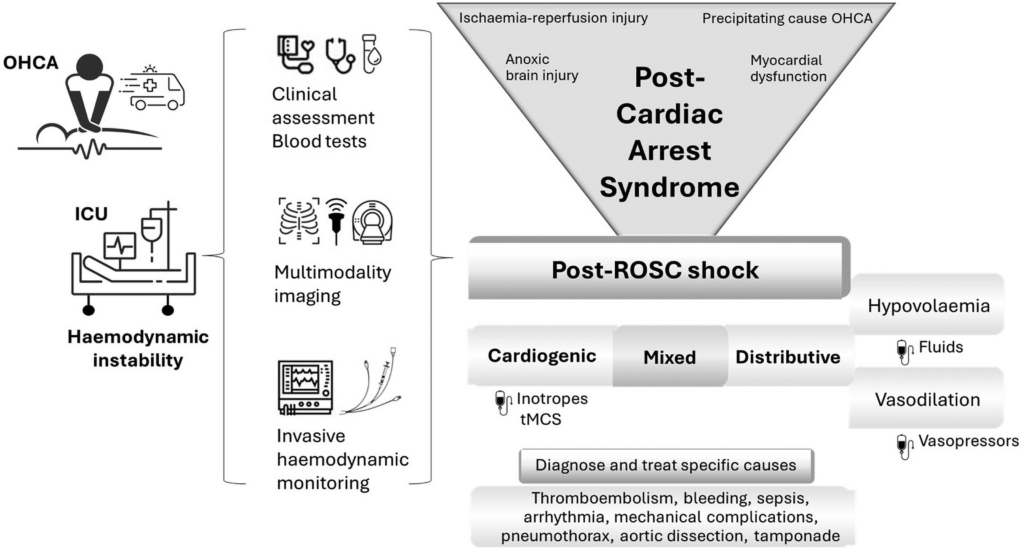
- Post-Reanimations-Syndrom ist komplexes Krankheitsbild, das eine oder mehrere, der nachfolgenden Komponenten umfasst:
- Multiorgan-Ischämie/Reperfusionsschädigung
- Myokarddysfunktion
- anoxische Hirnschädigung
- OHCA-auslösenden Pathologie
- Reperfusion nach prolongierter Ischämie induziert oxidativen Stress, Endotheldysfunktion und systemische Entzündungsreaktion, die mehrere Organsysteme betrifft
- Effekte können zu sepsisähnlichen hämodynamischen Zuständen und in manchen Fällen zu vasodilatatorischem Schock mit Multiorganversagen führen
- Myokarddysfunktion wird in 70 % der Fälle nach OHCA beobachtet und manifestiert sich häufig als reduzierte LVEF oder biventrikuläre Dysfunktion aufgrund von Myokardstuning, ischämischer Herzkrankheit sowie myokardial-toxischen Wirkungen eines Zytokinsturms
- Hypoxisch-ischämische Hirnschäden, sekundäre Hirnschäden und Dysregulation der zerebralen Perfusion sind weiterhin die Hauptursachen für Morbidität und MortalitätHypotonie und Hypoperfusion nach OHCA
Hypotonie und Hypoperfusion nach OHCA
- ausreichende systemische Sauerstoffversorgung zeichnet sich durch ausreichenden Blutdruck, ausreichende Durchblutung und ausreichenden Sauerstoffgehalt im Blut sowie eine ausreichende Sauerstoffaufnahme aus dem Blut in die Gewebe aus
- Minderdurchblutung –> Organfunktionsstörung (Schock nach OHCA)
- HZV und RR alleine nicht ausreichend als Marker für die Sauerstoffversorgung und Gewerbeperfusion
- Unterteilung der Hypotonie nach OHCA anhand des hämodynamischen Profils
- Hypotonie mit niedrigen Füllungsdrücken (verursacht durch niedrigen systemischen Gefäßwiderstand oder Hypovolämie)
- Hypotonie aufgrund primärer Herzfunktionsstörung (in schweren Fällen ggf. kardiogener Schock)
- niedriger systemischer Gefäßwiderstand (in schweren Fällen ggf. vasodilatatorischer Schock)
- gemischte hämodynamische Zustände
- generelle Anstrebung von höherem MAD mit vasoaktiven Substanzen scheint nicht ausreichend, um Behandlungsergebnisse zu verbessern
- individualisierte hämodynamische Zielwerte in der Phase nach OHCA, da standardisierter Ansatz an Grenzen stößt
individuelles Management
- Pathophysiologie der Post-OHCA-Hypotonie zeigt, dass niedriger RR allein kein zuverlässiger Marker für unzureichende Perfusion ist und höherer MAD-Zielwerte in Kombination mit Katecholaminen das Outcome nicht durchgängig verbessern
- Annahme, dass protokollierte Steigerung des MAD unwirksam und potenziell schädlich ist, während individualisiertes Management bis zum Abschluss zukünftiger, ausreichend aussagekräftiger klinischer Studien potenziell physiologisch gerechtfertigt und klinisch notwendig bleibt
Ursachen von Hypotonie und Hypoperfusion nach OHCA
- Ursachen, Diagnostik und Management der post-OHCA-Hypotonie
| Ursache | Diagnostik | mgl. Therapien |
|---|---|---|
| niedrige Füllungsdrücke (z.B. Blutung, Hypovolämie, Sepsis) | klinische Beurteilung, Echokardiographie, ZVD-Überwachung, Laktatwerte | Flüssigkeit i.v., Bluttransfusion, chirurgischer Eingriff, Vasopressoren, Antibiotika bei Sepsis |
| Hypotonie ohne Hypoperfusion (z.B. durch Sedierung, Temperaturkontrolle, Antihypertensiva) | klinische Beurteilung, Echokardiographie, Überprüfung der Sedierung, Temperaturmanagementprotokolle | Beobachtung, Anpassung der Sedierung, Normothermieprotokoll |
| kardiogener Schock (z.B. Myokarddysfunktion, Myokardbetäubung) | klinische Beurteilung, Echokardiographie, Laktatwerte, Pulmonalarterienkatheter, nicht-invasive HZV-Messung, kardiale Biomarker | Inotropika, Vasopressoren, mechanische Kreislaufunterstützung |
| vasodilatorischer Schock (z.B. systemische Entzündungsreaktion, Sepsis) | Messung des systemischen Gefäßwiderstands, Echokardiographie | Vasopressoren (Noradrenalin, Vasopressin), entzündungshemmende Mittel (in Erprobung), Methylenblau |
| gemischter Schock (z.B. Kombi aus kardiogenem und vasodilatorischem Schock) | Echokardiographie, Pulmonalarterienkatheter, gemischtvenöse SpO2 | Kombination aus Inotropika, Vasopressoren & mechanischer Kreislaufunterstützung |
- klinische Beurteilung
- Überwachung der Vitalfunktionen
- HF: Kontinuierliche Überwachung bzgl. Tachy-/Bradykardie, die auf zugrunde liegende Herzfunktionsstörung hinweisen können
- RR: regelmäßige oder kontinuierliche Messung über invasive arterielle Zugang
- AF: Überwacht wird auf Anzeichen von Atemnot, Tachypnoe oder abnormale Atemmuster
- SpO2: Gewährleistung einer ausreichenden Sauerstoffversorgung des Gewebes
- Temperatur: Überwachung auf Unterkühlung (häufig bei therapeutischer Kühlung) oder Fieber (Hinweis auf Infektion oder Entzündung)
- Herz-Kreislauf-Status
- körperliche Untersuchung: Abhören der Herztöne, Erkennen von Herzgeräuschen und Beurteilung des peripheren Pulses
- Rekap-Zeit: schneller Indikator für Kreislaufstatus und Durchblutung
- Hautbeurteilung: Überprüfung auf Anzeichen mangelhafter Durchblutung (z. B. Marmorierung, kalte oder feuchte Haut)
- Jugularvenendruck: Indikator für Flüssigkeitsüberladung oder Herzinsuffizienz
- Ödeme: Vorliegen peripherer oder pulmonaler Ödeme als Hinweis auf Herzinsuffizienz oder Flüssigkeitsüberladung
- Atmungssystem
- körperliche Untersuchung: Auskultation der Lunge bzgl. Rasselgeräuschen, Keuchen oder fehlenden Atemgeräuschen als Hinweis auf Pneumonie, Lungenödem oder Pneumothorax
- neurologischer Status
- Bewusstsein: anhand von Instrumenten wie GCS, um Gehirnfunktion zu bewerten, v.a. bei komatösen Patient*innen nach OHCA
- Pupillenreaktion: Prüfung, um Hirnstammfunktionen zu beurteilen
- motorische Reaktion: Beobachtung spontaner Bewegungen, Körperhaltungen oder Reaktionen auf Reize
- Flüssigkeitshaushalt und Nierenfunktion
- Urinausscheidung: wichtiger Indikator für Nierendurchblutung und gesamten Flüssigkeitshaushalt (Zielwert: ≥ 0,5 mL/kg/h)
- Flüssigkeitshaushalt: regelmäßige Überprüfung der Flüssigkeitsaufnahme und -ausscheidung, um Über- oder Unterhydratation zu vermeiden
- Überwachung der Vitalfunktionen
kardiogener Schock nach OHCA
- kardiogener Schock: Syndrom schwerer Myokarddysfunktion, das trotz normalem oder erhöhtem Füllungsdruck zu vermindertem HZV, unzureichender Gewebedurchblutung und Organversagen führt
- kardiogener Schock nach OHCA assoziiert mit 1-Wochen-Mortalität von 50 – 70 %
- entsteht typischerweise durch akuten Myokardinfarkt, Myokardstunning oder Verschlechterung einer bestehenden Myokard- oder strukturellen Herzerkrankung
- Hyperlaktatämie in diesem Zusammenhang durch verschiedene Faktoren bedingt, z.B. Stresshyperglykämie infolge sympathischer Aktivierung und Katecholaminanstieg (endogen oder exogen) sowie verminderte Clearance
vasodilatatorischer Schock (distributiver Schock)
- generalisierte Vasodilatation (Vasoplegie) trotz normalem oder erhöhtem HZV –> unzureichende Perfusionsdruck
- Vasoplegie häufig Folge des Ischämie-Reperfusions-Syndroms
- echte Sepsis, die nach OHCA klinisch relevante Infektionen hervorruft, kann auch zum hämodynamischen Profil beitragen
Hypovolämie
- aufgrund der Befürchtung negativer Folgen einer Flüssigkeitsüberladung bei Patient*innen mit potenzieller Myokarddysfunktion wird Hypovolämie ggf. unterbehandelt
- Vasoplegie der Kapazitätsgefäße, Kapillarlecksyndrom im Zusammenhang mit verlängerter Reanimation vor ROSC und/oder extrakorporale Verfahren sowie in der Spätphase Sepsis, Darmschädigung, Ileus und ggf. Blutungen –> niedriger Venendruck
gemischter Schock
- gemischter Schock nach OHCA häufig, gekennzeichnet durch Elemente eines kardiogenen, hypovolämischen und/oder vasodilatatorischen Schocks
- niedriges HZV, systemische Vasodilatation und Anzeichen einer Hypoperfusion trotz ausreichendem intravaskulärem Volumen
- Behandlung des gemischten Schocks erfordert umfassendes Verständnis der zugrunde liegenden Pathophysiologie
- Thromboembolien vor oder nach OHCA umfassen LAE und akuten Myokardinfarkt, die beide OHCA-Ursache sind und sich nachfolgend entwickeln können
- bei ungeklärter Hypotonie Thromboembolie in Betracht ziehen
Identifizierung der Hypotonie-Ursachen
- Identifizierung der zugrunde liegenden Ursachen einer Hypotonie nach OHCA ist für effektive Behandlung unerlässlich
| klinische Beurteilung | EKG | Biomarker | Echokardiographie | nicht-kardiale Ultraschalluntersuchung | Pulmonalarterienkatheter | Radiologie | |
|---|---|---|---|---|---|---|---|
| Zweck | Beurteilung klinischer Anzeichen einer Hypoperfusion sowie Überprüfung von Vitalfunktionen, Atmung, Bewusstsein und Flüssigkeitshaushalt | Diagnostizierung von Tachy- oder Bradyarrhythmien sowie Anzeichen von Myokardischämie und QT-Verlängerung | Organfunktionsstörungen, Anzeichen einer Minderdurchblutung (Laktat) und Beurteilung von Myokardschädigung | Beurteilung der Herzfunktion und Komplikationen | Beurteilung des Volumenstatus und der B-Linien der Lunge | Hämodynamik & HZV überwachen | mögliche Lungenpathologien identifizieren |
| Vorteile | schnell, direkt am Krankenbett und kostengünstig | schnell, direkt am Krankenbett und kostengünstig | Einblick in Organschäden | detaillierte Herzuntersuchung | nicht-invasiv und wiederholbar | Lieferung präziser hämodynamischer Daten | detaillierte strukturelle Bildgebung |
| Nachteile bzw. Komplikationen | subjektiv (für einige klinische Parameter) | keine | weniger spezifisch, beeinflusst von vielen Faktore | Fachkenntnisse erforderlich, ggf. nicht verfügbar | bediener*innenabhängig | invasiv mit Komplikationsrisiko | ggf. Transport erforderlich |
| Ergebnisse | Vitalzeichen, kardiovaskulärer Status (Herzgeräusche, Herzgeräusche, periphere Pulse, Rekap-Zeit, Hautbeurteilung, Jugularvenendruck, Ödeme), respiratorische Befunde (Auskultation der Lunge auf Rasselgeräusche, Giemen), neurologischer Status (Bewusstseinszustand, Pupillenreaktion, motorische Reaktion), Flüssigkeitsstatus (Ödeme, Hautturgor, Urinausscheidung, Flüssigkeitsbilanz) | Herzrhythmusstörungen oder Anzeichen einer Ischämie | Troponine, NT-proBNP, Laktat | LV/RV-Funktion, Erguss, Füllungsdrücke, Komplikationen | Durchmesser der Blutgefäße, Lungenstauung, Pleuraerguss oder innere Blutungen | HZV, Lungendrücke | Pneumonie, Pneumothorax, Ergüsse |
| Verwendung | schnelle Erstbeurteilung, kontinuierliche Überwachung der Vitalfunktionen, kardiovaskuläre, respiratorische und neurologische Beurteilung, Flüssigkeitsmanagement | erste Beurteilung vor KH-Einlieferung und Wiederholung bei Anzeichen einer Myokardischämie oder von Herzrhythmusstörungen | Beurteilung von Myokardschädigung, Therapiesteuerung | detaillierte Beurteilung der kardiovaskulären Ursachen | Volumenreagibilität, Flüssigkeitsüberladung | komplexe Hypotonie mit unklarer Ätiologie | Verdacht auf pulmonale Komplikationen |
| Verfügbarkeit | weitgehend verfügbar | weitgehend verfügbar | in den meisten Zentren leicht verfügbar | auf ITS verfügbar | i.d.R. auf ITS verfügbar | beschränkt auf erfahrene Zentren | ggf. Transport erforderlich |
Herzrhythmusstörungen nach Herzstillstand
- ventrikuläre Arrhythmien –> hämodynamischen Kollaps oder Herzstillstand mit Defibrillation
- Vorhofflimmern –> beeinträchtigte ventrikuläre Füllung und verringertes HZV –> ggf. elektrische Kardioversion
- erhöhter Vagotonus, Hypothermie, Elektrolytstörungen, Medikamente, Toxine oder intrinsische Reizleitungsstörungen –> Bradyarrhythmien
hämodynamische Behandlungsziele nach OHCA
- wichtigste hämodynamische Zielwerte
- Flüssigkeitstherapie
- Eckpfeiler der Behandlung von Hypotonie bei OHCA mit gleichzeitiger Hypovolämie
- Gabe von Kristalloiden als Mittel der 1. Wahl
- Flüssigkeitsüberladung unbedingt vermeiden
- individuelle Flüssigkeitstherapie basierend auf klinischer Beurteilung, ZVD und echokardiografischen Befunden
- Vasopressoren-Auswahl
- Noradrenalin als Mittel der 1. Wahl
- CAVE: Dopamin hat erhöhtes Risiko für Herzrhythmusstörungen
- Evidenzlage insgesamt gering für Empfehlung eines bestimmten Vasopressors
- Inotropika und Perfusionsziele
- Dobutamin oder Milrinon zur Verbesserung der myokardialen Kontraktilität und zur Steigerung des HZV bei kardiogenem Schock
- inotrope Unterstützung zur Verbesserung der Gewebedurchblutung unerlässlich bei unzureichendem HZV trotz adäquater Volumensubstitution und Anzeichen einer fortbestehenden Hypoperfusion wie erhöhte Laktatwerte
- Revaskularisierung
- bei Patient*innen mit primär ischämischer Ursache des Herzstillstands von entscheidender Bedeutung
- erfordert häufig notfallmäßige Koronarangiographie und perkutane Koronarintervention
- frühzeitige Erkennung und Behandlung von Koronarverschlüssen kann Prognose durch Wiederherstellung der Myokardperfusion und Reduzierung der Infarktgröße deutlich verbessern
- kein Überlebensvorteil durch Priorisierung der akuten Angiographie bei stabilisierten post-OHCA-Patient*innen ohne STEMI-Anzeichen
- Lungenembolie
- Behandlung mit Antikoagulanzien
- Thrombolyse, chirurgische Embolektomie oder interventionelle Verfahren wie Katheterbehandlungen bei massiver Embolie mit hämodynamischer Instabilität und obstruktivem Schock erwägen
mechanische Kreislaufunterstützung
- kurzfristige mechanische Kreislaufunterstützung (z.B. mittels mikroaxialer Flusspumpe oder veno-arterieller extrakorporaler Membranoxygenierung [VA-ECMO]) bei Nicht-Ansprechen auf medikamentöse Therapien
- VA-ECMO einer mikroaxialen Flusspumpe vorziehen, die nur linken Ventrikel unterstützt
- VA-ECMO ist auch Behandlungsoption, wenn ROSC nicht erreicht werden kann (eCPR)
- beim kardiogenen Schocks erhöht VA-ECMO die myokardiale Nachlast –> Verschlimmerung der ischämischen Schädigung
- Entscheidung für VA-ECMO erfordert sorgfältige Patient*innenauswahl unter Berücksichtigung der Behandlungsziele und Gesamtprognose (multidisziplinäre Entscheidungsfindung)
Management von Herzrhythmusstörungen
- Tachyarrhythmien
- sofortige Defibrillation und/oder Gabe von Antiarrhythmika wie Amiodaron oder Lidocain
- Einsatz von Overdrive-Pacing, Katheterablation oder Ganglion-stellatum-Blockade bei rezidivierenden, therapierefraktären ventrikulären Arrhythmien in hochspezialisierten Zentren
- Bradyarrhythmien
- temporäre transvenöse Stimulation und chronotrope Substanzen wie Adrenalin
- Sinusbradykardie = gutartiges Phänomen mit günstiger Prognose
- weiterführende elektrophysiologische Überwachung und Konsultation von Spezialist*innen für kardiale Elektrophysiologie bei rezidivierenden oder therapieresistenten Arrhythmien


Sei der Erste der einen Kommentar abgibt