veröffentlichende Fachgesellschaft: Deutsche Gesellschaft für Hygiene und Mikrobiologie e.V. (DGHM)
Klassifikation gemäß AWMF: S3
Datum der Veröffentlichung: 31.10.2025
Ablaufdatum: 30.10.2030
Quelle/Quelllink: https://register.awmf.org/de/leitlinien/detail/067-011
allgemeine Empfehlungen und mikrobiologische Diagnostik
- Einsatz von jeweils zwei Verfahren (inkl. orientierender oder bestätigender Verfahren) zur Erregeridentifizierung und zur Bestimmung der den MRE-Status bestimmenden Resistenzen bei erstmaliger Charakterisierung eines von Patient*innen gewonnenen Isolats mit V.a. Multiresistenz während eines stationären Aufenthaltes
- Labororganisation und Verfahren in der mikrobiologischen Diagnostik, inkl. prä- und postanalytischer Prozesse, bei schweren MRE-Infektionen so gestalten, dass die Zeitdauer von der Gewinnung des Untersuchungsmaterials bis zur (vorläufigen) Befundmitteilung möglichst kurzgehalten wird
- bei V.a. schwere MRE-Infektion kann mikrobiologische Schnelldiagnostik direkt aus dem Untersuchungsmaterial (Blut, Liquor) mit Nukleinsäure-basierten Testmethoden erwogen werden
- Bestimmung des Resistenzmechanismus, mind. aber Nachweis/Ausschluss von Metallo-b-Laktamasen und ggf. der nachgewiesenen Carbapenemasen bei schweren MRE-Infektionen durch gramnegative Bakterien
gramnegative Bakterien
Carbapenem-resistente Enterobacterales (CRE)
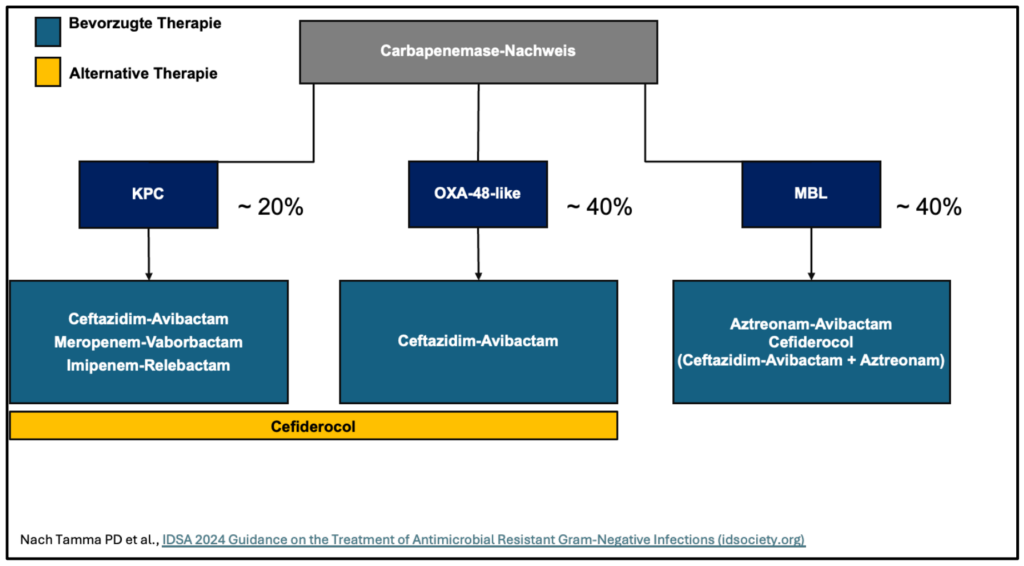
- gezielte Therapie von schweren Infektionen durch CRE immer basierend auf Antibiogramm und unter Berücksichtigung des Resistenzmechanismus
- schwere Infektionen durch CRE sollten unter Berücksichtigung des Antibiogramms mit folgenden Medikamenten behandelt werden:
- 1. Wahl: Ceftazidim-Avibactam, Meropenem-Vaborbactam oder Imipenem-Relebactam sofern keine MBL nachgewiesen wurde (alternativ bei Resistenz ggü. der 1. Wahl oder Nachweis einer MBL: Cefiderocol oder Aztreonam-Avibactam)
- Behandlung mit Eravacyclin oder Tigecyclin bei Patient*innen mit schweren intraabdominellen Infektionen erwägen
- begrenzte Datenlage bzgl. der Behandlung von Infektionen durch CRE, die keine Carbapenemase exprimieren –> in Abhängigkeit des Antibiogramms dieselben Therapien einsetzen, die bei Vorliegen von CRE mit Expression einer Carbapenemase genutzt werden
Pseudomonas aeruginosa mit schwer zu therapierender Resistenz (Difficult-to-Treat Resistance; Difficult-to-Treat -P. aeruginosa)
- nachfolgende kombinierte Diagnostikstrategie empfohlen
- molekulare Diagnostik (z. B. PCR-basierte Carba-R-Assays oder Whole-Genome Sequencing) –> ermöglicht raschen Nachweis spezifischer Carbapenemasen (z. B. KPC, VIM, NDM), erlaubt aber meist keine Aussage über Porin- oder Efflux-vermittelte Resistenzen
- phänotypische Empfindlichkeitstestung –> entscheidend, um die tatsächliche in vitro- Wirksamkeit aller therapeutisch relevanten Reserveantibiotika zu beurteilen
- Definition „schwere Infektionen Difficult-to-Treat -P. aeruginosa“
- Sepsis und septischer Schock (gemäß Sepsis-3-Kriterien)
- Blutstrominfektionen (BSI) mit systemischer Entzündungsreaktion
- nosokomiale Pneumonien, insbesondere beatmungsassoziierte Pneumonien (VAP)
- komplizierte Harnwegsinfektionen (cUTI) mit systemischen Symptomen
- intraabdominelle Infektionen (cIAI) mit Peritonitis oder Abszessbildung
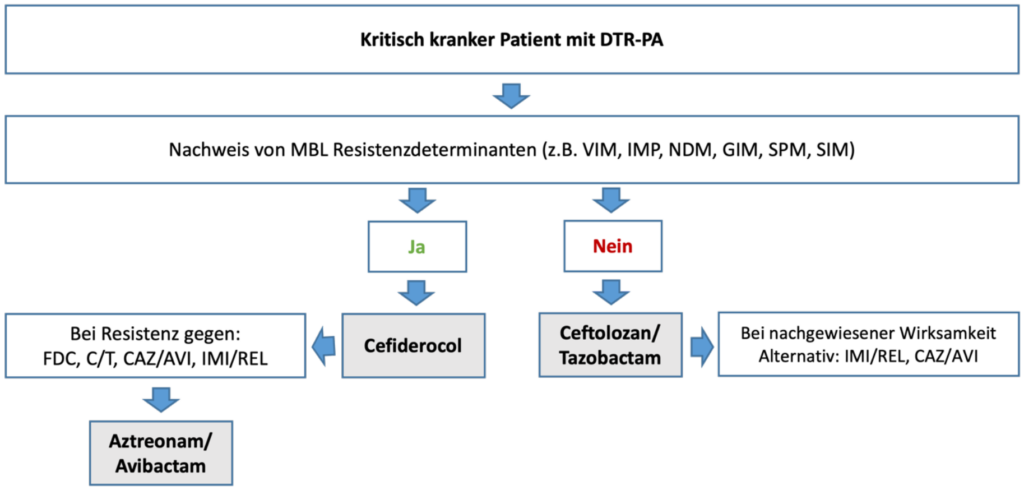
- bei nachgewiesener Empfindlichkeit sind folgende Substanzen für die Behandlung von schweren DTR-PA Infektionen geeignet: Ceftolozan-Tazobactam, Ceftazidim-Avibactam, Imipenem-Relebactam, Cefiderocol
- unter Berücksichtigung von Antimicrobial Stewardship Aspekten Ceftolozan-Tazobactam bevorzugen
- Cefiderocol für die Therapie von Infektionen mit Nachweis von Metallo-β-Laktamasen vorbehalten
- wenn Ceftolozan-Tazobactam, Ceftazidim-Avibactam, Imipenem-Relebactam und Cefiderocol nicht wirksam –> Aztreonam in Kombination mit Avibactam erwägen (folgende Aspekte berücksichtigen: MHK-Wert von Aztreonam-Avibactam, Dosierungsmöglichkeiten, Toxizität und angenommene Wirksamkeit älterer Substanzen)
Carbapenem-resistente Acinetobacter baumannii
- schwere Infektionen durch A. baumannii mit Cefiderocol therapieren
- Sulbactam-Durlobactam hat derzeit keine Europäische Zulassung (wenn verfügbar, in Kombination mit Carbapenem, als Alternative zu Cefiderocol einsetzen)
- wenn medizinische/mikrobiologische Gründe gegen die Verwendung von Cefiderocol oder Sulbactam-Durlobactam bestehen, kann Sulbactam mit einer der folgenden Substanzen kombiniert eingesetzt werden: Levofloxacin bei vorliegender Empfindlichkeit, alternativ Tigecyclin bei niedriger MHK, oder Colistin bei vorliegender Empfindlichkeit (falls keine dieser Substanzen einsetzbar –> Co-Trimoxazol in Monotherapie verabreichen, falls dieses sensibel getestet ist)
- vor Cefiderocol-Einsatz Empfindlichkeitstest durchführen –> wenn Verwendung von Cefiderocol oder Sulbactam-Durlobactam angestrebt, Bestimmung der Carbapenemase (Empfindlichkeitstestung von Colistin mit Referenzverfahren)
grampositive Bakterien
Methicillin/Oxacillin-resistente Staphylococcus aureus (MR/MRSA)
- Daptomycin oder Vancomycin i.v. als 1. Wahl für die Behandlung von MRSA-Blutstrominfektionen (Auswahl des Antibiotikums soll sich nach Infektionsfokus und
Nephrotoxizitätsrisiko richten) - wenn Daptomycin und Vancomycin kontraindiziert –> Teicoplanin, Linezolid oder Ceftobiprol für Blutstrominfektionen durch MRSA
- Daptomycin oder Vancomycin i.v. als 1. Wahl für durch MRSA verursachte Endokarditis
- bei einer durch MRSA verursachten Kunstklappen-Endokarditis oder sonstigem intrakardialen Fremdmaterial zusätzlich Kombination mit Fosfomycin oder Rifampicin zu Daptomycin oder Vancomycin erwägen
- Linezolid oder Vancomycin (initial i.v.) bei einer durch MRSA verursachten Pneumonie (Wahl des Antibiotikums entsprechend dem Toxizitätsrisiko und der Co-Medikation)
- initial Daptomycin, Linezolid oder Vancomycin bei Knochen- und Gelenkinfektionen ohne Fremdmaterialbeteiligung durch MRSA
- Kombinationstherapie mit Fosfomycin oder Rifampicin bei Infektionen von Fremdkörpern in Knochen und Gelenken durch MRSA erwägen
- Linezolid oder Daptomycin für komplizierte Haut- und Weichgewebeinfektionen durch MRSA bei in vitro-Empfindlichkeit (bei in vitro-Empfindlichkeit mit Tedizolid, Ceftarolin bzw. Ceftobiprol oder Delafloxacin therapieren; alternativ mit Vancomycin bzw. Teicoplanin plus Kombinationspartner, z.B. Rifampicin oder Fosfomycin, therapieren)
- Linezolid, TrimethoprimSulfamethoxazol (Cotrimoxazol), Doxycyclin, Moxifloxacin oder Levofloxacin zur oralen Sequenztherapie bei schweren Infektionen durch MRSA sind bei nachgewiesener in vitro-Empfindlichkeit (Delafloxacin prinzipiell ebenfalls geeignet)
- Sequenztherapie mit langwirkenden Lipoglykopeptiden (Dalbavancin oder Oritavancin) bei komplizierten Haut-Weichgewebe-Infektionen durch MRSA
vancomycinresistente Enterokokken
- Behandlung mit Linezolid oder Daptomycin bei Patient*innen mit Blutstrominfektionen (BSI) durch Vancomycinresistente Enterokokken (VRE-BSI; bei Daptomycin-Einsatz höhere Dosis (10 – 12 mg/kg/d) geben; kein Daptomycin bei einer durch Boulliondilution bestimmten MHK > 2 mg/L)
- keinTigeyclin oder Eravacyclin wegen unzureichender Wirkspiegel bei Blutstrominfektionen
- keine Empfehlung für Teicoplanin und Dalbavancin bei VRE-BSI aufgrund fehlender Evidenz
- Therapie mit Tigecyclin, Eravacyclin oder Linezolid (in Kombination mit geeignetem Partner) bei Patient*innen mit intraabdominellen Infektionen unter Beteiligung Vancomycin-resistenter Enterokokken erwägen


Sei der Erste der einen Kommentar abgibt