veröffentlichende Fachgesellschaft: American Heart Association (AHA)
Klassifikation gemäß AWMF:
Datum der Veröffentlichung: 18.09.2023
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.1161/CIR.0000000000001161
Benzodiazepine
- Behandlung von Angstzuständen, Schlaflosigkeit, Krampfanfällen und Entzugssyndromen sowie Bestandteil von Allgemeinanästhesien und Sedierungsverfahren
- an großer Zahl von Vergiftungsfällen beteiligt, i.d.R. kombiniert mit Opioiden oder Alkohol
- Überdosierung verursacht ZNS-Depression durch agonistische Wirkungen am GABA-A (Gamma-Aminobuttersäure-A)-Rezeptor, Folge davon ist Beeinträchtigung der Atmung durch Verlust der Schutzreflexe sowie Hypoxämie und Hyperkarbidämie –> Tod
- Antidot ist Flumazenil (kompetitiver Antagonist an der Benzodiazepin-Bindungsstelle am GABA-A-Rezeptor), welches die Benzodiazepin-vermittelte Unterdrückung des Sympathikustonus auf
- ggf. Gefahr von Krampfanfällen bei Gabe von Flumazenil bei Patient*innen mit vorbestehenden Anfallsleiden
- isolierte Benzodiazepin-Intoxikation führt nur selten zu lebensbedrohlicher Hypoventilation oder hämodynamischer Instabilität
Empfehlung
- bei kombinierte Opioid- & Benzodiazepin-Vergiftung initial Naloxon-Gabe zur Bekämpfung der Atemdepression
- keine Relevanz bei Herzstillstand im Zusammenhang mit Benzodiazepin-Vergiftung
- Flumazenil-Gabe bei Patient*innen mit erhöhtem Krampfrisiko oder Risiko für Herzrhythmusstörungen ggf. mit selbigen Folgen verbunden
β-Blocker
- β-Blocker sind mit hohem Letalitätsrisiko verbunden, v.a. mit Hypotonie aufgrund von Bradykardie und verminderter kardialer Kontraktilität
- Bradykardie ist auf direkte Wirkung auf den β1-adrenergen Rezeptor zurückzuführen
- Hypotonie, die kardiogen, vasodilatatorisch durch α1-adrenergen Rezeptorantagonismus oder multifaktoriell bedingt sein kann, ist häufig refraktär gegenüber einer vasopressorischen Therapie
- zur normalen Therapie gehören Atropin, Glukagon, Kalzium, Vasopressoren sowie hochdosiertes Insulin
Empfehlungen
- Gabe von Vasopressoren bei Hypotonie infolge β-Blocker-Vergiftung
- Gabe von hochdosiertem Insulin bei Hypotonie aufgrund β-Blocker-Vergiftung, die auf Therapie mit Vasopressoren refraktär ist (hochdosiertes Insulin verbessert Inotropie)
- Glucagon-Bolus, gefolgt von Dauerinfusion bei Bradykardie oder Hypotonie infolge β-Blocker-Vergiftung (Glucagon i.v. erhöht Kontraktilität und verbessert Hämodynamik)
- bei kardiogenem, therapeirefraktärem Schock, extrakorporale lebenserhaltende Maßnahmen wie VA-ECMO erwägen
- ggf. Gabe von Atropin bei β-Blocker-induzierter Bradykardie
- ggf. Pacing bei β-Blocker-induzierter Bradykardie (elektrische & mechanische Stimulation nicht immer erfolgreich und Hypotonie kann trotz mechanischer Stimulation fortbestehen)
- ggf. Hämodialyse bei lebensbedrohlicher Atenolol- oder Sotalol-Vergiftung
- keine Lipidemulsionstherapie i.v. bei lebensbedrohlicher β-Blocker-Vergiftung
Kalziumkanal-Blocker
- Einteilung in Dihydropyridine (z.B. Nifedipin, Amlodipin) und Nicht-Dihydropyridine (z.B. Diltiazem, Verapamil)
- Nicht-Dihydropyridine bewirken negative Chronotropie
- Dihydropyridine bewirken periphere Vasodilatation
Empfehlungen
- Atropin-Gabe als First-Line-Therapie bei Kalziumkanal-Blocker-Intoxikation
- Vasopressoren-Gabe bei Hypotonie infolge Kalziumkanalblocker-Vergiftung (z.B. Norepinephrin mit 100 µg/min bei Erwachsenen)
- Gabe von hochdosiertem Insulin bei Hypotonie infolge Kalziumkanalblocker-Vergiftung (hochdosiertes Insulin verbessert Inotropie bei kardiogenem Schock)
- Kalzium-Gabe bei Kalziumkanal-Blocker-Intoxikation
- VA-ECMO bei kardiogenem Schock infolge Kalziumkanalblocker-Vergiftung (Überlebensraten von bis zu 77 %)
- ggf. Pacing bei refraktärer Bradykardie infolge Kalziumkanalblocker-Vergiftung
- unklare Wirksamkeit von Methylenblau bei refraktärem vasodilatatorischem Schock aufgrund Kalziumkanalblocker-Vergiftung
- keine routinemäßige Lipidemulsionstherapie i.v. bei Kalziumkanalblocker-Vergiftung
Kokain
- symptomatische Wirkung von Kokain besteht aus Tachykardie, Hypertonie, Hyperthermie, starkem Schwitzen, erhöhter psychomotorischer Aktivität und Krampfanfällen
- Kokain induziert Tachykardie (postsynaptischer β-adrenerger Rezeptor-Agonismus) und Hypertonie (peripherer postsynaptischer α-adrenerger Rezeptor-Agonismus) durch Hemmung der Katecholamin-Wiederaufnahme
- hemmt zusätzlich Wiederaufnahme von Noradrenalin, Epinephrin, Dopamin und Serotonin
- ggf. auch QT-Verlängerung durch Blockade kardialer Kaliumkanäle
Empfehlungen
- schnelle externe Kühlung bei lebensbedrohlicher Hyperthermie durch Kokainvergiftung (Verdunstungs- oder Tauchkühlungsmethoden besser als Kühldecken, Kältepacks etc.)
- Natriumbicarbonat-Gabe ist bei Breitkomplex-Tachykardie oder Herzstillstand infolge Kokainvergiftung
- Lidocain-Gabe bei Breitkomplex-Tachykardie infolge Kokainvergiftung
- Vasodilatatoren-Gabe (z.B. Nitrate, Phentolamin, Kalziumkanalblocker) bei kokaininduzierten koronaren Vasospasmen oder hypertensiven Notfällen
Cyanide
- Cyanid hemmt Zellatmung in den Mitochondrien
- Folgen sind rascher kardiovaskulärer Kollaps, Laktat-Azidose, Krampfanfälle und ggf. auch der Tod
- Hydroxocobalamin (Vitamin B12a) fängt Cyanid auf äquimolarer Basis ab und bildet ungiftiges Cyanocobalamin (alternativ oxidiert Natriumnitrit Hämoglobin zu Methämoglobin, das dann Cyanid bindet und Cyanmethämoglobin bildet)
- Natriumthiosulfat dient als Substrat für Cyanid-Stoffwechsel und bildet minimal toxisches Thiocyanat
- Hydroxocobalamin wird wegen schnellem Wirkungseintritt und einfacher Anwendung bevorzugt (Nebenwirkungen sind z.B. vorübergehender Bluthochdruck, Hautverfärbungen, Hautausschlag)
Empfehlungen
- Hydroxocobalamin-Gabe bei Cyanidvergiftungen.
- Natriumnitrit-Gabe bei Cyanidvergiftungen, wenn Hydroxocobalamin nicht verfügbar
- zusätzlich zu Hydroxocobalamin- oder Natriumnitrit-Gabe Natriumthiosulfat-Gabe
- Gabe von 100 % Sauerstoff
Digoxin und andere kardiale Glykoside
- z.B. Medikamente wie Digoxin und Digitoxin, Pflanzen wie Fingerhut und Oleander und bestimmte Krötengifte, die als Ethnopharmaka oder Halluzinogene eingenommen werden
- akute Digoxinvergiftung führt häufig zu Hyperkaliämie, welche gemäß ALS-Leitlinien mit Kalzium-Gabe therapiert werden soll, sowie Herzrhythmusstörungen
Empfehlungen
- Gabe von digoxinspezifischen Antikörperfragmenten (Digoxin-Fab) bei Digoxin- oder Digitoxin-Vergiftungen
- Digoxin-Fab-Gabe bei Vergiftung durch Bufo-Krötengift und gelben Oleander sowie durch andere Herzglykoside
- Atropin-Gabe bei Bradykardie, die durch Digoxin und andere Herzglykoside verursacht ist
- ggf. Pacing bei Bradykardie aufgrund von Digoxin-Intoxikation und Vergiftung aufgrund anderer Herzglykosid
- Gabe von Lidocain, Phenytoin oder Bretylium zur Behandlung von ventrikulären Rhythmusstörungen
- keine Hämodialyse, Hämofiltration, Hämoperfusion oder Plasmapherese zur Behandlung einer Digoxinvergiftung
Lokalanästhetika
- typische Symptome bei Lokalanästhetika-Vergiftung sind Krampfanfälle, Unruhe, Synkope, Dysarthrie, periorale Taubheit, Verwirrtheit, Obtundation und Schwindel sowie kardiovaskuläre Störungen wie Asystolien, Kammerflimmern oder ventrikuläre Tachykardie
Empfehlungen
- Gabe von Lipidemulsion i.v. bei Lokalanästhetikavergiftung
- Anfallsbehandlung mit Benzodiazepinen
- Natriumbicarbonat-Gabe bei lebensbedrohlichen Breitkomplextachykardien
- Atropin-Gabe bei lebensbedrohlicher Bradykardie
- VA-ECMO bei refraktärem kardiogenem Schock
Methämoglobinämie
- erworbene Methämoglobinämie tritt auf, wenn Eisen im Hämoglobinmolekül vom Eisen (Fe2+) zum Eisen (Fe3+) oxidiert
- im eisenhaltigen Zustand kann Hämoglobin O2 nicht mehr wirksam binden
- Methämoglobinämie verursachende Stoffe sind Nitrate, Nitrite und Arzneimittel (z.B. Dapson, Benzocain, Phenazopyridin)
Empfehlungen
- Gabe von Methylenblau bei Methämoglobinämie
- Austauschtransfusion bei Methämoglobinämie, die nicht auf Methylenblau anspricht, erwägen
- hyperbare O2-Therapie zur Behandlung, die nicht auf Methylenblau anspricht, erwägen
- keine Gabe von N-Acetylcystein oder Ascorbinsäure zur Methämoglobinämie-Behandlung
Opioide
- allein in den USA 75673 Todesfällen im Jahr 2021 aufgrund von Opioiden (Anstieg um 35 %)
- isolierter Opioid-Intox ist mit ZNS- & Atemdepression verbunden, die zu Atem-/Herzstillstand führt
- meiste Opioid-assoziierte Todesfälle gehen auf gleichzeitige Einnahme mehrerer Substanzen oder auf medizinische & psychische Begleiterkrankungen zurück
- Antidot für Opioid-Intox ist Naloxon, ein µ-Opioidrezeptor-Antagonist
Empfehlungen
- ALS/pALS-Maßnahmen, v.a. notfallmäßige Beatmung, bis Spontanatmung wieder einsetzt
- bei Herzstillstand und (vermutetem) Opioid-Intox hat qualitativ hochwertige HLW in Ermangelung eines nachgewiesenen Naloxon-Nutzens Vorrang
- Naloxon-Gabe zusätzlich zu ALS/pALS-Maßnahmen bei V.a. Opioid-Intox und eindeutig tastbarem Puls
- Transport auf ITS zur weiteren Überwachung
- CAVE: ggf. wiederholte Naloxon-Gaben notwendig, da Naloxon-Wirkdauer kürzer als atemdepressive Wirkung
Organophosphate und Carbamate
- Organophosphate hemmen Acetylcholinesterase an muskarinergen und nikotinergen Rezeptoren dauerhaft durch kovalente Bindung
- Carbamate hemmen Acetylcholinesterase an muskarinergen und nikotinergen Rezeptoren, spalten sich aber spontan wieder von Acetylcholinesterase ab, was dann wieder aktiviert ist
- Intoxikation führt parasympathisch zu Bradykardie, Bronchospasmus, Bronchorrhoe, Miosis, Hypersalivation, Tränenfluss, Einnässen, Durchfall, Erbrechen, Schwitzen
- Intoxikation führt nikotinerg zu Tachykardie, Mydriasis, Krämpfen, neuromuskulärer Blockade und Lähmung
- Intoxikation führt zentralnervös zu Bewusstseinsstörungen, zentraler Apnoe & Krampfanfällen
Empfehlungen
- Verwendung geeigneter persönlicher Schutzausrüstung bei Behandlung von Patient*innen
- Dekontamination der Haut bei äußerer Organophosphat- oder Carbamat-Exposition
- sofortige Atropin-Gabe bei Bronchospasmus, Bronchorrhoe, Krampfanfällen oder erheblicher Bradykardie (Anfangsdosis alle 5 min bis vollst. Antagonisierung, also bds. ves. AG, HF > 80/min & RRsys > 80 mmHg, verdoppeln)
- frühzeitige ETI bei lebensbedrohlichem Organophosphat- oder Carbamatintox
- Benzodiazepin (Diazepam oder Midazolam) zur Behandlung von Krampfanfällen und Unruhe
- Pralidoxim-Gabe bei Organophosphatvergiftung erwägen
- keine Verwendung von Muskelrelaxien wie Succinylcholin und Mivacurium
Natriumkanal-Blocker
- Natriumkanal-Blocker-Intox führt zu QRS-Verlängerung, Hypotonie, Krampfanfällen, ventrikulären Herzrhythmusstörungen und Kollaps
- ventrikulären Rhythmusstörungen gehen i.d.R. charakteristische EKG-Veränderungen wie QRS-Intervall-Verlängerung und RAD (Right Axis Deviation) voraus
Empfehlungen
- Natriumbicarbonat-Gabe bei lebensbedrohlicher Kardiotoxizität
- Einsatz von ECLS wie VA-ECMO bei refraktärem kardiogenen Schock
- Gabe von Vaughan-Williams Antidysrhythmika der Klasse Ib (z. B. Lidocain) bei lebensbedrohlicher Vergiftung mit Natriumkanalblocker der Klasse Ia oder Ic
- Lipidemulsion i.v., wenn andere Therapieansätze frustran verlaufen
Sympathomimetika
- Sympathomimetika-Vergiftung kann plötzlichen Herzstillstand in Form von VF, VT oder PEA verursachen
- Vasospasmus kann Herzinfarkt verursachen, selbst bei normalen Koronararterien
- Hyperthermie ist eine schwere und schnell lebensbedrohliche klinische Symptomatik
- obwohl es kein direktes Antidot gibt, können Sedativa die psychomotorische Unruhe, die zum Delir, Rhabdomyolyse und Hyperthermie führt, therapieren
- bei angemessener Sedierung ist i.d.R. keine blutdrucksenkende Medikation erforderlich
- externe Kühlung wirkt Hyperthermie direkt entgegen und kann Schädigung des Gehirns und anderer Organe verringern
Empfehlungen
- Sedierung bei schwerer Unruhe infolge Sympathomimetika-Vergiftung (z.B. mit Benzodiazepinen, Antipsychotika, Ketamin)
- rasche externe Kühlung bei lebensbedrohlicher Hyperthermie infolge Sympathomimetika-Vergiftung (Verdunstungs- oder Tauchkühle besser als Kühldecken, Kältepacks etc.)
- Vasodilatatoren, wie z.B. Phentolamin und/oder Nitrate, bei koronaren Gefäßspasmen erwägen
- mechanische Kreislaufunterstützung, wie z.B. eine intraaortale Ballonpumpe oder VA-ECMO, bei kardiogenem Schock, der auf andere Therapieansätze frustran verlaufen, erwägen
- längere körperliche Fixierung ohne Sedierung ist potenziell schädlich
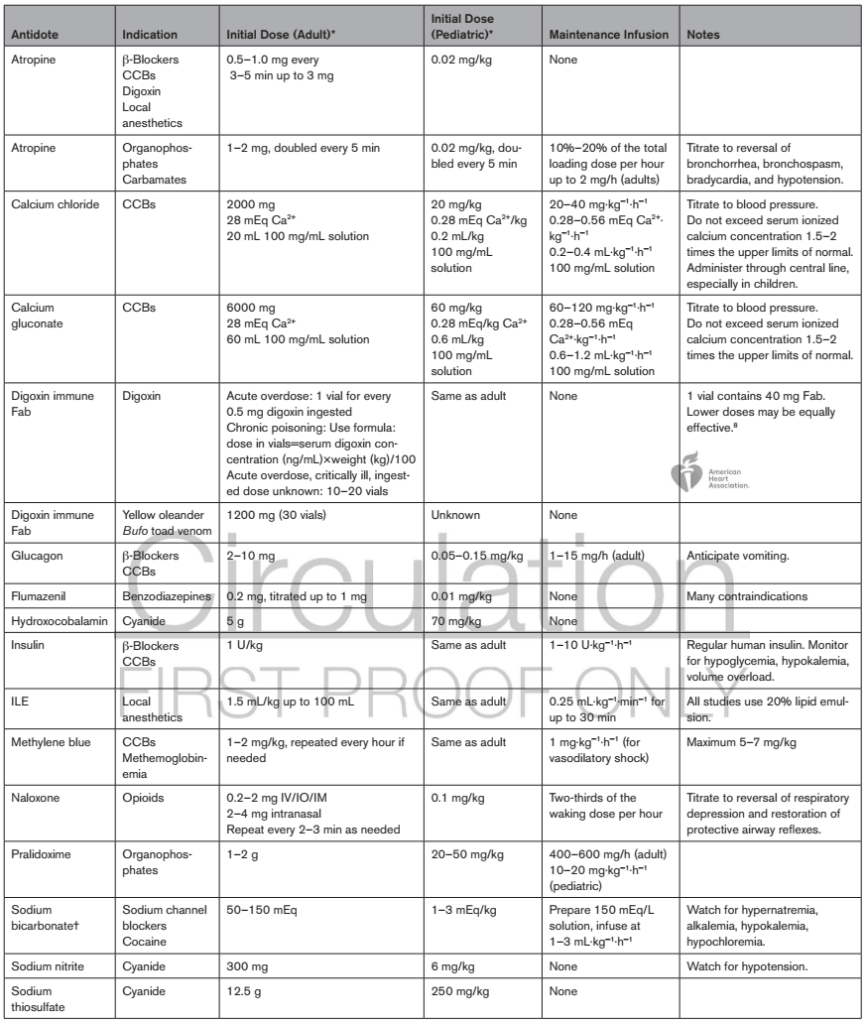
Dosierungen


Sei der Erste der einen Kommentar abgibt