Seit dem Jahr 2008 wird auf Initiative der European Foundation for the Care of Newborn Infants (EFCNI) und weiterer europäischer Elternorganisationen am 17. November initial als Internationaler Frühgeborenen-Tag und ab 2011 als Welt-Frühgeborenen-Tag begangen, um ein Bewusstsein für die Herausforderungen und die Belastung rund um das Thema der Frühgeburt und frühgeborener Kinder zu schaffen. Deswegen dreht sich heute auch bei FOAMio alles um das Thema Frühgeburt.
Die meisten Mitarbeitenden im Rettungsdienst bzw. in der präklinischen Notfallmedizin sind wahrscheinlich froh, wenn sie nie mit einer Geburt im präklinischen Setting konfrontiert sind, und wahrscheinlich noch erfreuter, wenn es sich dabei nicht um eine Frühgeburt handelt. Die meisten kann man diesbezüglich auch beruhigen, da die Zahl an ungeplanten außerklinischen Geburten ohne Hebammenbeteiligung, aber mit Rettungsdienstbeteiligung, bei ca. 500 Geburten liegt, was etwa 0,07 % aller Geburten ausmacht. Besorgniserregend ist aber die mehr als 2-fach erhöhte präklinische Mortalität bei der Gruppe der frühgeborenen Kindern im Vergleich zu den intrahospitalen Frühgeburten.
Grundsätzliches
Bei ca. 65 % aller Frühgeburten sind vorzeitige Wehen mit/ohne einem früh-/vorzeitigen Blasensprung ursächlich. Grundsätzlich lässt sich konstatieren, dass Frühgeborene aufgrund einiger erhöhten Risiken einer besonderen Beobachtung bedürfen. Zu diesen Risiken gehören v.a.:
- fetale Azidose
- Hypothermie < 36 °C (durch Verminderung des subkutanen braunen Fettgewebes)
- postnatale Hypoglykämie (10-fach erhöhtes Risiko aufgrund von erhöhtem Energiebedarf)
- Polyzythämie mit respiratorischen Störungen sowie zerebrale Minderperfusion (10-fach erhöhtes Risiko aufgrund chronischer intrauteriner Hypoxien)
Des Weiteren haben frühgeborene Kinder oftmals ein Apnoe-Bradykardie-Hypoxämie-Syndrom (ABHS), eine bronchopulmonale Dysplasie, einen offenen Ductus Botalli, intraventrikuläre Hirnblutungen, periventrikuläre Leukomalazie sowie eine nekrotisierende Enterokolitis und/oder eine Retinopathia praematurorum.
Initial ist es wahrscheinlich wichtig erstmal ein paar Begriffe zu klären bzw. zu erklären. Deshalb nachfolgend ein kleines, kurzes und knappes Glossar mit den wichtigsten Begriffen:
- Neugeborenen-/Neonatalperiode (CAVE: hier divergieren die wissenschaftlichen Daten)
- frühe Neugeborenenperiode: 1. – 7. Lebenstag
- späte Neugeborenenperiode: 8. – 28. Lebenstag
- Perinatalperiode: 28. SSW bis zum 7. Tag nach der Geburt
- Lebendgeburt: Kind, bei welchem nach der Scheidung vom Mutterleib entweder das Herz geschlagen oder die Nabelschnur pulsiert oder die natürliche Lungenatmung eingesetzt hat (§ 31 PStV)
- Totgeburt: keiner der Punkte der Lebendgeburt (Herzschlag, Nabelschnurpulsation oder Einsetzen natürliche Lungenatmung) + Gewicht des Kindes > 500 g oder < 500 g, aber ≥ 24. SSW (§ 31 PStV)
- perinatale Mortalität: Sterblichkeit vor Geburt (Totgeburtlichkeit) und Sterblichkeit innerhalb der ersten 7 Lebenstage (frühe neonatale Sterblichkeit) bezogen 1000 Lebendgeborene pro Jahr
- Gestationsalter: Zeitraum von Tag 1 der letzten Menstruation bis zur Geburt des Kindes
- reifes Neugeborenes: Gestationsalter von 259 – 294 d (37. – 42. SSW)
- Frühgeborenes: Gestationsalter von < 259 d (< 37. SSW)
- übertragenes Neugeborenes: Gestationsalter von > 294 d (> 42. SSW)
- Neugeborenes mit niedrigem Geburtsgewicht: Geburtsgewicht < 2500 g
- Neugeborenes mit sehr niedrigem Geburtsgewicht: Geburtsgewicht < 1000 – 1500 g
Epidemiologie
In Deutschland wurden im Jahr 2021 insgesamt 771.222 Kindern geboren, wovon 768.012 lebend geboren wurden. Betrachtet man die Gruppe der frühgeborenen Kinder (< 37. SSW), so waren dies im Jahr 2021 in Deutschland 60.557 Kinder, was ca. 7,85 % ausmacht (bereinigte Zahlen zu den Lebendgeburten: 58.196 Kinder, also 7,58 %). Schaut man sich diese Gruppe nochmals genauer an, so ergibt sich folgendes Bild (CAVE: Zahlen bilden lebend- & totgeborene Kinder ab):
- 32. – 36. SSW: 49.893 Kinder
- 28. – 31. SSW: 6.246 Kinder
- < 28. SSW: 4.418 Kinder
Bezogen auf das Gewicht der frühgeborenen Kinder im Jahr 2021 kommt man zu folgender Verteilung, welche zur Verdeutlichung ergänzt ist um gleich schweres Obst/Gemüse (CAVE: Zahlen bilden lebend- & totgeborene Kinder ab):
- 2.000 – 2.499 g: 28.720 Kinder (Ananas bis Hokkaido-Kürbis)
- 1.500 – 1.999 g: 9.593 Kinder (typischer Sack Kartoffeln bis Papaya)
- 1.000 – 1.499 g: 5.104 Kinder (Flasche Wasser bis typischer Sack Kartoffeln)
- 750 – 999 g: 2.048 Kinder (große Süßkartoffel bis Flasche Wasser)
- 500 – 749 g: 1.891 Kinder (Brokkoli bis große Süßkartoffel)
- < 500 g: 1.127 Kinder
- 28.720 Frühgeborene zwischen 2.000-2.499 Gramm.
- 9.593 Kinder wogen zwischen 1.500-1.999 Gramm
- 5.104 Kinder wogen zwischen 1.000-1.499 Gramm.
- 2.048 Kinder wogen zwischen 750-999 Gramm.
- 1.891 Kinder wogen zwischen 500-749 Gramm.
- 1.127 Kinder wogen bei ihrer vorzeitigen Geburt unter 500 Gramm.
Im Jahr 2021 betrag die perinatale Mortalität (s.o.) insgesamt 4.205, wobei 1.375 in den ersten 7 Tagen starben. Weitet man diesen Zeitraum auf das erste Lebensjahr aus, so verstarben 2.368 zunächst lebend geborene Kinder. Weitere spannende epidemiologische Zahlen und Fakten gibt es nachfolgend im Kurzabriss:
- weltweite Inzidenz der Frühgeburt: 6,2 – 11,9 % (2,4 – 4,3 % bei Frühgeborenen < 32. SSW)
- Hitzestress von 30 °C erhöhte das Frühgeburtsrisikos um 20 % und bei Temperaturen > 35 °C sogar um 45 % (t zu Erhöhung des Frühgeburtsrisikos um 20 %, Temperaturen > 35 °C sogar um 45 Prozent* (Schätzung für 2033 das jedes 6. Kind, ca. 15 % zu früh geboren werden, also doppelt so viele wie heute; jeweils relatives Risiko)
- unmittelbare Kosten für die neonatologische Versorgung eines extrem frühgeborenen Kindes liegen bei ca. 100.000 € (Folgekosten nochmals erheblich höher)
- Frühgeburten stellen einen Hauptrisikofaktoren für DALYs, also verlorene Jahre aufgrund von Krankheit, Behinderung oder vorzeitigem Tod, dar
- in Deutschland sind 70 % der perinatale Morbidität und Mortalität verursacht durch Frühgeburten
- perinatale Mortalität in Deutschland
- < 28 + 0 SSW: ca. 35 %
- 28 + 0 bis 31 + 6 SSW: ca. 8 %
- 32 + 0 bis 36 + 6 SSW: ca. 1 -2 %
- am Termin: 0,1 %
Risikofaktoren für Frühgeburt
- Z.n. spontaner Frühgeburt
- Präeklampsie
- Z.n. medizinisch indizierter Frühgeburt
- Z.n. Konisation (operative Entfernung von Gewebekegeln aus dem Cervix uteri)
- Schwangerschaftsintervall < 12 Monate
- Schwangerschaftsalter < 18 Jahre
- schlechtere sozioökonomische Lebensbedingungen
- alleinstehende Mutter
- bakterielle Vaginose
- asymptomatische Bakteriurie
- vaginale Blutung in der Früh- oder Spätschwangerschaft
- Zwillingsschwangerschaft
- Rauchen
- Parodontitis
- Anämie
Diagnostik
Nach der Geburt des Kindes ist es initial am Wichtigsten den körperlichen Status von selbigem zu bewerten. Hierzu eignet sich der nachfolgend dargestellte Apgar-Score, welcher in Minute 1, Minute 5 und Minute 10 nach Geburt erhoben werden soll:
| Kriterium | 0 Punkte | 1 Punkt | 2 Punkte |
|---|---|---|---|
| Kolorit | blau oder weiß | Stamm rosig Extremitäten blau | rosig |
| Herzschläge | keine | < 100/min | > 100/min |
| Reflexe | keine | Verziehen des Gesichts, Grimassieren | Husten bzw. Niesen, Würgen, Schreien |
| Tonus | schlaff | mittel, träge Flexionsbewegungen | gut, normale Spontanbewegung |
| Atmung | keine | Schnappatmung oder unregelmäßige, langsame Atmung, Tachy-/Dyspnoe, Einziehungen | regelmäßig, kräftig schreiend |
Score > 7 Punkte nach Geburt –> Neugeborenes in gutem Zustand
Score < 4 Punkte nach einer Minute bzw. < 6 Punkte nach 5 Minuten –> Warnzeichen für Hypoxie
Nach dem Wärmemanagement und einer initialen taktilen Stimulation ist ein schnelles Monitoring zur Überprüfung der wichtigsten Vitalparameter von Bedeutung, hierzu zählt v.a. die Überwachung der Hezrfrequenz, Sauerstoffsättigung (CAVE: an der rechten Hand) und ggf. ein EKG. Wie in der Tabelle des Apgar-Score schon skizziert sind Atmungsprobleme, und hier an erster Stelle die perinatale Asphyxie, ein großes Problem. Die Asphyxie meint in diesem Zusammenhang einen Zustand, bestehend aus Hypoxie und gemischter Azidose. Abhängig ist die perinatale Asphyxie primär vom Ausmaß bzw. der Dauer des O2-Mangels. Die perinatale Asphyxie gliedert sich in die blaue Asphyxie, welche sich als Beeinträchtigung des Atem- und Kreislaufzentrums mit gestörten Anpassungsvorgängen, einer Bradykardie und einer Zyanose zeigt. Sofern der Sauerstoffmangel nicht therapiert wird, werden die Hirnfunktionen sukzessive beeinträchtigt und zum Schock mit insuffizienter Mikrozirkulation, Tonuslosigkeit und Reflexverlust (auch weiße Asphyxie genannt).
Da neben dem Fakt, dass es sich bei einem Neugeborenen um ein Frühgeborenes handelt, vor allem auch wichtig ist abzuklären, ob und wie ausgeprägt es sich bei dem Neugeborenen um eine Mangelgeburt handelt, ist vor allem das Gestationsalter von großer Bedeutung, denn bei ca. 3 von 4 Neugeborenen stimmen Geburtsgewicht und Gestationsalter überein. Zur Bestimmung des Gestationsalters sind vor allem die nachfolgenden Faktoren von Relevanz:
- Schwangerschaftsdauer, also der Zeitraum ab dem ersten Tag der letzten Regelblutung bis zur jetzt stattfindenden Geburt (CAVE: i.d.R. liegt errechneter Geburtstermin vor)
- Zeichen der morphologischen Reife (z.B. bei übertragenen Neugeborenen spärliches subkutanes Fettgewebe, faltenreiche & tief gefurchte Haut, pergamentartig schuppende Haut sowie fehlende Käseschmiere)
- neurologischer Entwicklungsgrad
- Pupillenreaktion ab 29. SSW vorhanden & ab 31. SSW konstant vorhanden
- Glabella-Klopfreflex (Fingerschlag auf Stirnmitte –> Lidschluss) ab 32. SSW vorhanden & ab 34. SSW konstant vorhanden
- Schulterreflex (Beugen der Ellenbogen, Spannung der Schultern, Heben des Kopfes beim Hochziehen an den Händen in Rückenlage) ab 33. SSW vorhanden & ab 36. SSW konstant vorhanden
- Gewicht, Länge & Kopfumfang (intrauterine Mangelernährung –> proportional/dysproportionale Wachstumsverzögerungen)
Ein weiterer Punkt, der einer raschen Abklärung bedarf, ist das Bestehen bzw. Nichtbestehen einer Hirnblutung, welche sich in 50 % der Fälle am 1. Lebenstag entwickelt , in 25 % in den ersten 2. – 3. Lebenstagen. Denn as Risiko einer solchen ist bei Frühgeborenen extrem hoch, wie die nachfolgenden Zahlen zeigen:
- Hirnblutungsrisiko in 25. SSW: 50 %
- Hirnblutungsrisiko in 26. SSW: 38 %
- Hirnblutungsrisiko in 28. SSW: 20 %
Exkurs: Frühgeborene an der Grenze der Lebensfähigkeit
Bei der Behandlung von Frühgeborenen kommt man nicht um das Thema der Lebensfähigkeit von frühgeborenen Kinder herum. Die Gesellschaft für Neonatologie und Pädiatrische Intensivmedizin (GNPI) hat hierzu im Mai 2020 die passende Leitlinie „Frühgeborene an der Grenze der Lebensfähigkeit“ herausgegeben. Die wichtigsten Inhalte werden nachfolgend dargestellt, vorher ist aber noch wichtig die rechtlichen Rahmenbedingung darzulegen.
Kurz und knapp lässt sich sagen, dass jedes Kind „Anspruch auf Behandlung und Betreuung hat, die den individuellen Bedürfnissen angemessen sind, unabhängig von seinen Lebens- und Überlebensaussichten“ und es ist die ärztliche Aufgabe, „unter Achtung der Würde des Patienten (Grundgesetz Art 1.) und seiner Grundrechte auf Leben und körperliche Unversehrtheit (Grundgesetz Art. 2 Abs. 2) Leben zu erhalten, Gesundheit zu schützen oder wiederherzustellen sowie Leiden zu lindern und Sterbenden bis in den Tod beizustehen“. Aber es gilt zu betonen, dass die „ärztliche Verpflichtung zur Lebenserhaltung nicht unter allen Umständen besteht“ und „indizierte medizinische Maßnahmen darüberhinaus einer Einwilligung des Patienten bzw. im Falle der fehlenden Einwilligungsfähigkeit des Patienten der Einwilligung des Patientenvertreters bedürfen“ (aus GNPI-Leitlinie „Frühgeborene an der Grenze der Lebensfähigkeit“). Des Weiteren gelten die o.g. Vorschriften zur Lebend- und Totgeburt.
Grundsätzlich muss man konstatieren, dass die Überlebenswahrscheinlichkeit von Frühgeborenen mit abnehmendem Gestationsalter und abnehmendem Geburtsgewicht sinkt, aber zu berücksichtigen ist, dass sich eine Geburt in einem Perinatalzentrum der Maximalversorgung mit hohen Fallzahlen positiv auswirkt.
Die Grenze der Lebensfähigkeit Frühgeborener ist auch trotz größerer Datenmenge immer noch schwer zu definieren und spielt sich vor allem in einem großen Graubereich, welcher sich wie folgt zeigt:
- < 22. + 0/7 SSW & Gewicht < 400 g: bis auf Einzelfälle keine realistischen Möglichkeiten, daher sind medizinische Maßnahmen i.d.R. aussichtlos
- 22. + 0/7 – 22. + 6/7 SSW sowie 23. + 0/7 – 23. + 6/7 SSW & Gewicht < 400 g: ggf. Überleben mit z.T. erheblicher Morbidität; primär nur auf Lebensverlängerung oder Palliation zielende Behandlung nur auf ausdrücklichen Wunsch der Eltern
- 23. + 0/7 – 23. + 6/7 SSW sowie 24. + 0/7 – 24. + 6/7 SSW & Gewicht < 400 g: Überlebenschance von in spezialisierten Zentren behandelter Frühgeborener steigt auf über 50 %, aber oftmals mit schwerwiegenden Gesundheitsstörungen und einer trotzdem sehr unsicheren Gesamtprognose
- > 24. + 0/7 SSW & Gewicht ≥ 400 g: Überlebenschancen i.d.R. so hoch, dass lebenserhaltende Therapie anzustreben ist
Therapie
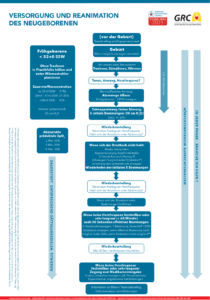
Für die Neugeborenenversorgung grundsätzlich, aber auch für die Versorgung von Frühgeborenen ist der Versorgungsalgorithmus der ERC/GRC zu nutzen. Weitere Informationen für die grundsätzliche Neugeborenenversorgung, egal ob prä- oder innerklinisch, sind im gleichnamigen Kapitel dieses Beitrages zu finden oder in der Leitlinienzusammenfassung der ERC/GRC-Leitlinien zur „Newborn resuscitation and support of transition of infants at birth“.
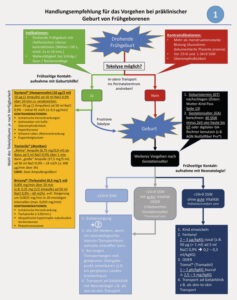
Für die präklinische Therapie einer (drohenden) Frühgeburt gibt es, vor allem für den deutschsprachigen Raum, keine spezifische Literatur. Hervorzuheben sind hier aber die „Regionalen Handlungsempfehlungen zur notärztlichen Versorgung Frühgeborener nach präklinischer Geburt für die Steiermark“ von Schwaberger et al. aus dem Jahr 2019. Was primär aber zu bedenken ist, ist, dass ein Pädiater und/oder Neonatologe frühzeitig in die Behandlung und Beratung bei drohender Frühgeburt einbezogen werden sollte, v.a. um eine initiale medikamentöse Therapie abzuklären (ggf. auch als Zubringer über NEF/RTH oder mit Baby-NAW mit Inkubator an der Einsatzstelle).
Sofern eine Tokolyse und damit auch ein In-utero-Transport in das nächst gelegene Perinatalzentrum sowie ggf. die Gabe antenataler Steroide möglich ist, sollte diese, nach Abwägung in der (Kontra-)Indikationen, erfolgen, um die Schwangerschaft um min. 48 h zu verlängern (i.d.R in 75 – 93 % der Fälle möglich). Zu den relevantesten Indikationen und Kontraindikationen gehören:
Indikationen
- Gestitationsalter: 22. + 0 bis 33. + 6 SSW
- drohende Frühgeburt mit spontanen, rhythmischen, vorzeitigen Uterus-kontraktionen (Wehen >30 s, mind. 2x in 10 min. bzw. Wehen > 4/20 min mit verkürzter funktioneller Zervixlänge und/oder Eröfnung der Zervix)
- Wehentatigkeit bei Schrag-/ Quer-/ Beckenendlage
Kontraindikationen
- Blutung der Mutter mit hämodynamischer Instabilität
- vorzeitige Plazentalösung mit notwendiger Schwangerschaftsbeendigung
- Gestitationsalter: < 20. + 0 & ≥ 34. + 0 SSW
- Substanz-spezifische Kontraindikationen der Tokolytika
- intrauteriner Fruchttod
- letale fetale Fehlbildung
- schwere Präeklampsie/Eklampsie mit Notwendigkeit zur Entbindung
Die Literatur ist hier bei der Auswahl des Tokolytikums eher uneindeutig. Die Leitlinie „Prävention und Therapie der Frühgeburt“ der DGGG verweißt hier auf Atosiban, Nifedipin und NO-Donoren und die oben erwähnte regionalen Handlungsempfehlungen aus der Steiermark nennt die folgenden drei Tokolytika:
- 1 Ampulle Hexoprenalin (10 μg/2 mL) + 10 mL NaCI 0,9% i.v. über 10 min, dann 2 Ampullen + 50 mL NaCl 0,9% mit initial 45 mL/h (KI: ischämische Herzerkrankungen, Asthmatiker mit Sulfite-Überempfindlichkeit, Hyperthyreose, schwere Leber-/Nierenerkrankung, Engwinkelglaukom)
- 1 „kleine“ Ampulle Atosiban (6,75 mg/0,9 mL) + 5 ml NaCI 0,9% über 1 min, dann 1 „große “ Ampulle (37,5 mg/5 mL) + 50 mL NaCl 0,9% mit 24 mL/h (CAVE: Zwei Ampullengrößen!!!)
- 1 „halbe“ Ampulle Terbutalin (also 0,5 mL = 0,25 mg) + 50 mL NaCl 0,9% mit 60 mL/h, ggf. Steigerung um 0,0025 mg/min in 20-minütigen Intervallen (max. 0,020 mg/min) (KI: ischämische Herzerkrankung, Tachykardie > 120/min, idiopathische hypertrophe subalvuläre Aortenstenose, Phäochromozytom)
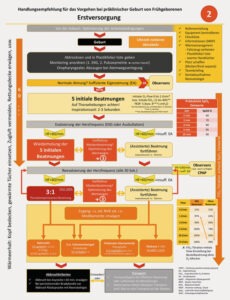
Zusätzlich kann zur Neuroprotektion des Kindes Magnesium i.v. erwogen werden. Für die Geburt selbst sind die Vorgaben der aktuell gültigen ERC/GRC-Leitlinien zu befolgen (siehe Algorithmus „Versorgung und Reanimation des Neugeborenen“ am Ende). Zu den relevantesten Punkten, v.a. in Hinsicht auf die Versorgung frühgeborener Kinder, zählen:
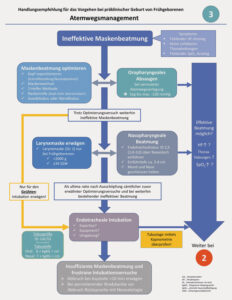
- Atemunterstützung & Atemwegsmanagement
- routinemäßiges oro- oder nasopharyngeales Absaugen
- bei insuffizienter Atmung (bzw. ggf. auch bei Spontanatmung & HF > 100/min) Atemunterstützung mittels CPAP über Gesichtsmaske oder Rachentubus (CAVE: i.d.R. nicht mgl. über Beatmungsgeräte im RD)
- mit FiO 2 von 21 – 40 % beginnen (0 – 1 L/min ohne Reservoirs = FiO 2 von 21 – ca. 65%) mit Ziel der präduktalen SpO2 von min. > 80% nach 5 Lebensminuten
- CAVE: richtige Wahl der Größe des Kinderbeatmungsbeutel
- bei > 2000 g bzw. ≥ 34. SSW Einsatz supraglottischer Atemwegenshilfen erwägen
- CAVE: ETI beim Frühgeborenen ist schwierig und sollte nur bei Expertise erwogen werden
- Temperaturmanagement mit Ziel-Temperatur von 36,5 – 37,5°C
- regelmäßige Evaluation zur Vermeidung von Hypo- (≤ 36,0°C) oder Hyperthermie (> 38,0°C)
- bei < 32. + 0 SSW Frühgeborenes unter Aussparung des Gesichts komplett in durchsichtige Plastikfolie hüllen und nicht vorher abtrocknen (ggf. zusätzlich vorgewärmte Handtücher, z.B. in Mikrowelle bei 600 – 800 Watt über 30 sec; CAVE: Wärmeverlust über Kopf)
- therapeutische Hypothermie nach erfolgreicher Reanimation in Betracht ziehen
- späteres Abnabeln & danach Skin-to-Skin-Kontakt mit Mutter (frühestens nach 1 min; idealerweise erst nach Belüftung der Lunge; kein Ausstreichen der Nabelschnur bei Kindern < 28. SSW, Ausnahme: verzögertes Abnabeln nicht möglich)
- Nabelvenenkatheter = Zugangsweg der 1. Wahl (CAVER: erfordert Expertise), alternativ i.o.-Zugang oder pVK
- Medikamente
- Adrenalin i.v./i.o. bei HF < 60/min trotz suffizienter Beatmung und Thoraxkompression (10 – 30 µg/kg KG
- Volumentherapie i.v./i.o. bei Verdacht auf Blutverlust oder Schock (10 mL/kg KG Rh-negatives Blut (Gr. 0) oder VEL
- bei insuffizientem Atemantrieb Theophyllin erwägen
- bei erhöhten Hypoglykämierisiko Glucose erwägen (4x kgKG = mL/h ODER 250 mg/kg KG als Bolus; 5 – 10%ige Lsg.)
- präklinische Surfactant-Gabe erwägen, wenn vorhanden & Expertise vor Ort (über ET oder über Sonde)
- Maßnahmen bei (V.a Hirnblutung) bestehen aus RR-Stabilisierung, normale Ziel-Oxygenierung (Vermeidung von Hyper- & Hypokapnien), Gerinnungskontrolle, Vermeidung von Hypoglykämie, großzügiger Antikonvulsiva-Einsatz & frühzeitiges neurochirurgisches Konsil
- Abbruch von Reanimationsmaßnahmen
- bei Asystolie > 10 – 20 min trotz suffizienter Beatmung, suffizienter Thoraxkompression & (mehrfach) erfolgter Adrenalin-Gabe sowie Ausschluss reversibler Ursachen Abbruch von Reanimationsmaßnahmen erwägen (CAVE: Entscheidung nur auf Grundlage gültiger Leitlinien o.Ä., nach Rücksprache mit Eltern & bestenfalls mit Neonatolog*innen bzw. Kinderärz*innen; siehe „Exkurs: Frühgeborene an der Grenze der Lebensfähigkeit“)
Hinsichtlich des Transportes ist grundsätzlich zu konstatieren, dass Schwangere mit drohender Frühgeburt mit Gestationsalter zw. 20 – 26 vollendeter SSW direkt in ein Perinatalzentrum der höchsten Versorgungsstufe zu transportieren bzw. verlegen sind. Bzgl. der Transportmodalitäten gelten sonst die nachfolgenden Regelungen:
- bei zeitnahem Eintreffen eines neonatologischen Intensivtransportteams ist die Erstversorgung vor Ort zu bevorgen, um den Transport dann begleitet durch genügend Expertise zu realisieren (ggf. im Einzelfall Rendezvous-Verfahren erwägen, v.a. bei weiten Transportstrecken)
- Transport erst, sobald effektive Beatmung bzw. suffiziente Eigenatmung & Stabilisierung erreicht
- grundsätzlich ist der Transport in einem Inkubator allen anderen Verfahren zu bevorzugen, außer daraus resultiert eine nicht akzeptable Zeitverzögerung (sofern kein Inkubator-Transport mgl. „Känguru-Transport“, also Skin-to-Skin-Transport an der Brust der Mutter)
Die Kriterien zur Verlegung von Früh- und Reifgeborenen in Krankenhäuser der adäquaten Versorgungsstufe sind in der gleichnamigen Leitlinie zu finden und können auch zur Zielortauswahl in der Präklinik genutzt werden. Für die Gegebenheiten der anschließenden innerklinischen Versorgung lohnt sich ein Blick in die S2k-Leitlinie „Empfehlungen für die strukturellen Voraussetzungen der perinatologischen Versorgung in Deutschland“ der Deutsche Gesellschaft für Perinatale Medizin e.V. (DGPM).
Exkurs: idiopathische Apnoen, Bradykardien und Hypoxämien
Viele Frühgeborene haben Apnoen oder andere Atemauffälligkeiten, ab einem Reifealter > 43 Wochen treten diese nicht häufiger auf als bei Termingeborenen. Bei intermittierende Hypoxämie handelt es sich um den SpO2-Abfall auf < 80 % (CAVE: Mittelungszeit des Pulsoximeters von 8 – 10 sec berücksichtigen; z.B. ist bei Pulsoximeter-Mittelungszeit von 10 sec die Hypoxie-Alarmrate um die Hälfte reduziert als bei Mittelungszeit von 2 sec) und bei einer Bradykardie um einen HF-Abfall auf <80/min. jeglicher Dauer. Die Diagnosestellung erfolgt mittels klinischer Beobachtung und kontinuierlicher Monitorüberwachung. Die Ursachen für das sog. Apnoe-Bradykardie-Hypoxämie-Symptomatik (ABHS) sind mannigfaltig und umfassen z.B. Infektion, Hirnblutung, Krampfanfall, Hypoglykämie, -natriämie, -kalzämie, Anämie, Hyper-/Hypothermie, aber auch andere Grunderkrankungen. Aber auch die maternale Opiatgabe kurz vor Geburt kann hierfür ursächlich sein. Therapiert wird das ABHS i.d.R. durch die Behandlung der Grundkrankheit. Sofern die ABHS aber persistiert, sollten Differentialdiagnosen wie ein zentrales Hypoventilationssyndrom, Robin-Sequenz, Joubert-Syndrom oder eine mütterliche Myasthenie berücksichtig werden. Der SpO2-Zielbereich liegt bei 91 – 95 %. Weitere Therapieempfehlungen sind die Oberkörper-Hochlagerung (15°-Hochlagerung), die Gabe von Koffeinzitrat als Mittel der 1. Wahl und nasale Atemhilfen. Die Gabe von Doxapram ist nicht empfohlen.
Versorgungsalgorithmen (Klick zum Vergrößern)
Quellen
- AMBOSS GmbH. „Drohende Frühgeburt“. AMBOSS, 12. September 2023. https://www.amboss.com/de/wissen/drohende-fruhgeburt.
- Berger, R., H. Abele, Y. Garnier, R. Kuon, W. Rath, und H. Maul. „Frühgeburt: Epidemiologie, Prädiktion und Prävention“. Der Gynäkologe 53, Nr. 5 (Mai 2020): 331–37. https://doi.org/10.1007/s00129-020-04584-5.
- Deutsche Gesellschaft für Gynäkologie und Geburtshilfe (DGGG), Österreichische Gesellschaft für Gynäkologie und Geburtshilfe (ÖGGG), und Schweizerische Gesellschaft für Gynäkologie und Geburtshilfe (SGGG), Hrsg. „S2k-Leitlinie ‚Prävention und Therapie der Frühgeburt‘“. Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften, 1. Oktober 2022. https://register.awmf.org/de/leitlinien/detail/015-025.
- Deutsche Gesellschaft für Perinatale Medizin e.V. (DGPM), Deutsche Gesellschaft für Gynäkologie und Geburtshilfe e.V. (DGGG), Gesellschaft für Neonatologie und pädiatrische Intensivmedizin e.V. (GNPI), Deutsche Gesellschaft für Kinder- und Jugendmedizin e.V. (DGKJ), Deutsche Gesellschaft für Anästhesiologie und Intensivmedizin e.V. (DGAI), Deutsche Gesellschaft für Hebammenwissenschaft e.V., Deutsche Gesellschaft für Kinderchirurgie e.V. (DGKCH), und Deutsche Gesellschaft für Pflegewissenschaft e.V. (DGP), Hrsg. „S2k-Leitlinie ‚Empfehlungen für die strukturellen Voraussetzungen der perinatologischen Versorgung in Deutschland‘“. Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften, 31. März 2021. https://register.awmf.org/de/leitlinien/detail/087-001.
- Gesellschaft für Neonatologie und pädiatrische Intensivmedizin e.V. (GNPI), Deutsche Gesellschaft für Gynäkologie und Geburtshilfe e.V. (DGGG), Deutsche Gesellschaft für Kinder- und Jugendmedizin e.V. (DGKJ), und Deutsche Gesellschaft für Perinatale Medizin e.V. (DGPM), Hrsg. „S1-Leitlinie ‚Verlegung von Früh- und Reifgeborenen in Krankenhäuser der adäquaten Versorgungsstufe‘“. Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften, 1. Mai 2019. https://register.awmf.org/de/leitlinien/detail/024-002.
- Gesellschaft für Neonatologie und pädiatrische Intensivmedizin e.V. (GNPI), Deutsche Gesellschaft für Gynäkologie und Geburtshilfe e.V. (DGGG), Deutsche Gesellschaft für Kinder- und Jugendmedizin e.V. (DGKJ), Deutsche Gesellschaft für Perinatale Medizin e.V. (DGPM), Deutsche Gesellschaft für Pflegewissenschaft e.V. (DGP), und Deutsche Gesellschaft für Hebammenwissenschaft e.V., Hrsg. „S2k-Leitlinie ‚Betreuung von Neugeborenen in der Geburtsklinik‘“. Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften, 14. März 2021. https://register.awmf.org/de/leitlinien/detail/024-005.
- Gesellschaft für Neonatologie und pädiatrische Intensivmedizin e.V. (GNPI), und Deutsche Gesellschaft für Kinder- und Jugendmedizin e.V. (DGKJ), Hrsg. „S2k-Leitlinie ‚Therapie idiopathischer Apnoen, Bradykardien und Hypoxämien bei Früh- und Reifgeborenen‘“. Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften, 2. Februar 2020. https://register.awmf.org/de/leitlinien/detail/024-013.
- Gesellschaft für Neonatologie und pädiatrische Intensivmedizin e.V. (GNPI), Deutsche Gesellschaft für Kinder- und Jugendmedizin e.V. (DGKJ), Deutsche Gesellschaft für Gynäkologie und Geburtshilfe e.V. (DGGG), Deutsche Gesellschaft für Perinatale Medizin e.V. (DGPM), und Akademie für Ethik in der Medizin e.V. (AEM), Hrsg. „S2k-Leitlinie ‚Frühgeborene an der Grenze der Lebensfähigkeit‘“. Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften, 1. Mai 2020. https://register.awmf.org/de/leitlinien/detail/024-019.
- Gortner, Ludwig, und Sascha Meyer, Hrsg. Duale Reihe Pädiatrie. 5. Aufl. Stuttgart: Georg Thieme Verlag, 2018. https://doi.org/10.1055/b-005-145246.
- Madar, John, Charles C. Roehr, Sean Ainsworth, Hege Ersdal, Colin Morley, Mario Rüdiger, Christiane Skåre, u. a. „European Resuscitation Council Guidelines 2021: Newborn Resuscitation and Support of Transition of Infants at Birth“. Resuscitation 161 (April 2021): 291–326. https://doi.org/10.1016/j.resuscitation.2021.02.014.
- Roos, Reinhard, Orsolya Genzel-Boroviczény, und Hans Proquitté, Hrsg. Checkliste Neonatologie. 4. Aufl. Stuttgart: Georg Thieme Verlag, 2010. https://doi.org/10.1055/b-002-5204.
- Schwaberger, Bernhard, Michael Eichinger, Johann Martensen, Nariae Baik-Schneditz, Mirjam Pocivalnik, und Berndt Urlesberger. „Regionale Handlungsempfehlungen zur notärztlichen Versorgung Frühgeborener nach präklinischer Geburt für die Steiermark“. Der Notarzt 35, Nr. 06 (Dezember 2019): 314–22. https://doi.org/10.1055/a-0903-2357.
- Yüzen, Dennis, Isabel Graf, Ann-Christin Tallarek, Bettina Hollwitz, Christian Wiessner, Ekkehard Schleussner, Detlef Stammer, u. a. „Increased Late Preterm Birth Risk and Altered Uterine Blood Flow upon Exposure to Heat Stress“. eBioMedicine 93 (Juli 2023): 104651. https://doi.org/10.1016/j.ebiom.2023.104651.


Sei der Erste der einen Kommentar abgibt