veröffentlichende Fachgesellschaft: American Diabetes Association (ADA), European Association for the Study of Diabetes (EASD), Joint British Diabetes Societies for Inpatient Care (JBDS), American Association of Clinical Endocrinology (AACE), and Diabetes Technology Society (DTS)
Datum der Veröffentlichung: 22.06.2024
Ablaufdatum:
Quelle/Quelllink: https://doi.org/10.2337/dci24-0032
Grundsätzliches
- diabetische Ketoazidose (DKA) und hyperglykämisch hyperosmolarer Zustand (HHS) sind zwei schwerwiegende, akute & lebensbedrohliche hyperglykämische Notfallbilder bei Menschen mit Typ-1-/Typ-2-Diabetes
- DKA- & HHS-Einweisungen haben in den letzten 10 Jahren weltweit zugenommen
- DKA ist durch Trias aus Hyperglykämie, erhöhte Ketonkonzentration im Blut und/oder Urin sowie metabolische Azidose gekennzeichnet
- HHS ist durch schwere Hyperglykämie, Hyperosmolalität und Dehydratation bei Fehlen einer signifikanten Ketose oder Azidose gekennzeichnet
- DKA ist das Ergebnis einer Kombination aus absolutem oder relativem Insulinmangel und einer Erhöhung der gegenregulatorischen Hormone (Glukagon, Epinephrin, Noradrenalin, Cortisol und Wachstumshormone)
- HHS hingegen gibt es noch Restmengen an Insulinsekretion, die die Ketose minimieren, aber die Hyperglykämie nicht mehr kontrollieren kann
Epidemiologie
- Mortalität bei DKA liegt bei < 1 % und die Mortalität beim HHS ist weiterhin 5- bis 10-mal höher
- fast 1 % aller KH-Aufenthalte bei Menschen mit Diabetes sind auf hyperglykämische Krisen zurückzuführen
- DKA tritt i.d.R. bei jungen Erwachsenen im Alter von 18 – 44 Jahren (61,7 %) mit Typ-1-Diabetes (70,6 %) auf
- HHS tritt i.d.R. bei Erwachsenen im mittleren Alter von 45 bis 64 Jahren (47,5 %) mit Typ-2-Diabetes (88,1 %) auf
Pathogenese
- Hauptunterschied zw. DKA und HHS ist der Grad der Insulininsuffizienz
- DKA: schwerer Insulinmangel und Anstieg der Konzentrationen von gegenregulatorischen Hormonen (Glukagon, Cortisol, Adrenalin & Wachstumshormone) –> Veränderungen des Insulin-Glukagon-Verhältnis –> erhöhte Glukoneogenese + beschleunigte Glykogenolyse + gestörte Glukoseverwertung im peripheren Gewebe –> Freisetzung freier Fettsäuren aus dem Fettgewebe (Lipolyse) –> unkontrollierte hepatische Fettsäureoxidation & Produktion überschüssiger Ketonkörper –> Ketonämie & metabolische Azidose
- HHS: weniger schwerer Insulinmangel –> Ketogenese verhindert, ABER hohe hepatische Glukoseproduktion & verringerte Glukoseverwertung im peripheren Gewebe –> Hyperglykämie –> osmotische Diurese –> Volumenverlust & Hämokonzentration –> hyperosmolare Störung & Nierenfunktionsstörung –> Verschlechterung kognitiver Funktionen
- bei DKA & HHS schwere Entzündungszustände, gekennzeichnet durch Anstieg von proinflammatorischen Zytokinen (Tumornekrosefaktor-α und Interleukin-1, -6 und -8), C-reaktivem Protein und Lipidperoxidations-Biomarkern

Risikofaktoren
diabetische Ketoazidose
- Infektionen (in 14 – 58 % der Fälle)
- interkurrente Erkrankungen
- psychischer Stress
- unterlassene oder unzureichende Insulintherapie
- Schlaganfall
- Alkohol- & Drogenkonsum
- Pankreatitis
- Lungenembolie
- Myokardinfarkt
- Trauma
hyperglykämisch hyperosmolarer Zustand
- Diabetes Typ 1
- jüngeres Alter
- hyper- oder hypoglykämische Krisen in der Vorgeschichte
- Nierenerkrankungen
- Neuropathie
- Depressionen
- Rauchen, Alkohol- & Drogenmissbrauch
- hoher Hämoglobin-A1c-Wert (HbA1c)
- soziale Gesundheitsfaktoren (niedriges Einkommen, unsichere Wohnverhältnisse und fehlende/schlechte Krankenversicherung)
- Medikamente (z.B. Glukokortikoide, Antipsychotika, Checkpoint-Inhibitoren)
- Diabetes Typ 2
- jüngeres Alter
- hyper- oder hypoglykämische Krisen in der Vorgeschichte
- Vorhandensein von Komorbiditäten
- erhöhter HbA1c-Wert
- soziale Gesundheitsfaktoren (niedriges Einkommen, unsichere Wohnverhältnisse und fehlende/schlechte Krankenversicherung)
- Medikamente (z.B. Glukokortikoide, Antipsychotika, Checkpoint-Inhibitoren)
Diagnosekriterien
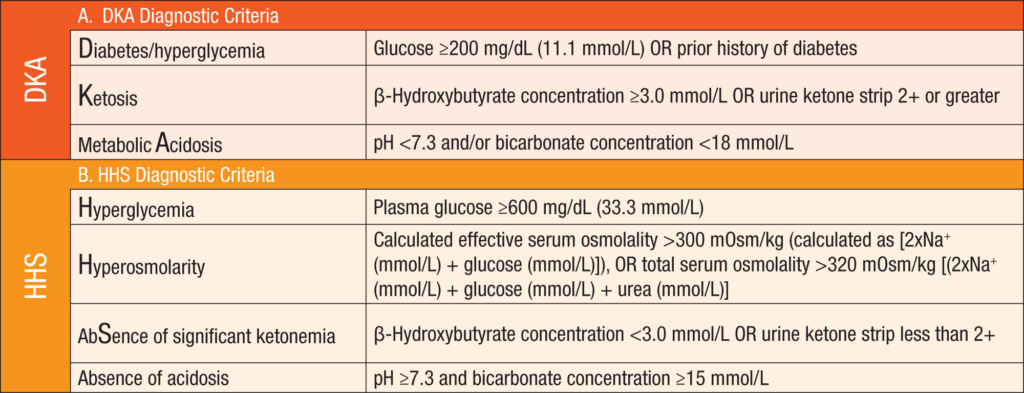
diabetische Ketoazidose
- D – Diabetes/Hyperglykämie (BZ ≥ 200 mg/dL ODER Diabetes in Vorgeschichte)
- K – Ketose (β-Hydroxybutyrat-Konzentration ≥ 3,0 mmol/L ODER Urinketonstreifen 2+ oder größer
- A – metabolische Azidose (pH < 7,3 UND/ODER Bicarbonat-Konz. < 18 mmol/L
- DKA-Klassifizierung & -Schweregrade
| milde DKA | moderate DKA | schwere DKA | |
|---|---|---|---|
| „D“: Diabetes in der Vorgeschichte oder erhöhter Blutzuckerspiegel | BZ: ≥ 200 mg/dL | BZ: ≥ 200 mg/dL | BZ: ≥ 200 mg/dL |
| „K“: Ketonämie | β-Hydroxybutyrate: 3,0 – 6,0 mmol/L | β-Hydroxybutyrate: 3,0 – 6,0 mmol/L | β-Hydroxybutyrate: > 6,0 mmol/L |
| „A“: Azidose | pH > 7,25 – < 7,30 ODER Bikarbonat zw. 15 – 18 mmol/L | – pH > 7,0 – 7,25 – Bikarbonat : 15 – < 18 mmol/L | – pH: < 7.0 – Bikarbonat : < 10 mmol/L |
| Bewusstsein | wach | wach/schläfrig | Stupor/Koma |
| vorgeschlagene Pflegestufe | normalpflegerische oder Beobachtungsstation | Intensivstation oder Intermediate-Care-Station | Intensivstation |
hyperglykämisch hyperosmolarer Zustand
- H – Hyperglykämie
- H – Hyperosmolarität
- S – keine Signifikante Ketonämie (β-Hydroxybutyrat-Konzentration < 3,0 mmol/L ODER Urinketonstreifen 2+ oder kleiner
- (keine Azidose, also pH ≥ 7,3 UND Bicarbonat-Konz. ≥ 15 mmol/L)
Symptomatik
diabetische Ketoazidose
- entwickelt sich über Stunden bis Tage
- normalerweise wach bzw. keine Bewusstseinsstörung
- Polyurie, Polydipsie, Gewichtsverlust & Dehydration
- Übelkeit, Erbrechen & Bauchschmerz (>50 %)
- Kussmaul-Atmung
- fruchtiger Aceton-Geruch der Ausatemluft
hyperglykämisch hyperosmolarer Zustand
- entwickelt sich über Tage bis Wochen
- überlichweise Bewusstseinsstörung
- Polyurie, Polydipsie, Gewichtsverlust & Dehydration
- ggf. Übelkeit, Erbrechen & Bauchschmerz (selten)
- oft als Ko-Erkrankung bei anderen akuten Erkrankungen
Therapie
- kapilläre BZ-Messung alle 1 – 2 h
- Bestimmung von Elektrolyten, Phosphat, Kreatinin, β-Hydroxybutyrat und pH venös alle 4 h (bei HHS zusätzlich Serumosmolarität)
- bei schwerer DKA oder HHS ODER bei kritischen Erkrankung als auslösende Ursache (z. B. Myokardinfarkt, gastrointestinale Blutung, Sepsis) Einweisung auf ITS
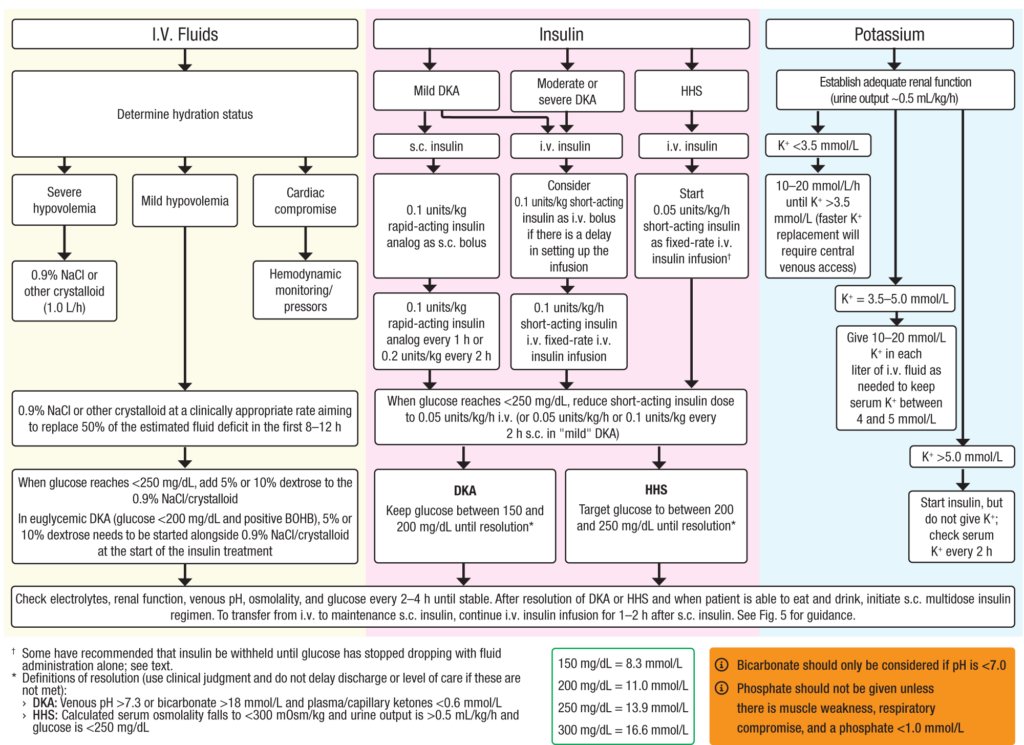
Flüssigkeitstherapie
- Flüssigkeitstherapie i.v. sorgt für erhöhte Gewebe-/Organperfusion (verringerte Laktatbildung), verbesserte Nierendurchblutung (geförderte renale Ausscheidung von Glukose & Ketonkörpern), korrigiertes Elektrolytdefizite & verringerte Plasmaosmolarität sowie korrigierte Insulinsensitivität (Absinken des BZ von ca. 50 – 70 mg/dL/h)
- initial Gabe von 500 – 1.000 mL/h isotonischer Kochsalzlösung (NaCl 0,9 %; CAVE: bei großen Mengen Gefahr einer hyperchlorämischen metabolischen Azidose) oder Vollelektrolytlösung in den ersten 24 – 48 h
- bei DKA sinkt die Plasmaglukosekonzentration i.d.R. in 4 – 8 h auf < 250 mg/dL, also vor dem Abklingen der Ketoazidose –> bei BZ < 250 mg/dL Flüssigkeitatherapie so anpassen, dass diese zusätzlich Glukose 5 – 10 %ig enthält (weitere Therapie anhand von RR, HF, Flüssigkeitsinput/-outputbilanz & Natriumkonzentration ausrichten)
- bei HHS klingt die Hyperglykämie i.d.R. in 8 – 10 h ab (CAVE: nicht schneller als 90 – 120 mg/dL/h)
- Flüssigkeitstherapie soll das geschätzten Defizite innerhalb der ersten 24 – 48 h ausgleichen
- CAVE: bei älteren Erwachsenen, Schwangeren und Personen mit Herz-/Nierenerkrankungen oder anderen schweren Begleiterkrankungen –> Gabe kleinerer Boli (z.B. 250 mL)
Insulintherapie
- Insulintherapie ist Eckpfeiler der DKA-Therapie und sollte so bald wie möglich nach Diagnosestellung erfolgen
- Gabe von kurzwirksamem Insuli i.v. als Dauerinfusion mit einer Laufrate von 0,1 Einheiten/kg/h oder gesteuertem Insulininfusionsprotokoll mit variabler Rate –> sobald BZ < 250 mg/dL wie oben erwähnt Anpassung der Flüssigkeitstherapie mit zusätzlicher Glukose sowie Reduktion der Insulin-Dosis auf 0,05 Einheiten/kg/h –> zuletzt Insulininfusion so anpssen, dass BZ bei etwa 200 mg/dL gehalten wird und dies fortführen bis die Ketoazidose abgeklungen ist
- bei Patient*innen, welche vor Aufnahme Basal-(Bolus-)Insulintherapie erhalten haben, diese in üblichen Dosierung fortsetzen und bei Bedarf anpassen
- bei Patient*innen mit neuer Diabetes-Diagnose nach Abklingen der DKA Beginn der Insulintherapie mit prandialem Insulin sowie Basalinsulin mit 0,15 – 0,3 Einheiten/kg s.c. (danach tägliche Fortführung der Therapie)
- Insulintherapie bei HHS
- bei Vorbehandlung mit Basalinsulin diese Therapie fortsetzen und ggf. anpassen
- bei HHS ohne Ketose oder mit leichter/mäßiger Ketonämie (β-Hydroxybutyrat im Blut ≥ 1,0 bis < 3,0 mmol/L oder Ketone im Urin < 2+) und ohne Azidose (pH ≥ 7,3 und Bikarbonat ≥ 18 mmol/L) Insulininfusionstherapie i.v. mit fester Rate von 0,05 Einheiten/kg/h
- bei signifikanter Ketonämie (d. h. β-Hydroxybutyrat ≥3,0 mmol/L, Ketonurie ≥2+, pH <7,30 oder Bikarbonat <18 mmol/L), also gemischter DKA/HHS, mit Rate von 0,1 Einheiten/kg/h beginnen
Elektrolytausgleich
- Kalium
- trotz Kaliumdepletion (3 – 6 mmol/kg) aufgrund langjähriger osmotischer Diurese, Erbrechen und Hyperaldosteronismus haben die meisten Patient*innen mit DKA einen normalen oder hohen Serumkaliumspiegel
- Insulintherapie, Korrektur der Azidose, Volumengabe & verstärkte Kaliurese senken Serumkalium
- Kaliumspiegel sinkt bei Behandlung von DKA, HHS & gemischter DKA/HHS i.d.R. innerhalb von 48 h nach Aufnahme um 1 – 2 mmol/L
- zur Hypokaliämie-Prävention bei Serumkaliumspiegel < 5,0 mmol/L Gabe von 20 – 30 mmol Kalium pro Liter Flüssigkeit i.v. mit Ziel-Kalium von 4 – 5 mmol/L
- bei 5 – 10 % der Patient*innen mit DKA Kaliumwerte < 3,5 mmol/L –> Kaliumersatz mit Rate von 10 mmol/h & Insulintherapie aufschieben bis Kaliumspiegel > 3,5 mmol/L
- CAVE bei schwerer Hypokaliämie ≤ 2,5 mmol/L, da Mortalität dreifach erhöht
- Serumkalium 2 h nach Beginn der Insulingabe und danach alle 4 h kontrollieren
- Bikarbonat
- keine routinemäßige Bikarbonat-Gabe, da Flüssigkeits- & Insulintherapie i.d.R. ausreichend
- Bikarbonat-Gabe bei schwerer Azidose (pH < 7,0) erwägen –> 100 mmol Natriumbicarbonat (8,4 %) in 400 mL sterilem Wasser (isotonischer Lsg.) alle 2 h bis pH > 7,0
- Phosphat
- keine routinemäßige Phosphat-Gabe, wenn Phosphatwert <1,0 mmol/L
- falls notwendig, 20 – 30 mmol Kaliumphosphat der normalen Flüssigkeitstherapie zugeben
Kriterien für Beendigung von DKA & HHS
- DKA
- Plasmaketone <0,6 mmol/L
- venöser pH-Wertes ≥ 7,3
- Bikarbonats ≥ 18 mmol/L
- Anionenlücke nicht als Beendigungskriterium verwenden
- keine feste Kriterien für HHS-Beendigung
- Serumosmolalität < 300 mOsm/kg
- korrigierte Hyperglykämie (<250 mg/d)
- Urinausscheidung > 0,5 mL/kg/h
- gebesserter Bewusstseinszustand
Komplikationen
- Hypoglykämie
- häufige Komplikation bei der Behandlung von DKA mit Risiko von 16 – 28 % für BZ <70 und 2 % für schwere Hypoglykämie mit <40 mg/dL
- Hypoglykämie (< 40 mg/dL) während Behandlung hat einen 4,8-fachen Mortalitätsanstieg
- bei BZ < 250 mg/dL Reduktion der Insulininfusionsrate auf 0,05 Einheiten/kg/h und Glukose 5 – 10 % der Flüssigkeitstherapie zugeben
- Hypokaliämie
- häufige Komplikation mit Rate von ∼55 % bei DKA- und 51 % bei HHS
- schwere Hypokaliämie <2,5 mmol/L bei 16 % der DKA- und 9 % bei HHS-Patient*innen
- Flüssigkeitstherapie um Kaliumersatz ergänzen
- Thrombose
- keine prophylaktische Gabe von niedermolekularem Heparin, wenn kein V.a. Thrombose besteht
- Hirnödem
- seltene Komplikation bei Erwachsenen (< 0,1 % bei schneller Osmolaritätsverschiebung)
- schwerwiegende Komplikation mit Sterblichkeit von ∼ 30 %
- Prüfung auf potenzielle Risikofaktoren und regelmäßige Überprüfung des Bewusstseins (CAVE: Hirnödem kann subklinisch sein und nur bei Bildgebung sichtbar)
- empfohlene Therapie: Gabe von Mannitol und mechanische Beatmung
- osmotisches Demyelinisierungssyndrom
- früher auch zentrale pontine Myelinolyse
- Auftreten bei schneller Korrektur der Hyponatriämie (unklare Inzidenz)
- bei Abfall der Serumosmolarität Korrektur mit NaCl 0,9 % (Abfall der Serumosmolalität sollte zw. 3,0 – 8,0 mOsm/kg/h liegen)
- akute Nierenschädigung
- gemäß RIFLE-Kriterien (risk, injury, failure, loss) bei ca. 50 % der erwachsenen Patient*innen vorliegend
- häufiger bei älteren Erwachsenen, bei Patient*innen mit höherer Osmolarität und bei Patient*innen mit höheren Aufnahmeglukosespiegeln
- in der Regel durch Rehydrierung behebar (tgl. Überwachung der Nierenfunktion)
Management-Strategien für besondere Bevölkerungsgruppen
- gebrechliche oder ältere Erwachsene
- hoher Anteil mit vorbestehenden Komorbiditäten
- isolierte HHS und gemischte DKA/HHS häufiger als DKA
- Suche nach spezifischen auslösenden Faktoren und Begleitdiagnosen (kardiovaskuläre Ereignisse, Infektionen, Medikamente)
- Therapie: Polypharmazie sowie Komorbiditäten & akute auslösende Ereignisse bei Flüssigkeitstherapie berücksichtigen
- Einnahme von SGLT2-Inhibitoren
- spontanes Auftreten oder durch Reduktion/Weglassen der Insulindosis, längeres Fasten oder akute Erkrankung ausgelöst
- kann bei nahezu normalem BZ oder euglykämischer DKA (Glukose < 200 mg/dL auftreten
- Therapie: wie bei „allgemeiner“ DKA (bei euglykämischer DKA Glukose 5 – 10 % der Flüssigkeitstherapie zusetzen oder gleichzeitig mit NaCl 0,9 % beginnen) sowie SGLT2-Hemmer absetzen
- Nierenerkrankung im Endstadium
- ca. 4 % der Patient*innen mit Diabetes & Nierenerkrankung im Endstadium haben DKA/HHS
- Patient*innen mit Nierenerkrankungen im Endstadium weisen in der Regel eine stärkere Hyperglykämie, häufigere Hyponatriämie, höhere Osmolalität, Hyperkaliämie und niedrigere Ketonkonzentrationen von β-Hydroxybutyrat auf
- Therapie: kontrollierte Flüssigkeitszufuhr und Kaliumersatz
- Schwangerschaft
- bei bis zu 2 % der Schwangerschaften mit Schwangerschaftsdiabetes entwickeln DKA (i.d.R. bei vorbestehendem Diabetes Typ 1; Inzidenz von < 0,1 %)
- euglykämische DKA (Glukose < 200 mg/dL) möglich
- sofortiges Eingreifen durch erfahrene Ärzt*innen & Geburtshelfende, da erhebliches feto-maternale Risiko (i.d.R. Therapie im Kreißsälen oder auf Intensivstation)
- COVID-19
- höhere Häufigkeit von DKA während COVID-19-Pandemie (Risikogruppe: Erwachsene mit vorbestehendem Diabetes Typ 2)
- höhere Häufigkeit von gemischter DKA/HHS, v.a. bei älteren Erwachsenen
- Behandlung mit hochdosierten Steroiden erfordert höhere Insulindosis zur Behandlung der refraktären Ketonämie
- Diabetes-Phänotypisierung bei neu diagnostiziertem Diabetes hilfreich


Sei der Erste der einen Kommentar abgibt